
1 个月前

1 个月前
每次你体内的细胞分裂,都要精准复刻30亿个碱基对的DNA——这是生命最基础的流水线作业。四十年来,教科书都写着:复制因子C(RFC)是个“一次性装卸工”,把环形的PCNA滑动夹套上DNA就功成身退,剩下的复制工作全交给PCNA和聚合酶。但2026年初发表在《细胞》的研究,把这个定论彻底推翻了:RFC根本没走,它套上PCNA后就黏在上面,跟着整个复制机器沿DNA一路滑到底,成了维持复制稳定的“隐形支架”。为什么这个发现值得改写教科书?它藏着癌症和神经疾病的分子线索吗?
你可以把DNA复制想象成给火车轨道铺新钢轨:PCNA是套在轨道上的“滑套”,把负责铺轨的聚合酶死死扣在轨道上,避免它中途掉链子;而RFC原本被认为是“开套人”,掰开PCNA的环套到轨道上,就转身去打下一份工。 但O’Donnell团队用单分子光阱技术,把一根DNA链拴在两个激光固定的微珠之间,给RFC和PCNA分别染上绿光和红光——当两种蛋白一起移动时,荧光会重叠成黄色。他们亲眼看到:RFC把PCNA套上DNA后,绿光和红光始终黏在一起,跟着聚合酶以每秒数百个碱基的速度滑过DNA。
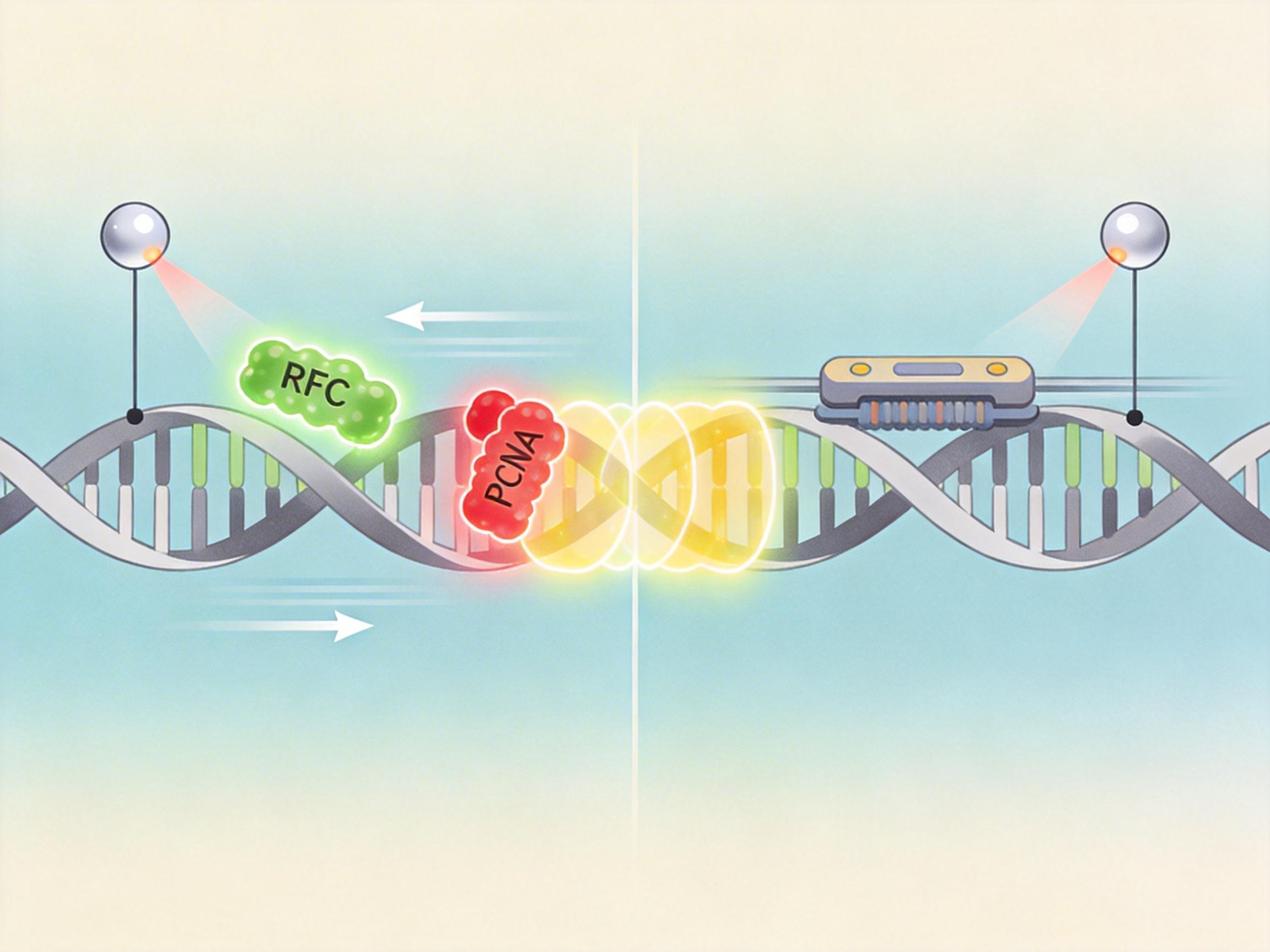
研究人员做了个突变实验:把RFC上负责“黏住”PCNA的BRCT结构域删掉,结果聚合酶像个没站稳的工人,频繁从PCNA上脱落,复制速度直接慢了一半,细胞对DNA损伤的敏感度也大幅上升。这说明RFC的新身份,是维持复制机器稳定的“结构性支架”——它不需要再“干活”,只要待在那儿,就能让整个复制流水线不崩溃。
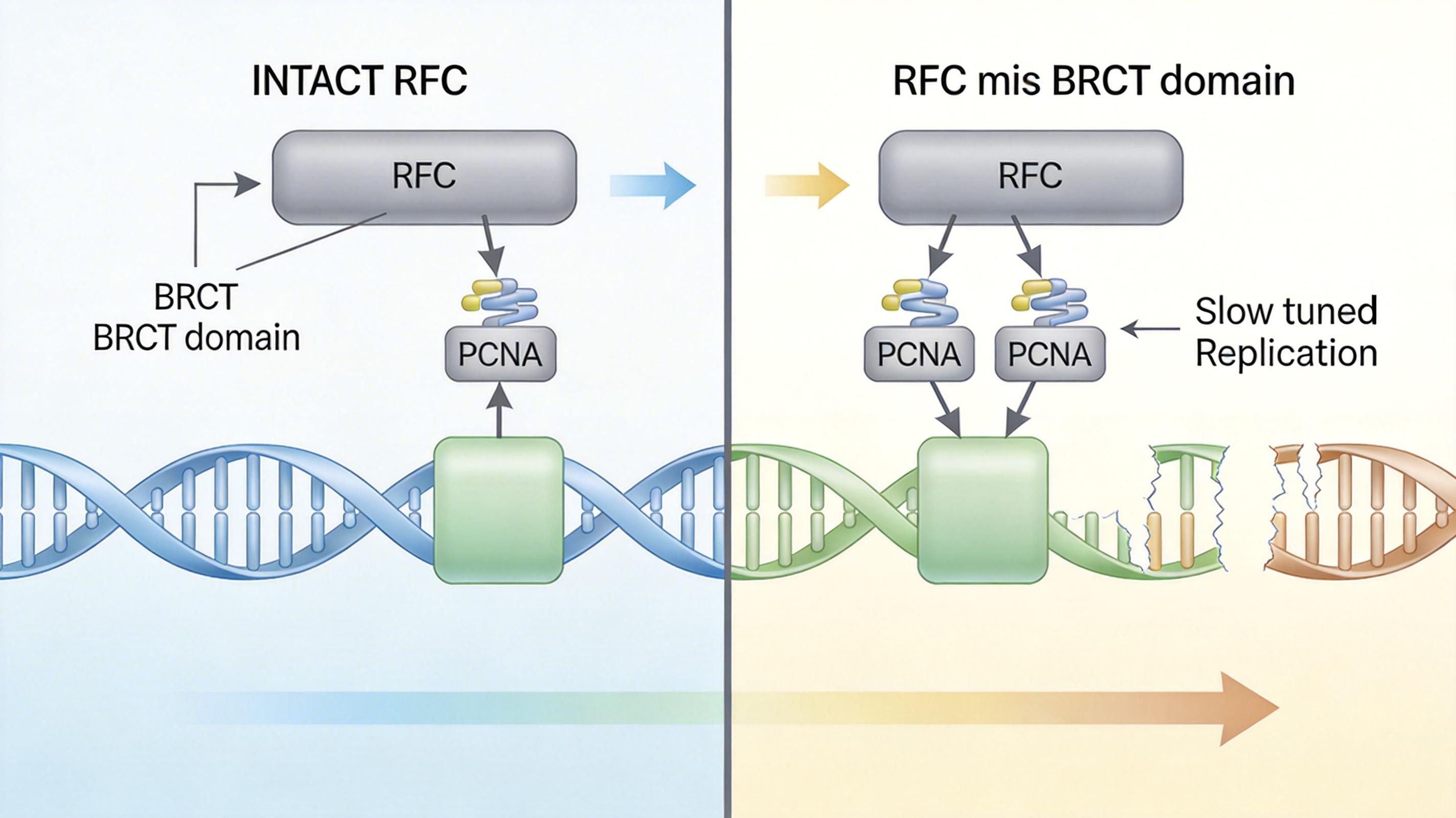
更有意思的是,细胞给这个“支架功能”上了双保险。除了RFC,另一种叫FEN1的酶也能起到类似的黏合作用——它原本的工作是切除复制时留下的“小尾巴”,但研究发现,当RFC的支架功能失效时,FEN1能顶上去,继续稳住PCNA和聚合酶的复合物。
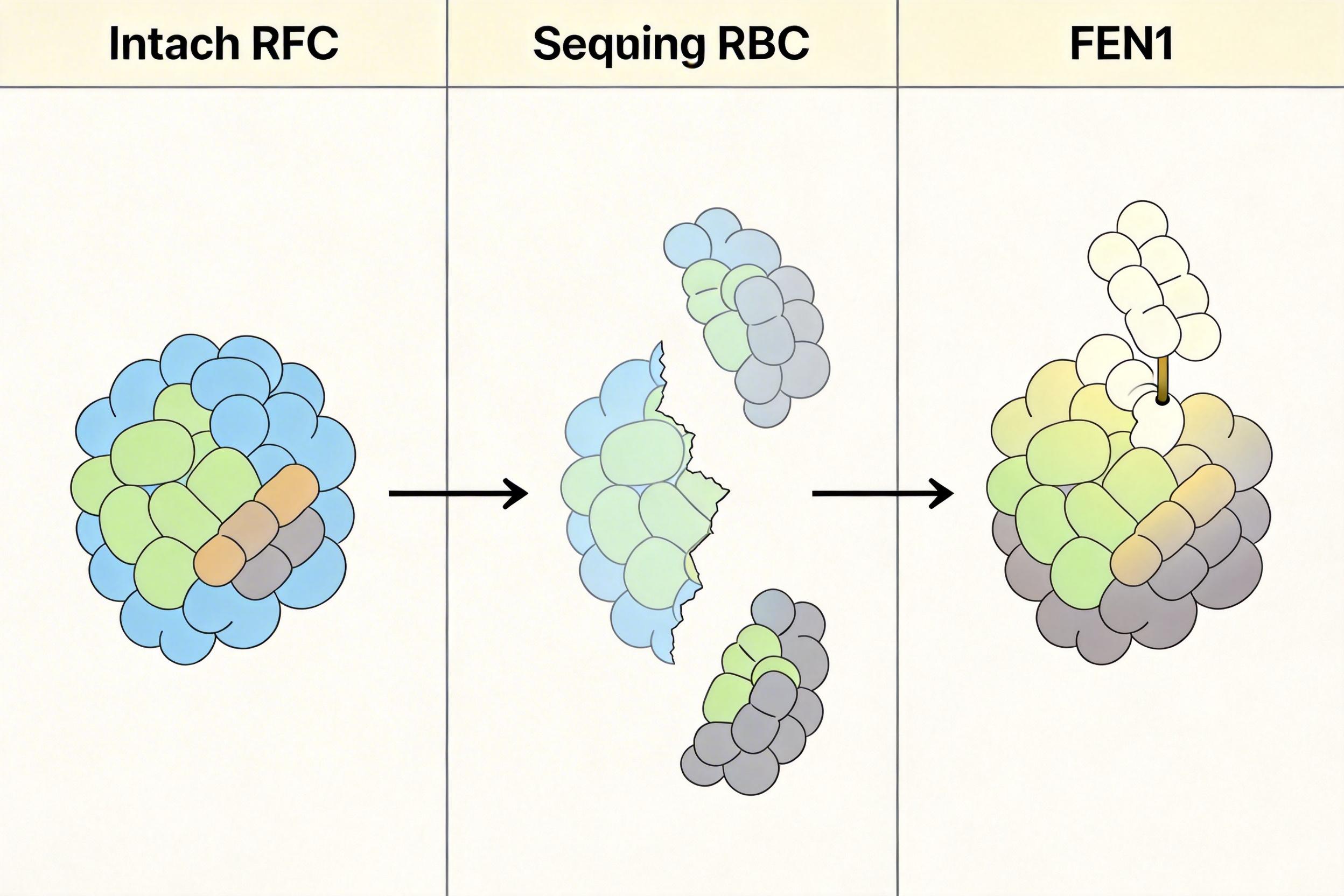
实验室在酵母里验证了这个结论:如果只削弱RFC的黏合能力,酵母还能勉强活下去;但同时让FEN1失活,细胞立刻就死了。这种“冗余设计”说明,维持复制机器的稳定性,对细胞来说是生死攸关的大事。 反过来想,如果这个支架功能出了问题,细胞复制DNA时就会频繁出错,基因组稳定性被打破——这正是癌症和部分神经系统疾病的核心诱因。比如,当RFC的BRCT结构域突变,细胞修复DNA损伤的能力会大幅下降,突变积累的速度加快,癌变的风险也就随之升高。而针对这个新发现的靶点,未来或许能开发出更精准的抗癌药物:比如只阻断肿瘤细胞里RFC的支架功能,让它们的复制机器崩溃,却不影响正常细胞的复制。
这个发现还戳破了一个生物学的老偏见:我们总习惯把蛋白质当成“专一的工具”——比如RFC就是“加载器”,FEN1就是“切割酶”,只看它们的催化功能。但实际上,很多蛋白质的“非催化功能”,才是维持生命活动的关键。 就像RFC,它的本职是“开环加载”,但“黏合支架”这个“副业”,对复制的稳定性贡献更大;FEN1的本职是“切割尾巴”,但“替补支架”这个“副业”,是细胞的救命保险。研究人员统计发现,人类蛋白质组里约3%的“多功能蛋白”,往往是细胞调控网络的核心节点,也是疾病的关键靶点——它们就像身兼数职的“超级员工”,一旦出问题,整个系统都会瘫痪。 更重要的是,这些“非催化功能”往往藏在蛋白质的无序区域或特定结构域里,以前很容易被忽略。这次RFC的发现,相当于给生物学家提了个醒:别再只盯着蛋白质的“本职工作”了,它们的“副业”里,可能藏着生命最核心的秘密。
四十年前,O’Donnell团队首次发现PCNA是套在DNA上的“滑动夹”,改写了教科书;四十年后,他们又发现RFC的“隐形支架”功能,再次刷新了我们对DNA复制的理解。 这正是生命科学最迷人的地方:我们以为已经摸透了最基础的生命过程,却总能在最熟悉的角色里,发现全新的身份。就像RFC,从“一次性装卸工”到“隐形支架”,它的功能从未改变,只是我们终于看清了它的全貌。 蛋白质的价值,远不止于它的本职工作。这个发现不仅让我们重新认识DNA复制,更让我们意识到:生命的复杂性,往往藏在那些被忽略的“细节”里——而那些细节,或许就是解开疾病谜团的关键。
点击充电,成为大圆镜下一个视频选题!