对抗知识焦虑,从看懂这条开始
App 下载
迷你肝脏获生命线:血管化突破开启肝病新纪元?
三维培养|肝脏疾病|血管化|干细胞|肝脏类器官|再生医学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
三维培养|肝脏疾病|血管化|干细胞|肝脏类器官|再生医学|医学健康
肝脏,是人体内沉默的化工厂,昼夜不息地执行着超过500种生命必需的功能。然而,当酒精、病毒或代谢紊乱悄然侵蚀它时,这座工厂便会走向衰败,最终导致肝硬化乃至肝癌。几十年来,科学家们试图在培养皿中重建这座复杂的“生命之城”,以窥探疾病的秘密并寻找解药。他们成功培育出了“肝脏类器官”——一种由人类干细胞自组装形成的微型三维肝脏模型。
这曾被誉为一场革命。然而,这些微型肝脏却始终存在一个致命缺陷:它们是一座座没有道路与管网的孤城。它们缺乏功能性的血管网络,无法有效输送营养、氧气和排出废物。随着体积稍稍增大,其核心区域便会因缺氧而坏死。这不仅限制了它们的尺寸和寿命,更使其无法真实模拟人体内肝脏复杂的生理功能与病理过程。这个“血管化”的瓶颈,如同一道天堑,阻碍了肝脏类器官从实验室走向临床的步伐。
直到现在,这道天堑终于被一道曙光撕开。
2025年12月5日,一篇发表在国际顶级期刊《Advanced Science》上的研究,宣告了一个里程碑式的突破。由上海中医药大学的葛广波、郭兆彬团队与柏林夏里特医学院的Liu Hanyang团队共同完成的这项工作,成功构建了一种新型的、功能完备的血管化人类肝脏类器官(Vascularized Human Liver Organoids, 简称3HLOs)。
这不仅仅是为微型肝脏添加了几根“管道”,而是真正赋予了它与外界沟通的“生命线”。研究团队通过一种创新的多细胞共培养策略,将三种关键细胞巧妙地融合在一起,让它们在三维空间中协同作战,最终“编织”出一个兼具肝脏功能和精密血管网络的活体结构。这一成果不仅解决了长期困扰该领域的“血管化”难题,更在肝病建模、药物筛选和再生治疗三个维度上展现了惊人的潜力,预示着一个肝脏研究与治疗新纪元的到来。
过去,构建肝脏类器官的尝试之所以屡屡受挫,核心在于细胞来源的局限性和细胞间相互作用的缺失。传统的肝细胞在体外极难维持功能,而由诱导多能干细胞(iPSCs)分化而来的肝细胞则面临成熟度不足和潜在的致瘤风险。
此次研究的精妙之处,在于组建了一支前所未有的“细胞梦之队”:
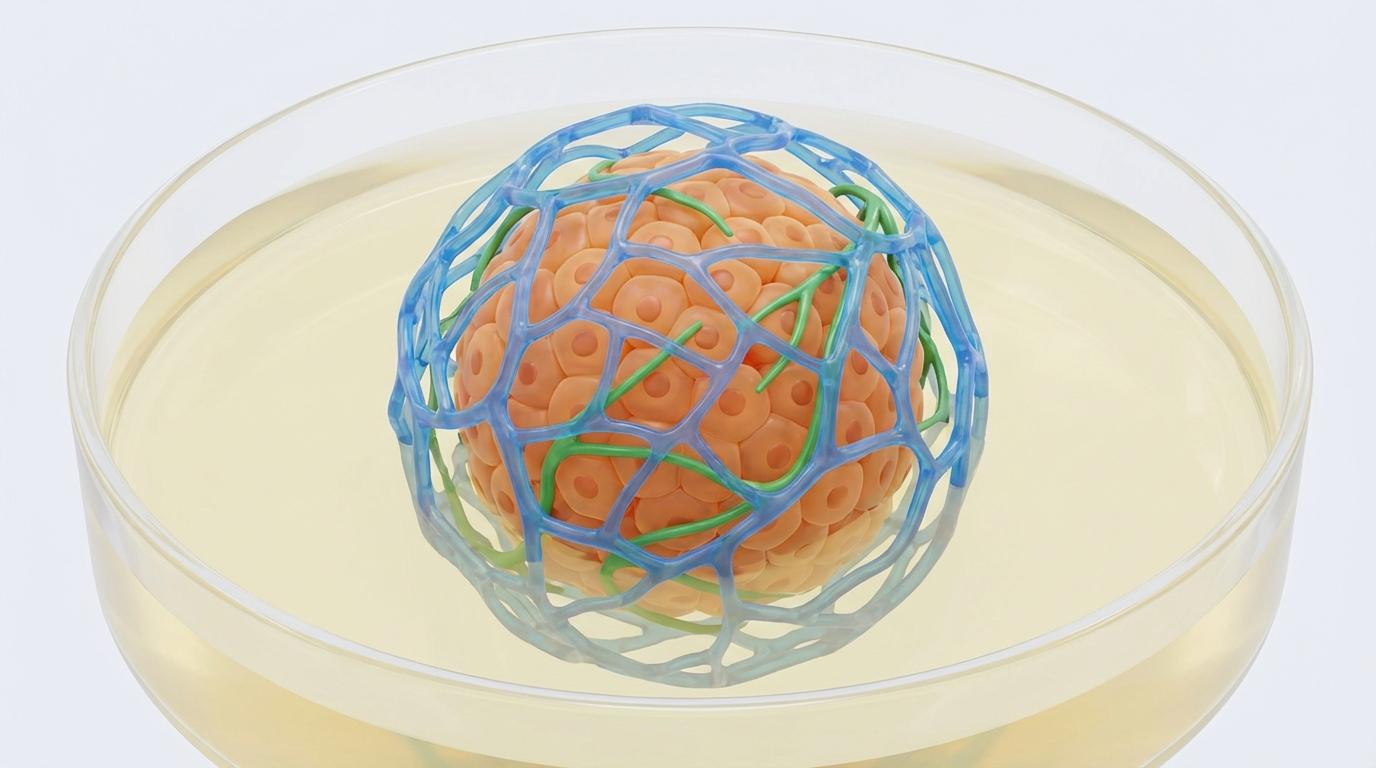
当这三种细胞在特制的培养体系中相遇,奇迹发生了。它们并非杂乱无章地堆砌,而是在内在信号的引导下,自发地组织成一个高度有序的结构:hrHLs构成了肝功能的核心,HUVECs则围绕其形成了由CD31⁺蛋白标记的内皮网络,甚至还出现了由CK19⁺蛋白标记的胆管结构。一个拥有“血管系统”和“胆管系统”雏形的微型肝脏,就此诞生。
拥有了血管系统,意味着这个微型肝脏能够更好地模拟真实的人体环境。为了验证其作为疾病模型的潜力,研究团队构建了一个“芯片上的3HLOs”平台,将其置于微流控芯片中,精准模拟酒精对肝脏的持续性伤害。
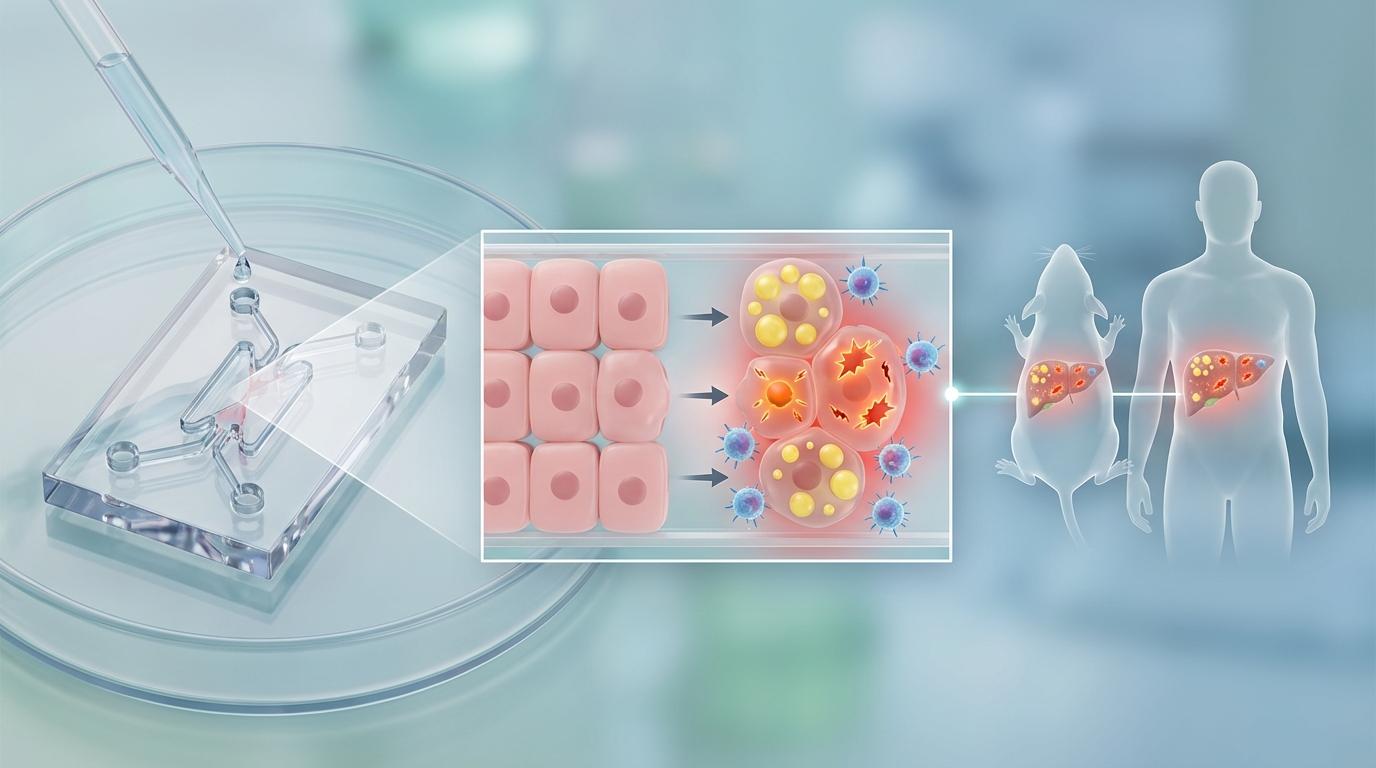
结果令人振奋。在酒精的刺激下,这个“芯片肝脏”完美复刻了**酒精性肝损伤(ALI)**的关键病理特征,包括肝细胞的脂肪变性、氧化应激和炎症反应。其各项指标的变化趋势与在动物模型甚至临床患者身上观察到的现象高度吻合。这意味着,科学家们终于拥有了一个高保真度的体外平台,可以在培养皿中“预演”酒精性肝病的发生发展过程。
这一平台的现实意义是巨大的。它将彻底改变肝病药物的筛选模式。过去,大量候选药物因动物实验与人体结果差异巨大而失败。如今,研究人员可以直接在源自人类细胞的、高度仿生的“芯片肝脏”上进行高通量测试,从而以更快的速度、更低的成本、更高的准确率筛选出真正有效的保肝药物,加速新药研发进程。
如果说精准建模是这项技术的“盾”,那么再生治疗就是它最锋利的“矛”。研究团队将目光投向了终末期肝病这一临床绝境,探索3HLOs作为一种“活体疗法”的可能性。
他们将培养好的3HLOs皮下植入到患有终末期酒精性肝损伤的小鼠体内。接下来发生的事情,堪称再生医学的奇迹:
这并非简单的细胞替代,而是一种更高级的“系统级修复”。3HLOs通过与宿主建立循环连接,远程调控其生理状态,最终唤醒了机体自身的修复潜能。这一发现为治疗肝衰竭等重症肝病提供了一种全新的、极具想象力的策略,未来甚至可能成为替代肝移植的重要选项。
上海中医药大学团队的这一突破,是类器官领域、乃至整个再生医学领域的一座分水岭。它标志着我们已经从构建器官的“静态模型”,迈向了创造具有动态循环和治疗功能的“活体组织”的新阶段。
当然,从实验室的成功走向广泛的临床应用,依然有很长的路要走。标准化、规模化生产、长期安全性验证以及伦理监管等,都是未来必须攻克的难题。然而,方向已经无比清晰:
这场始于培养皿的革命,最终指向的是人类健康的未来。当微小的“迷你肝脏”第一次在体外拥有了自己的生命线,它所连接的,是基础研究与临床应用之间的桥梁,是工程学与生命科学的深度交融,更是千千万万肝病患者对新生的期盼。