对抗知识焦虑,从看懂这条开始
App 下载
给大脑细胞装上千个开关,我们找到了治阿尔茨海默病的新靶点
小鼠模型|基因调控网络|阿尔茨海默病新靶点|星形胶质细胞|神经退行性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
小鼠模型|基因调控网络|阿尔茨海默病新靶点|星形胶质细胞|神经退行性疾病|医学健康
你或许没听过星形胶质细胞,但它是大脑里数量最多的“隐形管家”——给神经元送营养、清垃圾、维持环境稳定,甚至悄悄调控记忆形成。过去几十年,科学家们只能通过单个基因的敲除或过表达,像摸盲盒一样试探它的功能,更别提在生病的大脑里看清它的变化。直到2026年4月,一支中国团队在《Science》上发表的研究,把这扇门彻底推开了:他们给小鼠大脑的星形胶质细胞一次性装上了近千个“开关”,在活体里全景式测绘出了这些细胞的调控网络,还顺手揪出了一个能逆转阿尔茨海默病症状的关键靶点。这到底是怎么做到的?
你可以把传统的星形胶质细胞研究想象成:在黑屋子里,一次只能摸一个盲盒,还不知道盒子里的玩具在整个房间里能发挥什么作用。而这次团队开发的iGOF-Perturb-seq技术,就是给黑屋子装上了全景灯,还把所有盲盒的说明书一起递了过来。
这套系统的核心是三个环节:首先是打造一个“转录因子工具箱”——把近千个能调控基因表达的关键蛋白的编码序列,分别贴上独一无二的分子条码;然后用改造过的腺相关病毒当“快递员”,精准把这些“开关”递送到小鼠大脑的星形胶质细胞里,强制让每个细胞只打开一个“开关”;最后用单细胞测序技术,给每个被“扰动”的细胞做一次全基因表达的“体检”,通过条码对应上每个“开关”打开后引发的连锁反应。
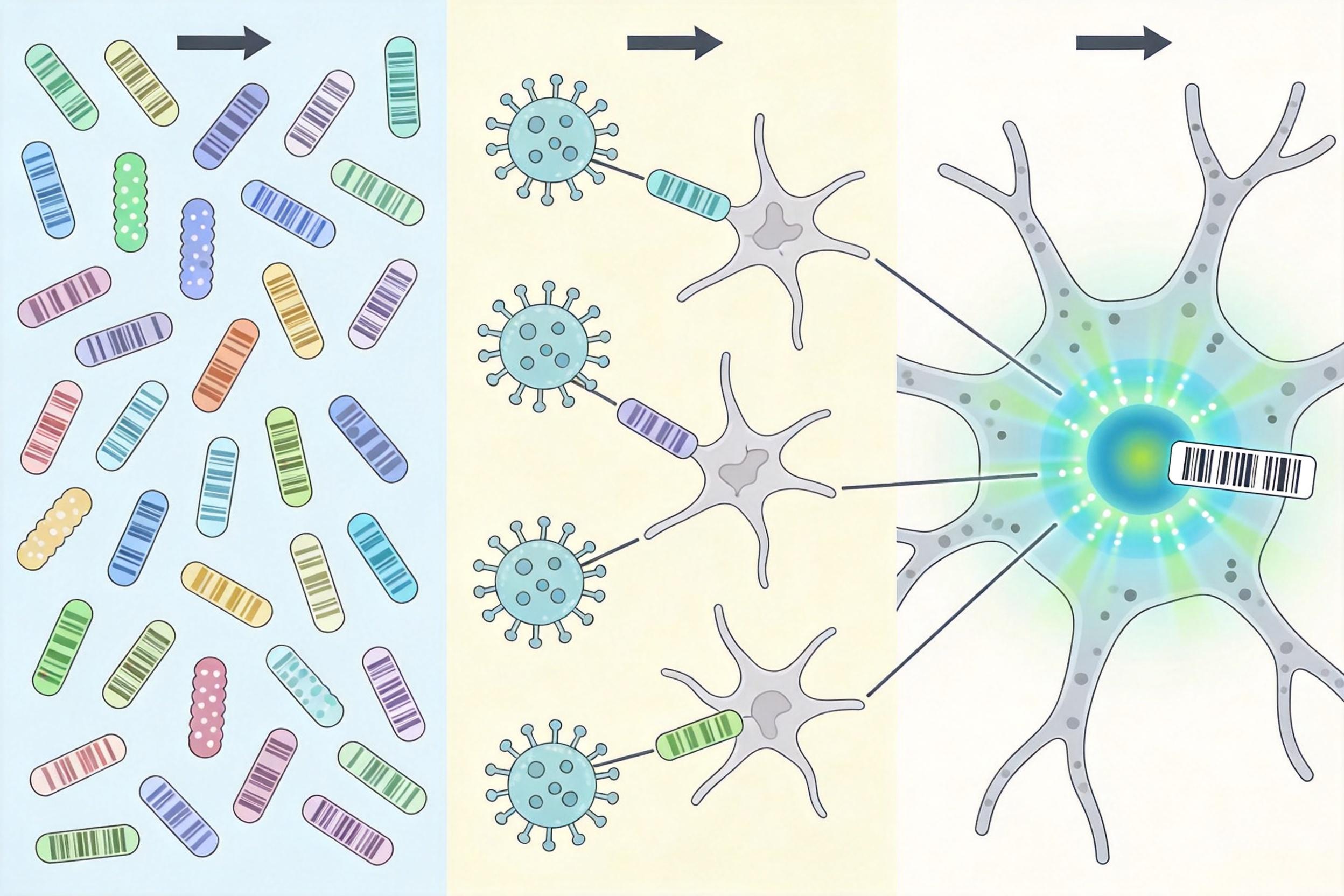
和传统方法比,这是从“管中窥豹”到“全景测绘”的跨越:以前在培养皿里研究的细胞,早就失去了大脑里的复杂环境;一次只能研究一两个基因的方法,永远拼不出完整的调控网络。而iGOF-Perturb-seq首次实现了在活体大脑里,一次性给近千个基因做“功能增强”测试,每个测试都在真实的脑环境中完成。
有了这套工具,团队先在健康小鼠的大脑里完成了第一轮筛选,绘制出了星形胶质细胞的第一张“转录因子功能图谱”。通过分析近千个“开关”打开后的细胞变化,他们发现这些转录因子并不是各自为政:有的形成了“代谢调控小组”,专门管细胞的能量供应;有的组成了“炎症反应小队”,负责应对外来刺激;还有的是“发育指挥家”,决定细胞的成熟方向。
更重要的是,他们把这套工具用到了阿尔茨海默病的小鼠模型里。在生病的大脑里,星形胶质细胞会从“管家”变成“破坏者”——释放炎症因子、攻击神经元、加重认知损伤。团队通过对比健康和患病大脑的筛选数据,再结合人类患者的基因数据库,很快锁定了一个叫Ferd3l的转录因子。
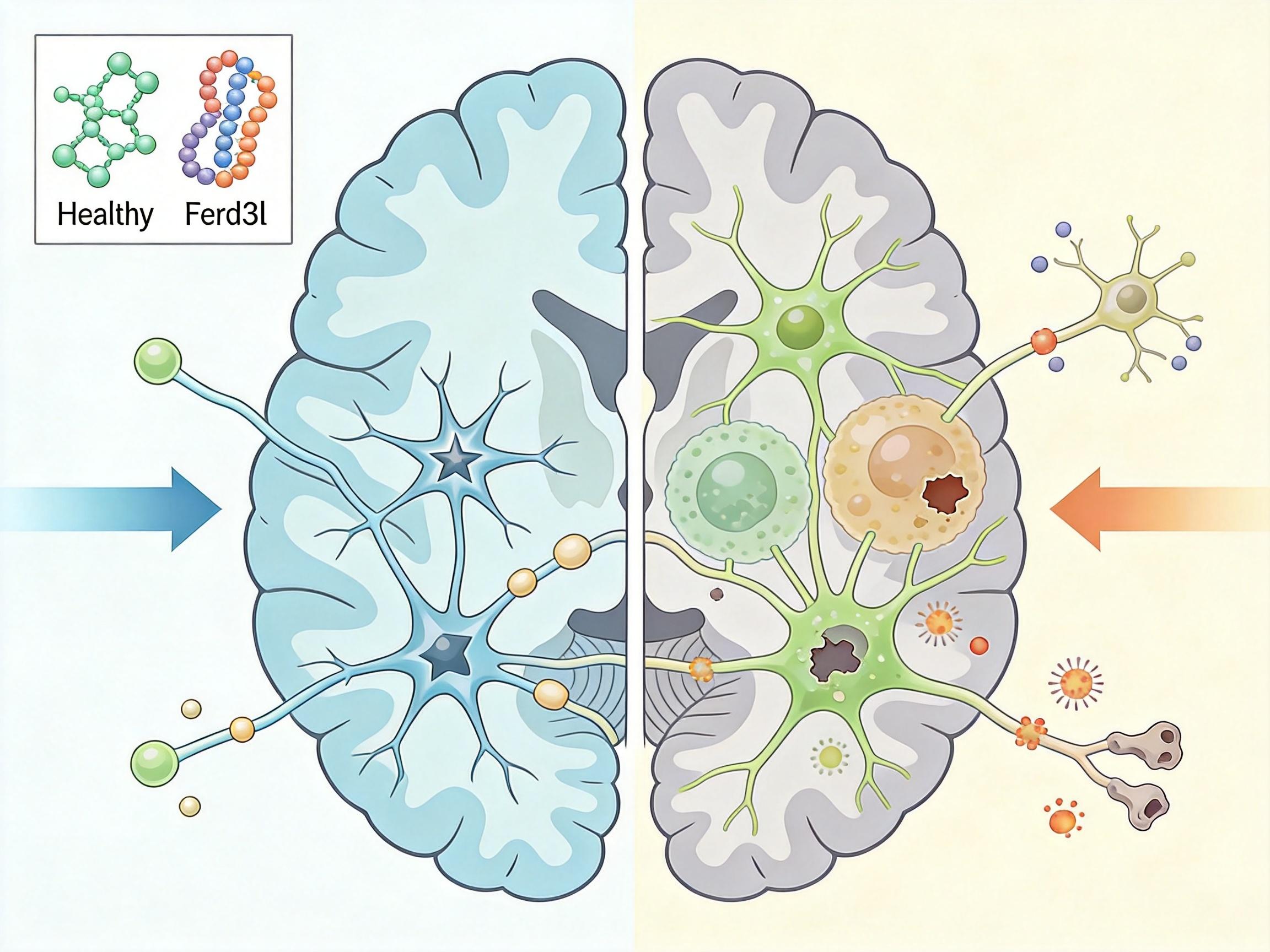
这是一个只在星形胶质细胞里活跃的“开关”。当团队在患病小鼠的大脑里强制打开这个“开关”后,神奇的事情发生了:原本处于“狂暴状态”的星形胶质细胞平静了下来,炎症因子的分泌大幅减少,神经元的损伤得到了抑制,甚至小鼠的认知测试成绩也明显提升了——就像给失控的细胞拉了一次紧急刹车。
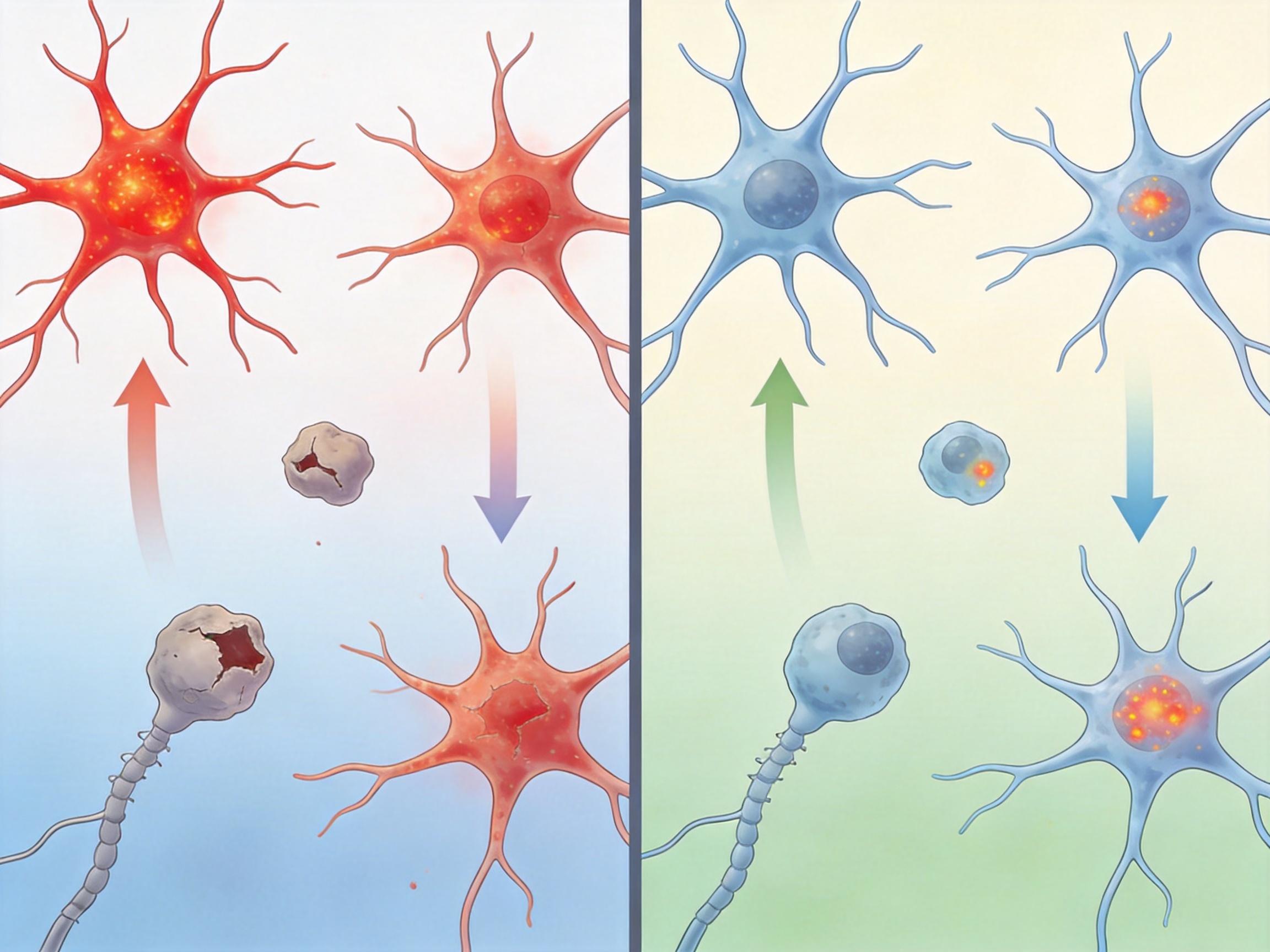
当然,这项技术也不是完美的。目前它还只能在小鼠大脑里实现高效递送,要用到人类身上,还得解决病毒载体穿越血脑屏障的效率问题;近千个转录因子的筛选虽然已经是大规模,但人类基因组里还有更多的调控蛋白等待测试;而且Ferd3l的神经保护作用还需要在更接近人类的模型里验证,距离真正的药物还有很长的路要走。
但不可否认的是,iGOF-Perturb-seq给神经科学研究打开了一扇新的大门。以前我们研究大脑疾病,大多盯着神经元,现在这套工具让我们能系统地研究星形胶质细胞这个“沉默的大多数”;以前我们找治疗靶点,靠的是一个个试错,现在我们可以在活体里一次性筛选出几百个潜在靶点。
更重要的是,这套技术不止能用来研究阿尔茨海默病。未来它还可以被用到帕金森病、抑郁症、脑损伤等更多神经系统疾病的研究中,甚至能扩展到心脏、肝脏等其他器官的细胞调控网络研究。
当我们谈论大脑时,总习惯把目光投向神经元——那些负责传递电信号的“主角”。但这次的研究让我们看到,那些默默支撑的“配角”,可能才是解开疾病谜团的关键。
看见沉默的细胞,才能读懂完整的大脑。 这句话或许能概括这项研究的真正价值:它不仅给我们找到了一个治疗阿尔茨海默病的新靶点,更给了我们一套读懂大脑“隐形管家”的方法。未来,当我们再面对复杂的神经系统疾病时,不用再像摸盲盒一样试错,而是可以拿着一张清晰的地图,精准找到那个能扭转局面的“开关”。