
3 天前

3 天前
想象一下:你手里攥着一把能精准杀死癌细胞的钥匙,可它插进锁孔后,要转三个小时才能锁住——等它生效,钥匙早被身体的代谢系统冲走了。这就是共价蛋白药物研发卡了十年的死局:这类药物能和靶点牢牢焊死,疗效持久,但结合速度慢到赶不上自身被清除的速度。
2026年4月,西湖大学的实验室里,这个死局被一把「快进键」打破。党波波、周挺团队开发的高通量筛选平台,第一次让共价蛋白的结合速度追上了体内代谢的节奏——原本要花几小时的结合,现在只要几分钟。这背后,是一场把分子级的「慢动作」硬生生加速成「快进镜头」的科学革命。为什么之前没人做到?这得从药物和靶点的「约会规则」说起。
你可以把共价蛋白药物和靶点的结合,看成一场需要精准时机的约会:药物得先靠亲和力「黏」在靶点身边(非共价结合),再用自带的化学「焊枪」(弹头)和靶点焊在一起(共价结合)。要快,就得同时满足三个苛刻条件:黏得牢、焊枪位置准、周围环境还得能帮着「点火」。
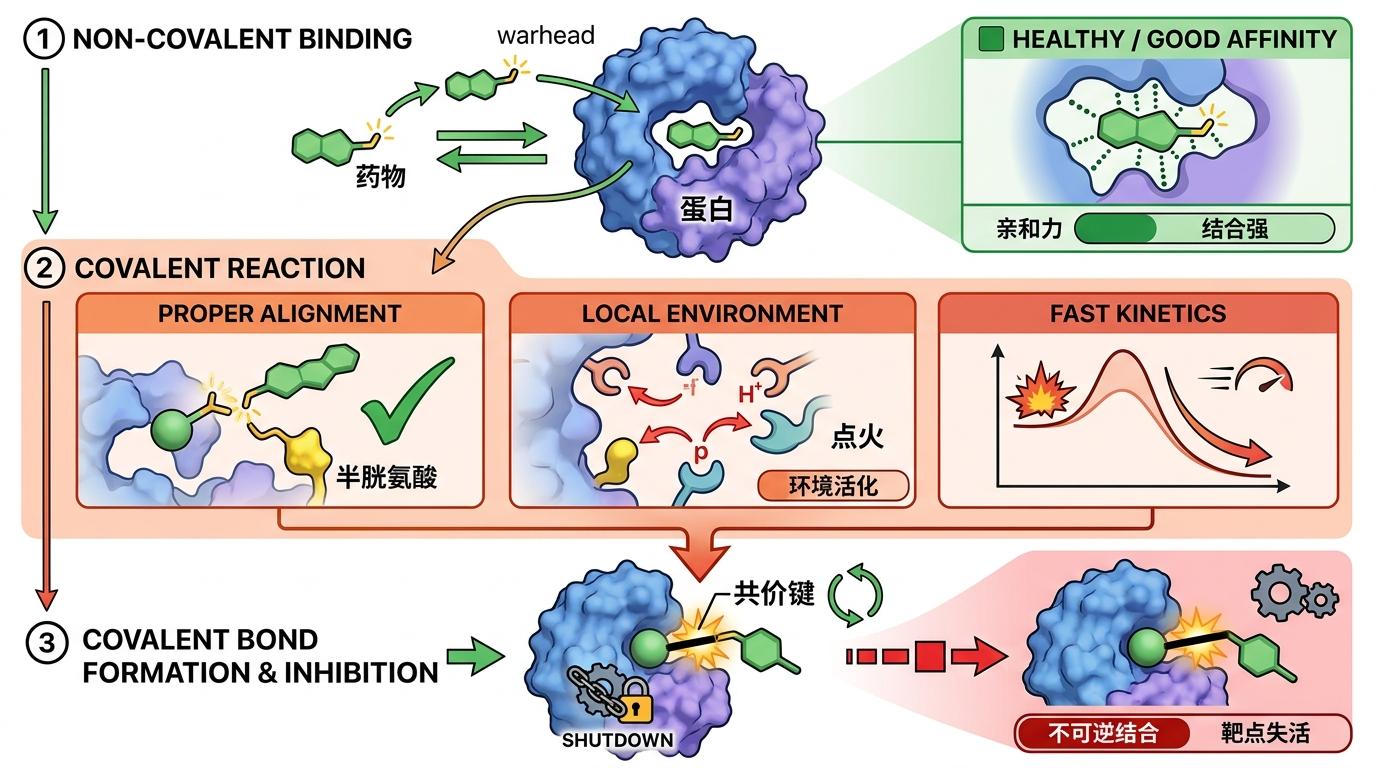
之前的研发者只能像拆盲盒一样试:换个弹头位置,或者改改旁边的氨基酸残基,一次只试一两个变量,效率低得像用勺子挖井。常用的氟硫酸盐弹头为了避免乱焊,天生反应性弱,要焊牢就得等几小时——可这类小蛋白药物在体内的半衰期通常不到30分钟,等焊上的时候,大部分药物已经被肾脏滤走了,相当于约会还没开始,人已经被拉走了。
西湖大学的团队换了个思路:既然单个试太慢,那就把所有可能的「约会对象」都请来,一次筛选几百万个。他们用酵母表面展示技术,把几百万种蛋白变体「贴」在酵母细胞表面,每个酵母都是一个带着不同「约会方案」的候选人。再用化学生物学方法给每个候选人装上焊枪,然后用流式细胞术快速筛选——谁能在几分钟内和靶点焊牢,谁就留下。
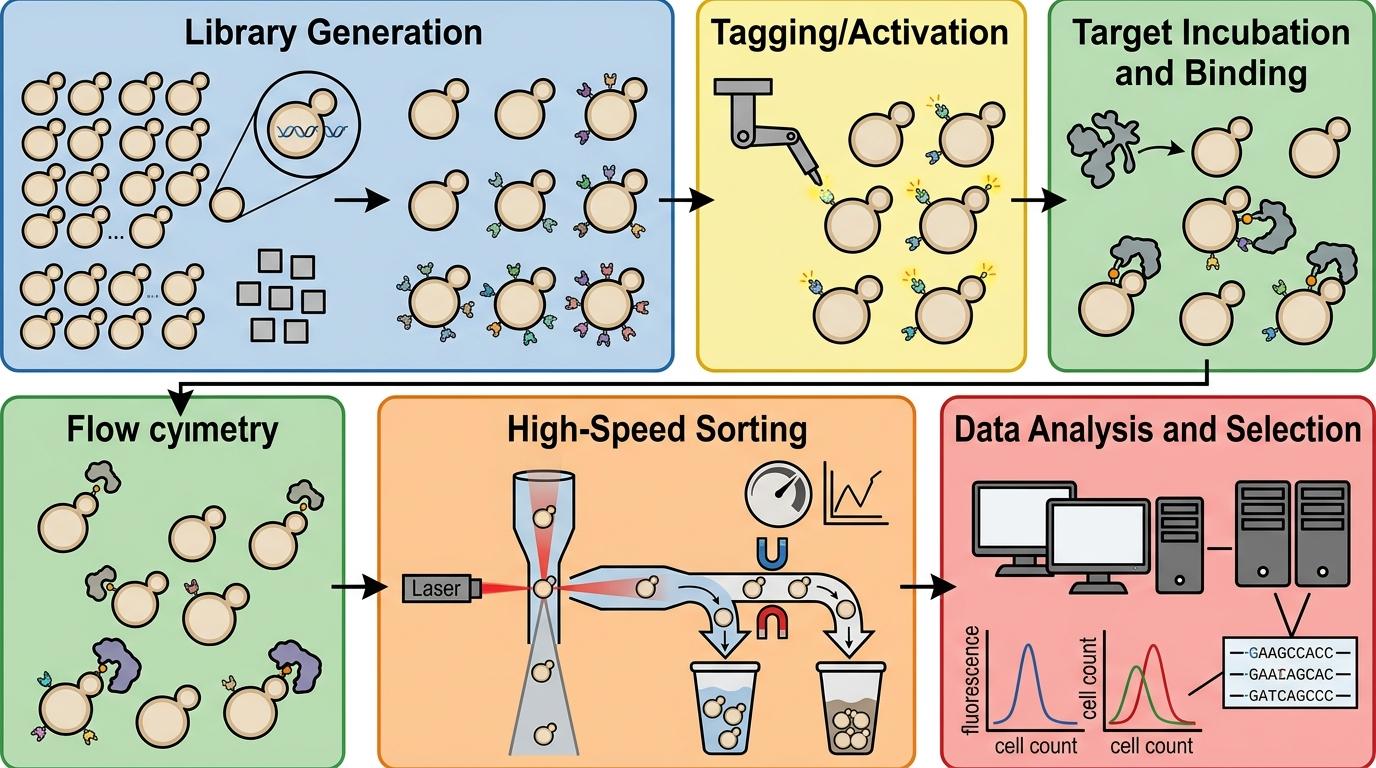
这个过程像给几百万个同时相亲的人拍快照,瞬间找出那个能一秒牵手的人。而且他们不用提高焊枪的反应性(避免乱焊),只靠优化蛋白的结构和焊枪的位置,就让结合速度快了几十倍。
这套高通量平台的厉害之处,在于它把「慢变量」变成了「可筛选的快参数」。团队用它筛出的PD-L1共价纳米抗体IB101,结合半衰期只有3.8分钟——意思是每3.8分钟就有一半药物和靶点焊牢。在小鼠肿瘤模型里,它的抗肿瘤效果比已经上市的临床抗体还要好,而且因为能快速焊牢,即使体内代谢快,依然能让靶点长时间被锁住。
他们还筛出了IL-18共价变体IB201,能快速和受体焊死,增强免疫信号,而且没有明显的系统毒性。针对新冠病毒的共价小蛋白更是能和病毒刺突蛋白牢牢焊住,对多种变异株都有效——就像给病毒的钥匙孔焊了个塞子,再也开不了门。
更重要的是,这是一套通用的方法。不管是抗肿瘤的免疫检查点抑制剂,还是抗病毒的中和蛋白,只要换个靶点,就能用这套平台快速筛选。之前研发这类药物可能要花几年,现在几个月就能得到候选分子。
当然,它也不是完美的。目前筛选出的药物还需要更多的体内安全性验证,比如会不会不小心焊到不该焊的蛋白上(脱靶效应),长期使用会不会引发免疫反应。而且这套平台的筛选规模虽然大,但还是依赖酵母表达系统,一些复杂的蛋白可能没法展示。但不可否认的是,它给共价蛋白药物的研发打开了一条快进通道——之前要翻山越岭才能到的地方,现在可以坐高铁了。
这场技术突破的背后,是药物研发思路的转变:从「试错优化」转向「高通量筛选」,从「单个变量调整」转向「系统优化」。未来,这套平台还可以和AI结合,让计算机先预测哪些蛋白变体可能有更快的结合速度,再用实验验证,进一步提高筛选效率。
还有一个值得关注的方向,是拓展可焊的靶点范围。之前的共价药物主要盯着半胱氨酸残基焊,现在团队用的氟硫酸盐弹头还能焊赖氨酸、酪氨酸等残基,相当于把能约会的对象从一个小圈子扩大到了整个社交圈。这意味着一些之前没法用共价药物靶向的「不可成药」靶点,现在也有了希望。
从更长远的角度看,共价蛋白药物的优势在于它能「持久起效」——一旦焊牢,靶点就一直被锁住,不用频繁给药。对于癌症、自身免疫病这类需要长期治疗的疾病,这能大大降低患者的给药负担,也能减少耐药性的产生。而快速结合的能力,让这种持久起效的优势终于能真正发挥出来。
当我们谈论药物研发的突破时,往往只关注「有没有」,却忽略了「快不快」。很多时候,不是药物没用,而是它起效的速度赶不上身体的代谢速度——就像消防员赶到时,房子已经烧完了。
西湖大学的这套平台,本质上是给药物和靶点的「约会」加了个快进键,让疗效能在身体把药物清除前发挥出来。「快结合,才是真有效」,这不仅是共价蛋白药物的破局点,也是整个药物研发领域的一个重要提醒:有时候,解决问题的关键不是发明新工具,而是把现有工具的效率提到极致。
未来,当更多这类快速结合的共价蛋白药物走进临床,那些之前因为代谢太快而被放弃的候选药物,可能会重新焕发生机。而这场发生在西湖大学实验室里的分子级加速,最终会变成病床前的希望——让药物的疗效,终于能跟上生命的节奏。
点击充电,成为大圆镜下一个视频选题!