对抗知识焦虑,从看懂这条开始
App 下载
胸腺里的分子开关:管发育也管白血病
去泛素化酶|胸腺发育|T细胞急性淋巴细胞白血病|MYC致癌因子|USP10|肿瘤学|免疫学基础|生命科学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
去泛素化酶|胸腺发育|T细胞急性淋巴细胞白血病|MYC致癌因子|USP10|肿瘤学|免疫学基础|生命科学|医学健康
当我们的身体遭遇病菌,最先冲上去的T细胞,全是在胸腺这个「免疫训练营」里练出来的——造血干细胞在这里一步步分化、筛选,最终变成能精准识别外敌的成熟T细胞。这个过程容不得半点差错:一旦调控失衡,本该发育成免疫卫士的细胞,就可能变成失控增殖的白血病细胞。
中南大学与美国国立卫生研究院的团队最近揪出了这个训练营里的「双面分子」:去泛素化酶USP10。它既是推动胸腺细胞正常增殖的「加速器」,也会在MYC致癌因子的驱动下,变成T细胞急性淋巴细胞白血病(T-ALL)的「帮凶」。为什么同一个分子能在健康与癌症间反复横跳?答案藏在它和另一个关键蛋白的绑定关系里。
要理解USP10的作用,得先认识细胞里的「垃圾处理系统」——泛素-蛋白酶体系统(UPS)。简单说,就是给要被降解的蛋白贴个「泛素标签」,蛋白酶体看到标签就会把蛋白拆成碎片,维持细胞内的蛋白平衡。
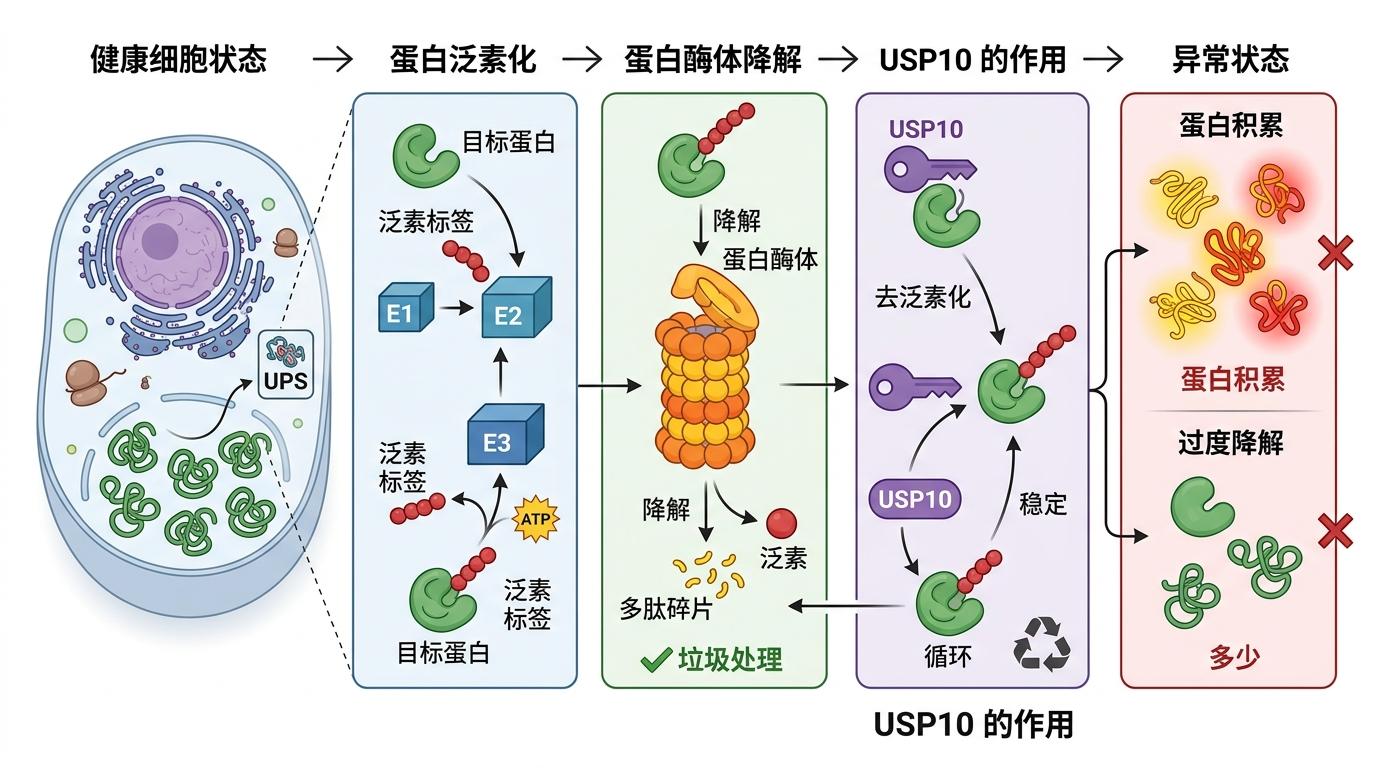
而USP10的角色,是「撕标签的人」。它是一种去泛素化酶,能把贴在蛋白上的泛素标签拆下来,让蛋白逃过降解,延长「保质期」。
团队通过小鼠文库筛选和单细胞测序发现,USP10在胸腺细胞的增殖高峰期表达量最高。如果把T细胞里的USP10特异性敲除,小鼠胸腺细胞的增殖和分化会直接「卡壳」——本该从双阴性阶段(既不表达CD4也不表达CD8)推进到双阳性阶段的细胞,大多停在了半路。
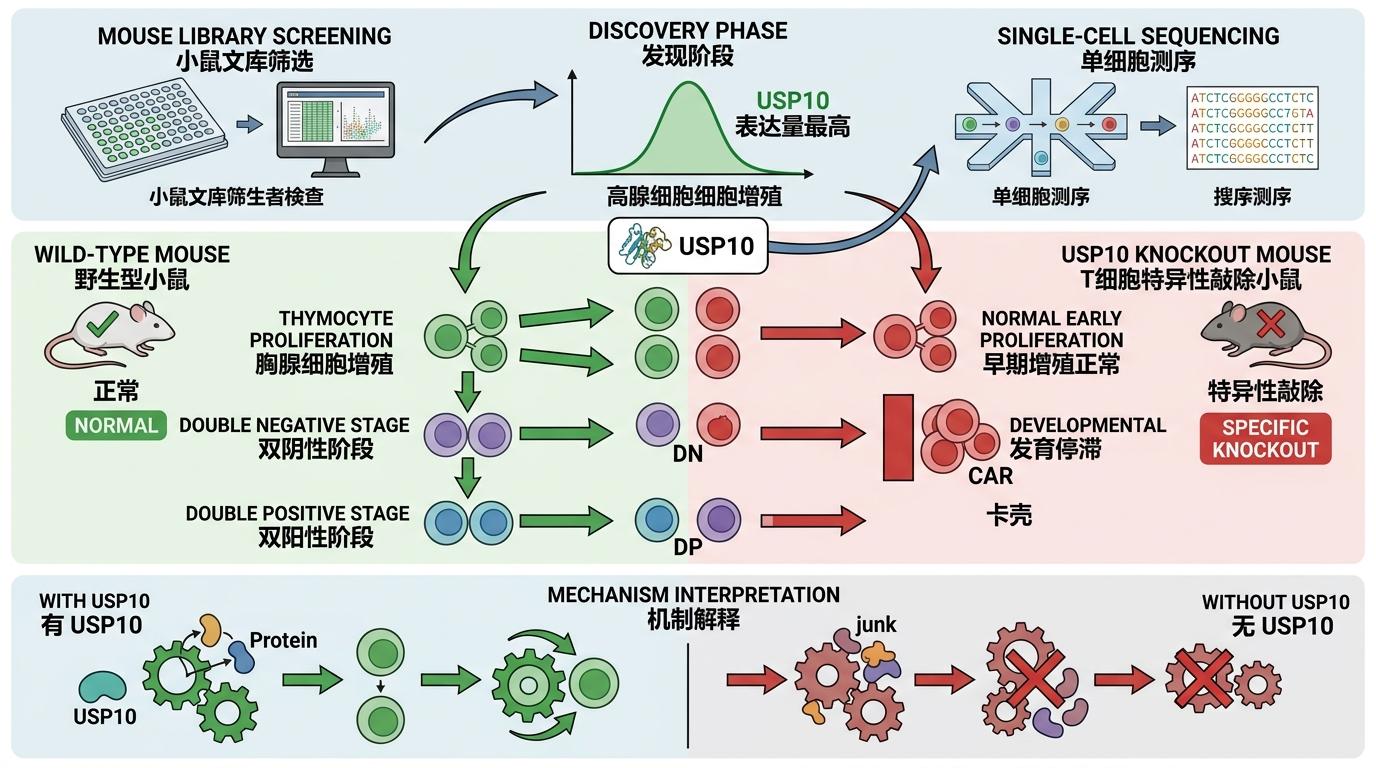
更关键的是,T-ALL患者外周血里的USP10水平,比健康人高得多;而在小鼠白血病模型里,用药物抑制USP10,就能明显延缓白血病的进展。
USP10的「双面性」,全因它绑定了另一个关键蛋白——SOX4。
SOX4是调控胸腺T细胞发育的核心转录因子,就像细胞里的「增殖指令官」,能启动一系列促进细胞分裂的基因。但这个「指令官」本身很不稳定,随时会被UPS系统贴上标签降解。
而USP10会直接和SOX4结合,把SOX4身上的泛素标签拆下来,让它能稳定存在,持续发号施令。团队做了个验证实验:把USP10敲除的小鼠,再给它们过表达SOX4,原本卡壳的胸腺细胞分化,居然恢复了正常。
但这套调控一旦被致癌因子盯上,就会彻底失控。MYC是T-ALL里常见的致癌因子,它能直接诱导USP10的表达——USP10越多,SOX4就越稳定,细胞增殖就越疯狂,最终突破正常调控,变成白血病细胞。
这就形成了一个可怕的正反馈环路:MYC诱导USP10,USP10稳定SOX4,SOX4又反过来促进细胞增殖,让MYC的致癌效应被无限放大。
USP10的特殊位置,让它成了T-ALL治疗的潜在靶点——它不像SOX4那样是「不可成药」的转录因子,而是可以用小分子抑制剂直接瞄准的酶。
目前已经有一些USP10抑制剂进入了前临床研究,比如Spautin-1、HBX19818等。在MYC驱动的小鼠白血病模型里,这些抑制剂能有效阻断USP10的功能,让SOX4被正常降解,从而延缓白血病的进展。
不过,USP10的「双面性」也给治疗带来了挑战:它在正常胸腺细胞发育里也扮演着重要角色,完全抑制它可能会影响正常T细胞的生成,削弱免疫系统。未来的研究重点,是开发能特异性针对肿瘤细胞里USP10的抑制剂,或者和其他治疗手段联合使用——比如和CAR-T疗法、免疫检查点抑制剂搭配,既打击白血病细胞,又尽量减少对正常免疫的损伤。
有意思的是,USP10还能通过稳定PD-L1等免疫检查点蛋白,帮助肿瘤细胞逃避免疫监视。这意味着,USP10抑制剂甚至可能和免疫治疗产生协同效应:一边让SOX4降解抑制肿瘤增殖,一边降低PD-L1水平,让免疫细胞能更好地识别和攻击肿瘤。
胸腺里的这场分子博弈,本质上是细胞正常发育与恶性转化的拔河。USP10就像拔河绳上的那个绳结,往左拉是维持免疫平衡的「功臣」,往右拉就是推动癌症的「帮凶」。
「发育与致癌,共享同一套分子密码。」这个发现不仅让我们对T-ALL的发病机制有了更深入的理解,也给未来的治疗提供了新的方向——与其直接瞄准那些「不可成药」的转录因子,不如去调控它们的「保鲜剂」,从源头切断致癌信号。
毕竟,细胞里的每一个分子,都在健康与疾病的边界上,做着细微的选择。