对抗知识焦虑,从看懂这条开始
App 下载
呼吸病新靶点:钾离子通道牵起炎症链条
气道黏液|炎症小体|哮喘患者|Kir2.1蛋白|KCNJ2通道|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
气道黏液|炎症小体|哮喘患者|Kir2.1蛋白|KCNJ2通道|感染性疾病|医学健康
当一位哮喘患者因胸闷喘息就诊时,医生的目光通常会聚焦在嗜酸性粒细胞、IgE这些熟悉的指标上——它们是2型炎症的标志性信号,驱动着气道黏液泛滥和管壁增厚。但很少有人会想到,这一切的源头,可能和细胞膜上一个不起眼的钾离子通道有关。广州国家实验室与广州医科大学的团队最近发现,这个名为KCNJ2的通道,正是串联起炎症小体、警报素与2型炎症的关键节点。为什么一个管离子流动的蛋白,会成为慢性气道病的核心推手?
KCNJ2编码的Kir2.1通道,原本的工作是像“离子水泵”一样维持细胞静息电位——就像给电池保持稳定电压,让心肌、神经等细胞能正常工作。但基因组关联研究(GWAS)很早就发现,它的基因变异和肺功能下降、慢性气道病进展有关,只是没人能说清其中的逻辑。
研究团队从临床样本入手,先在哮喘患者的气道上皮细胞里找到了第一个线索:KCNJ2的表达量显著降低,而且和黏液蛋白MUC5AC的水平刚好成反比——KCNJ2越少,黏液分泌越疯狂。为了确认因果,他们用基因编辑技术敲除了小鼠肺上皮细胞的Kcnj2基因,结果令人惊讶:在过敏原诱导的哮喘模型中,这些小鼠的气道高反应性大幅减轻,嗜酸性粒细胞浸润减少了近一半,Th2细胞因子IL-4、IL-5的水平直接腰斩。
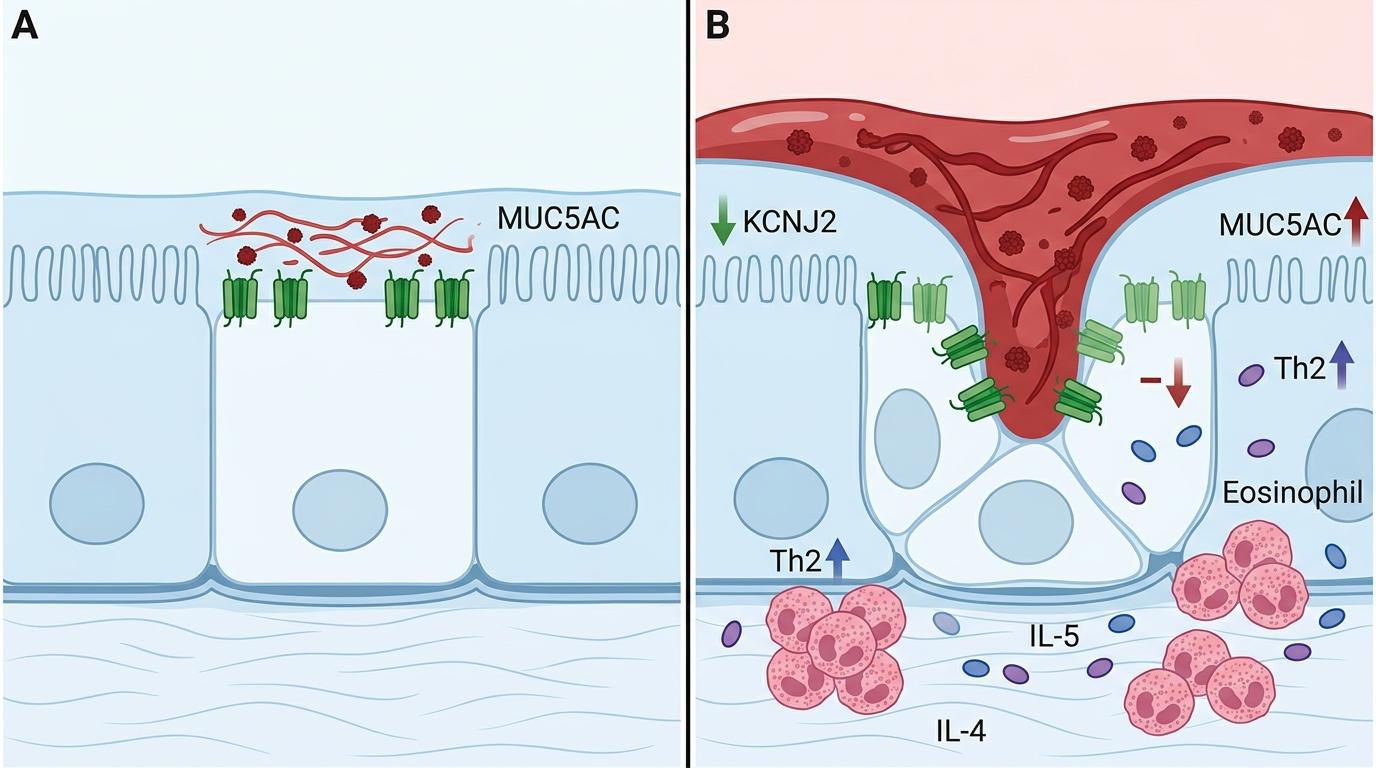
这不是简单的“缺了某个蛋白就变好”,而是一条隐藏的信号通路被揭开:KCNJ2通过调控细胞内外钾、钙离子的流动,影响着NLRP3炎症小体的活化——这个炎症小体就像细胞里的“炎症开关”,一旦被激活,就会诱导上皮细胞释放IL-33、TSLP这些“警报素”,进而招来大量免疫细胞,引爆2型炎症风暴。
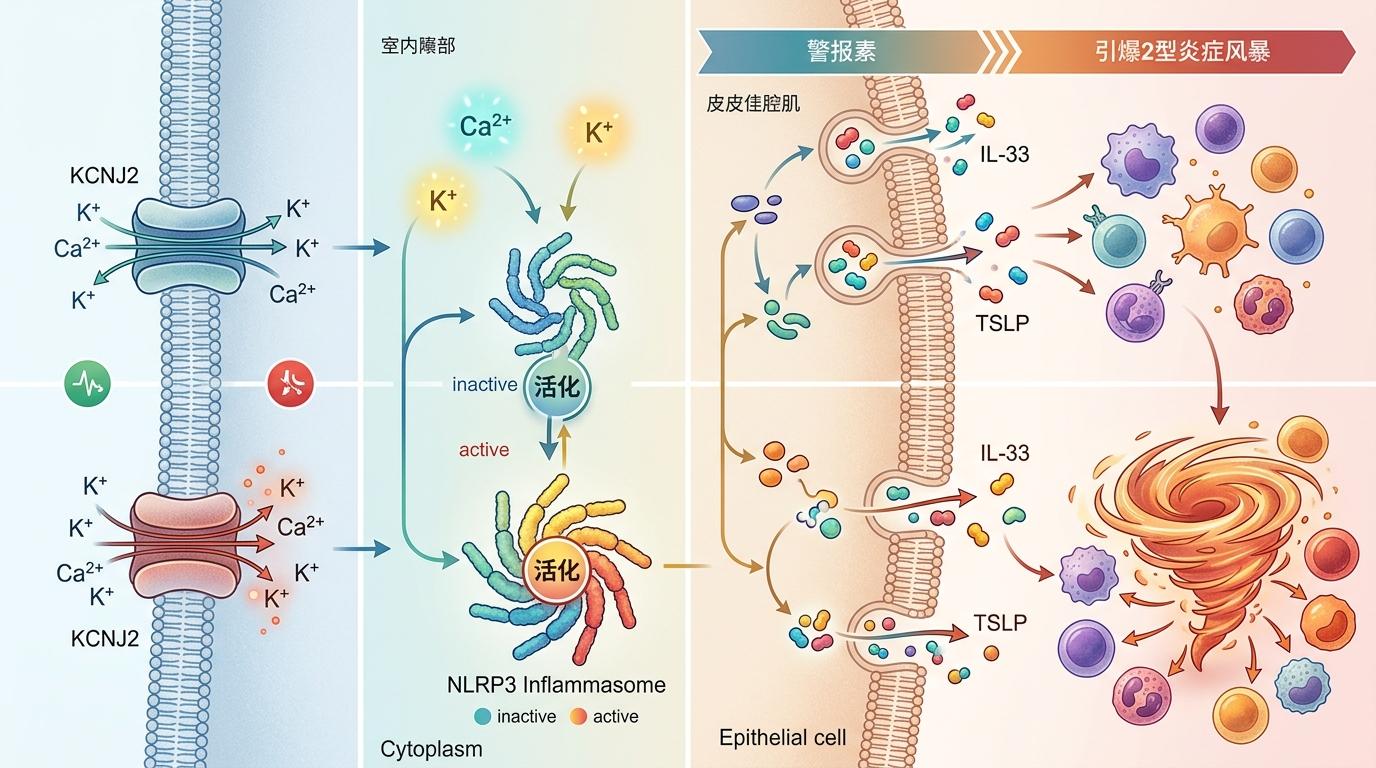
当KCNJ2-NLRP3这条信号轴被清晰描绘出来后,一个新的治疗方向也随之浮现:既然KCNJ2能促进炎症小体激活,那抑制它的功能,是不是就能从源头掐断2型炎症?
团队用一种叫ML133的KCNJ2抑制剂做了验证,结果和基因敲除的效果高度一致:无论是细胞实验还是动物模型,ML133都能有效减少黏液分泌、抑制炎症细胞浸润,甚至在患者的类器官模型里也能发挥作用。这意味着,KCNJ2有望成为继抗IgE、抗IL-5之后,又一个针对2型炎症的精准靶点——而且它的作用位置更上游,可能覆盖更多对现有生物制剂反应不佳的患者。
但这里也藏着陷阱。NLRP3炎症小体不是只会搞破坏的“坏分子”,它在维持气道上皮屏障完整性上还扮演着保护者的角色:之前有研究发现,NLRP3缺失的小鼠,气道紧密连接蛋白的表达会下降,反而让过敏原更容易侵入。这意味着,抑制KCNJ2的长期安全性需要更谨慎的评估——我们不能为了灭火,连房子的承重墙也拆了。
更现实的挑战是药物的特异性。KCNJ2不仅在肺部表达,在心肌细胞里也承担着关键功能,一旦抑制剂的选择性不足,很可能会引发心律失常等严重副作用。这也是为什么目前针对离子通道的药物研发,一直走得小心翼翼。
慢性气道病的治疗困境,本质上是“异质性”的困境:同样是哮喘或慢阻肺,有的患者是2型炎症驱动,有的是中性粒细胞炎症主导,还有的是混合表型。之前的治疗就像用广谱抗生素对付所有感染,有效但精准度不够。
KCNJ2的发现,恰恰给这种“异质性”提供了新的解释维度。研究显示,KCNJ2的基因变异在不同患者群体中的频率不同,这可能就是为什么有的患者2型炎症更严重,有的则相对温和。未来,通过检测患者KCNJ2的表达水平或基因变异类型,或许能更精准地划分患者亚型,进而选择最适合的治疗方案——比如对KCNJ2高表达的患者,优先考虑靶向KCNJ2的药物;对KCNJ2低表达但NLRP3活化明显的患者,直接用炎症小体抑制剂。
这正是精准医学的核心:不再把疾病当成一个整体,而是拆解成一个个由特定分子机制驱动的“内型”。而KCNJ2这条信号轴,就是连接基因、分子机制与临床表型的关键桥梁。
当我们谈论慢性气道病时,我们常常聚焦于那些看得见的症状——喘息、咳嗽、黏液,但真正决定疾病走向的,是细胞膜上那些看不见的离子流动,是细胞里那些微小的蛋白开关。KCNJ2的发现,不仅给患者带来了新的治疗希望,更让我们对疾病的认知从“症状”深入到“机制”。
精准医学的本质,就是在复杂的生命网络里,找到那个能撬动全局的关键节点。而KCNJ2,就是这样一个节点——它让我们看到,原来调节细胞的“电流”,就能平息气道的“炎症风暴”。