
3 个月前

3 个月前
故事始于约40年前,一则医学奇迹点燃了公众的希望:一名白血病患者通过砷剂与全反式视黄酸(维生素A的衍生物)的联合疗法被成功治愈。自此,“富含维生素A的食物(如胡萝卜)能抗癌”的观念深入人心。然而,科学的道路并非坦途。在随后的几十年里,几乎所有针对其他癌症的维生素A或类视黄醇临床试验都以失败告终,肿瘤非但没有被抑制,反而持续进展。这一巨大的反差,让维生素A在抗癌领域蒙上了一层神秘面纱:它究竟是盟友,还是伪装的敌人?这个困扰了科学界近半个世纪的悖论,直到最近才被揭开。
近日,普林斯顿大学康毅滨教授团队在国际顶尖期刊《自然·免疫学》(Nature Immunology)上发表了一项突破性研究,为上述悖论提供了清晰的答案。研究揭示,维生素A的代谢产物——视黄酸(Retinoic Acid, RA),在肿瘤免疫中扮演了一个意想不到的角色:它并非直接攻击癌细胞的“战士”,反而是给免疫系统踩下的一脚“隐形刹车”。
更重要的是,团队基于这一发现,成功研发出一款名为KyA33的新型小分子抑制剂。它能精准地“松开”这脚刹车,重新激活免疫系统对癌细胞的杀伤力,有望彻底改变癌症免疫治疗的现有格局。
这项重大突破的起点,源于博士生方草在实验中的一次意外观察。当时,她正在体外诱导骨髓细胞分化为树突状细胞(Dendritic Cells, DC)——这是免疫系统的“前线哨兵”和“总指挥官”。她发现,这些“哨兵”的活性并非随着培养时间的增加而线性增强,其活性在第三天达到顶峰后便开始神秘下滑。

“当时我还发现用储存时间偏长的完全培养基比用新的培养基能养出更高比例的高活性细胞。”方草回忆道。这个反常的现象让她产生了一个大胆的猜想:培养基中可能存在某种不稳定的“刹车”信号,它会随着时间流逝而失效。对光和氧气敏感的维生素A衍生物,完美符合这一条件。
这个偶然的线索,如同一束光,照亮了通往真相的道路。
顺着这条线索,研究团队迅速锁定了“元凶”。他们发现,在树突状细胞的分化过程中,一种名为ALDH1A2的酶会被激活。这种酶正是将维生素A转化为视黄酸(RA)的“加工厂”。
随着培养的进行,树突状细胞自己生产的RA越来越多,形成了一个负反馈循环:
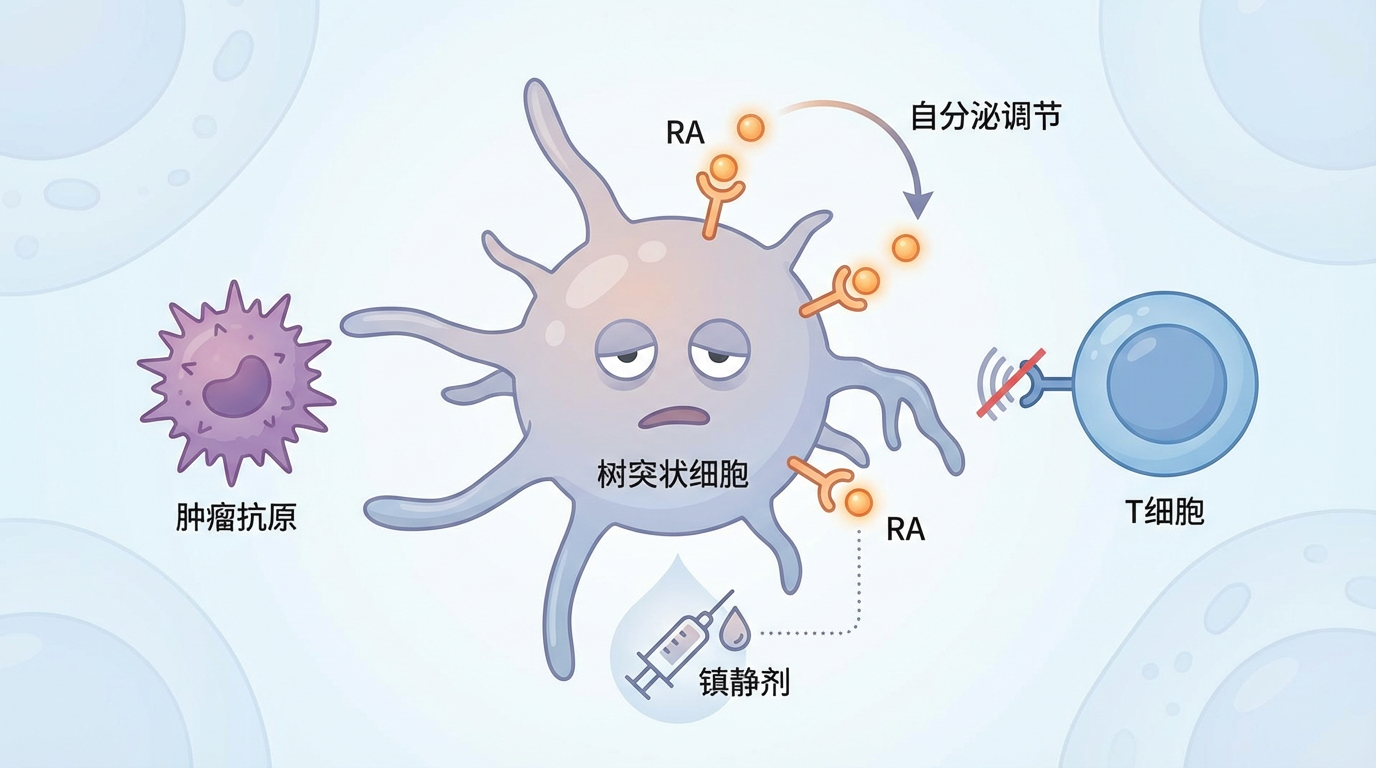
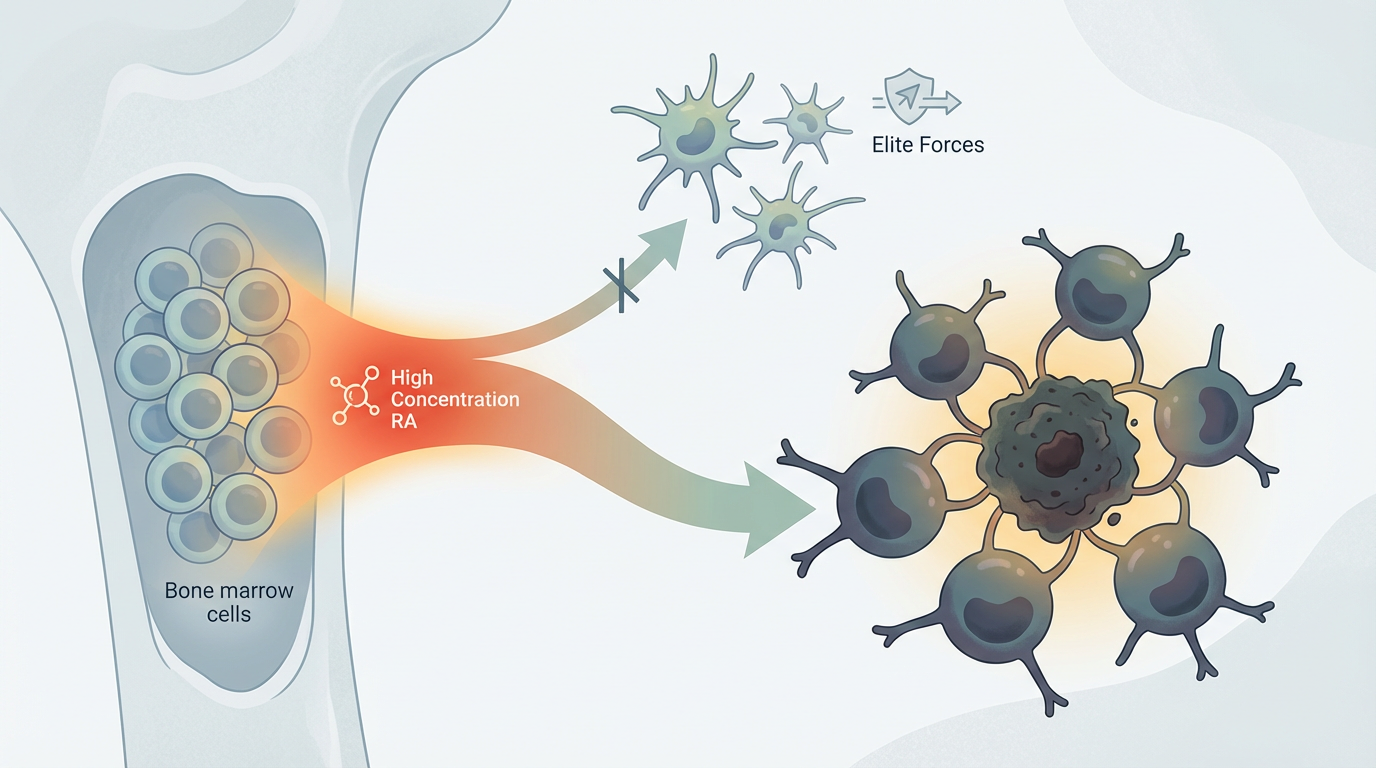
至此,维生素A的“双面间谍”身份被彻底揭穿。它在肿瘤微环境中产生的RA,成为了癌细胞逃避免疫监视的帮凶。
明确了敌人,下一步就是打造武器。树突状细胞疫苗(DC Vaccine)是癌症免疫治疗的重要方向,但临床响应率长期低于20%,其瓶颈正是ALDH1A2介导的这套“刹车系统”。
康毅滨团队利用其前期建立的药物研发平台,经过精密的分子演化和结构生物学设计,成功开发出小分子抑制剂KyA33。这把“利剑”锋利而精准:
在黑色素瘤小鼠模型中,经过KyA33处理的DC疫苗展现出惊人的抗肿瘤效果,肿瘤生长延迟时间延长了5.2天,肿瘤质量减少了4.8倍。更令人振奋的是,即便作为单一药物口服使用,KyA33也能显著抑制肿瘤生长。
这项研究的意义远不止于一篇顶级论文。它不仅完美解释了视黄酸在癌症治疗中“亦正亦邪”的历史悖论,更提供了一个极具临床转化潜力的解决方案。
目前,康毅滨教授团队已联合创立了生物科技公司Kayothera,全力推进ALDH1A抑制剂的临床转化。据透露,KyA33的GLP毒理学研究正在进行中,预计最早将于2026年进入I期临床试验。
从实验室培养皿中的一个意外发现,到一个可能改写癌症治疗规则的创新药物,这项研究生动地诠释了基础科学的强大力量。未来,通过精准地“松开”免疫刹车,KyA33及其同类药物有望与PD-1抑制剂等现有疗法协同作战,为更多癌症患者带来生命的曙光,真正突破免疫治疗的瓶颈。
点击充电,成为大圆镜下一个视频选题!