对抗知识焦虑,从看懂这条开始
App 下载
95%的人带EBV,为何仅少数得多发性硬化
病毒感染|免疫系统|B细胞|多发性硬化|Epstein-Barr病毒|自身免疫疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
病毒感染|免疫系统|B细胞|多发性硬化|Epstein-Barr病毒|自身免疫疾病|医学健康
你大概率已经携带了一种病毒——Epstein-Barr病毒(EBV),全球95%的成年人都逃不过它的感染,多数人只是在年少时发过一场不起眼的低烧,或者连症状都没有。但就是这种“无害”的常见病毒,却和一种致残性疾病深度绑定:多发性硬化(MS)。这种会让免疫系统攻击自身神经髓鞘的病,全球影响着近2000万人,而最新研究坐实了:几乎所有MS患者都曾感染EBV,感染后发病风险飙升32倍。为什么同样带病毒,有些人能安然无恙,有些人却要被免疫系统“背叛”?
EBV最擅长的,是悄悄潜入我们免疫系统里的B细胞——这种细胞本是生产抗体对抗感染的“免疫士兵”,却被病毒改造成了“卧底据点”。它会潜伏在记忆B细胞里,像藏在兵营里的间谍,一边偷偷复制自己,一边操控B细胞的基因表达。
你可以把EBV的核心蛋白EBNA2想象成一个“基因黑客”,它能直接绑定B细胞基因组里的关键调控区,启动一系列促炎和免疫激活的基因。原本负责生产保护性抗体的B细胞,开始大量表达MS风险基因,还会分泌信号分子,把免疫系统里的T细胞“策反”成攻击自身神经的“叛军”。
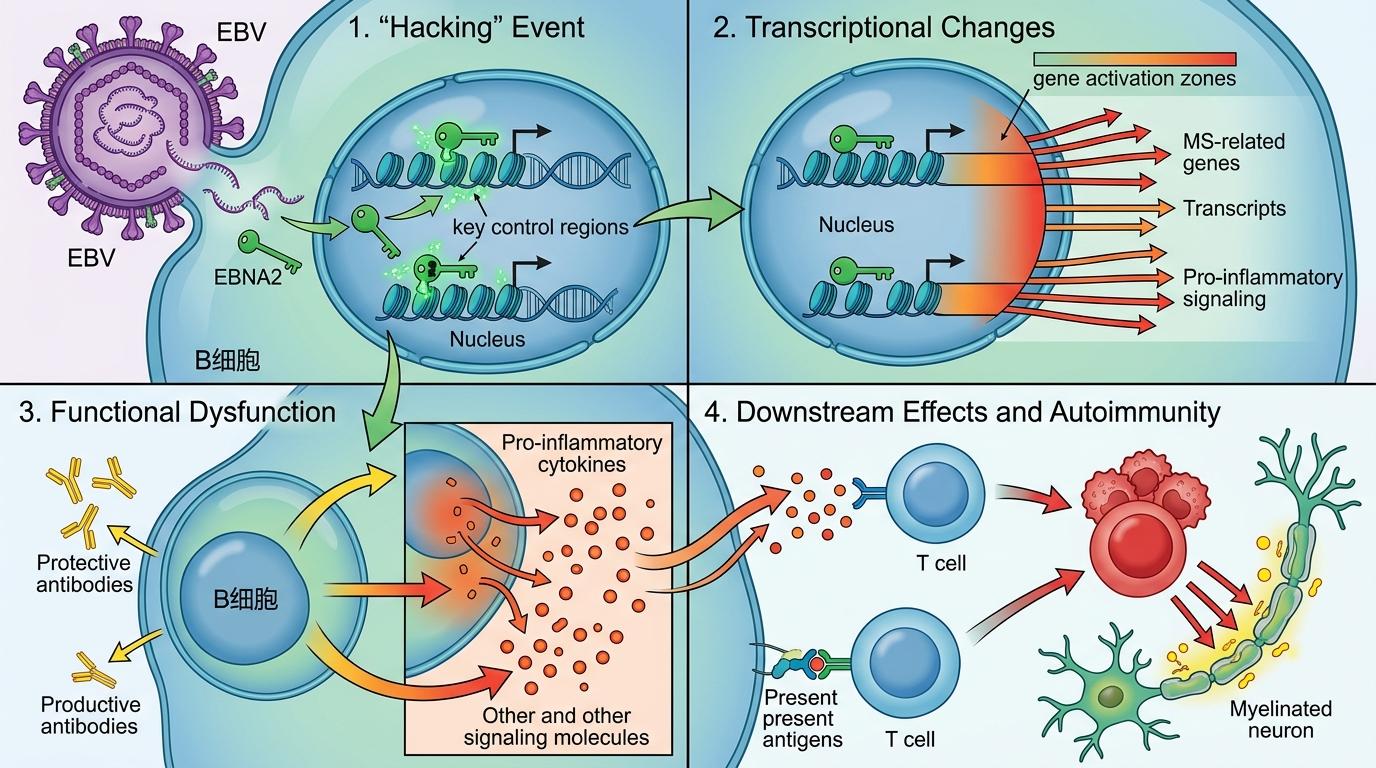
更精准地说,EBV感染的B细胞会异常激活JAK-STAT信号通路,让线粒体代谢过度亢奋,源源不断分泌促炎细胞因子GM-CSF,就像给T细胞浇上了汽油。这些被激活的T细胞会突破血脑屏障,疯狂攻击包裹神经的髓鞘,导致视力模糊、平衡失调、肢体震颤等MS症状。
95%的人都感染EBV,但只有极少数人得MS,这背后是基因和病毒的双重操控。大规模基因组研究发现,约10%的人携带特定遗传变异,这些变异一方面会让他们体内的EBV载量更高,另一方面会放大病毒对免疫系统的破坏。
比如HLA-DRB115:01这个MS高危基因,会让B细胞更高效地呈递EBV抗原,同时降低免疫系统对EBV的清除能力;而PVR基因的变异,则会让EBV更容易逃避免疫监视,在B细胞里大量繁殖。有趣的是,有些遗传变异反而会降低MS风险——比如HLA-A02:01能增强CD8+T细胞对EBV的杀伤,像给免疫系统装了个“病毒监控器”。
更关键的是分子模拟机制:EBV的EBNA1蛋白和神经胶质细胞上的GlialCAM蛋白结构高度相似,就像病毒戴了个“自身蛋白面具”。免疫系统在攻击EBV时,会误把GlialCAM当成敌人,连带着破坏神经髓鞘。约25%的MS患者体内,都能检测到这种“认错人”的交叉反应抗体。
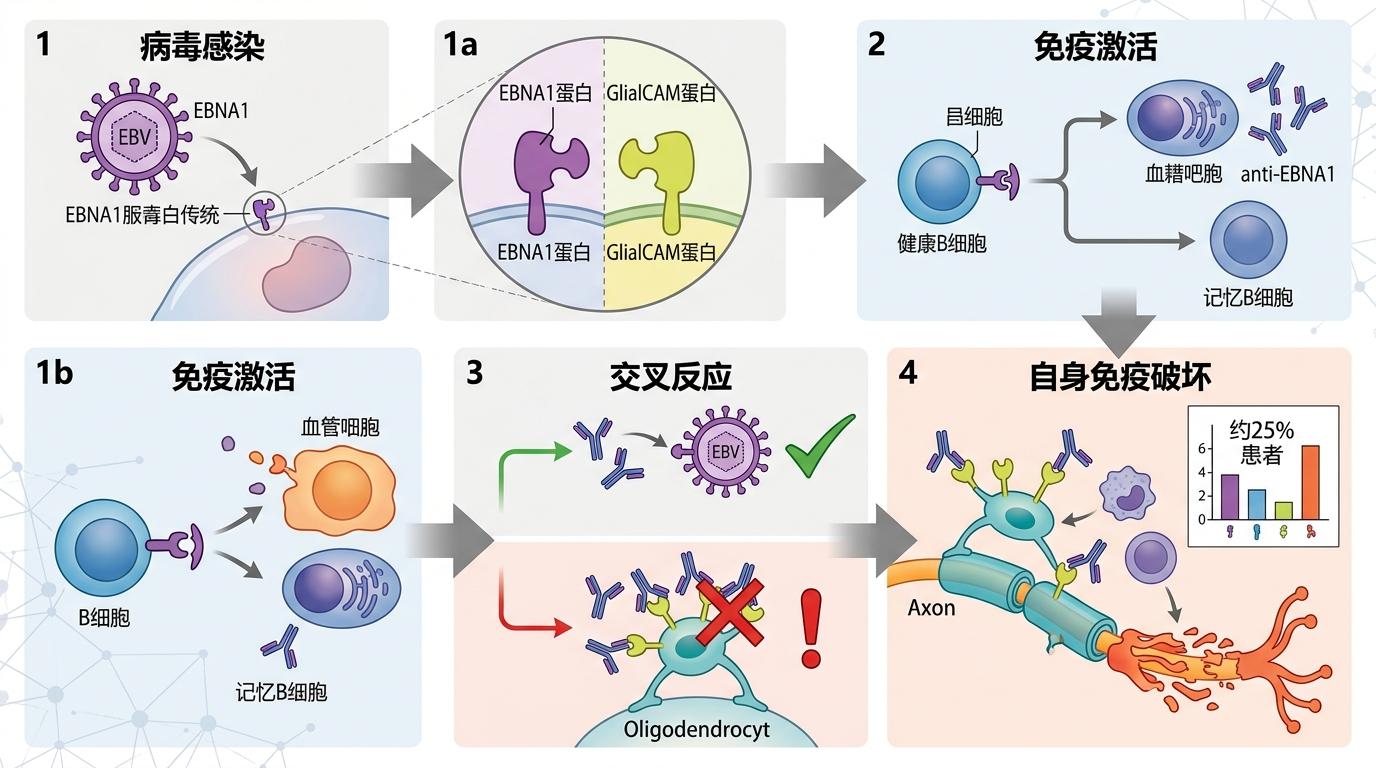
既然EBV是MS的核心触发点,那么针对病毒的治疗就成了突破口。目前已经广泛应用的抗CD20单抗,比如奥克珠单抗,就是通过清除体内的CD20+B细胞,间接消灭潜伏EBV的“卧底基地”,能让MS复发率降低50%以上,还能减缓原发进展型MS的恶化。
更精准的EBV特异性T细胞疗法也在临床试验中:科学家从患者体内提取能识别EBV的T细胞,在体外扩增后回输,让这些“特种部队”精准清除被EBV感染的B细胞。已有小规模试验显示,这种疗法能有效阻止MS进展,且副作用远小于广谱免疫抑制剂。
最值得期待的是EBV疫苗。目前多款基于mRNA技术的EBV疫苗已经进入临床,目标是阻止EBV初次感染,或者诱导免疫系统精准识别潜伏病毒。如果成功,不仅能减少传染性单核细胞增多症的发生,更能从根源上降低MS的发病风险——就像脊髓灰质炎疫苗消灭小儿麻痹症一样。
EBV和MS的关联,让我们重新认识了“常见病毒”的潜在威胁:那些看似无害的感染,可能在多年后成为自身免疫病的导火索。更值得关注的是,EBV不仅和MS有关,还和系统性红斑狼疮、类风湿关节炎等多种自身免疫病共享致病机制——都是通过操控B细胞、分子模拟破坏免疫耐受。
病毒潜伏在体内,基因藏在DNA里,两者的交互就像一组精密又危险的开关。病毒是导火索,基因是火药桶,而环境因素则是点燃引线的那根火柴。未来的MS防治,或许就是要在病毒感染早期就拔掉引线,在基因表达层面拆除火药桶,让那些携带EBV的人,永远不会等到免疫系统“背叛”的那天。