对抗知识焦虑,从看懂这条开始
App 下载
霍奇金淋巴瘤的糖衣陷阱,被老药艾格司他破解
艾格司他|糖衣盾牌|CD30蛋白|CAR-T疗法|霍奇金淋巴瘤|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
艾格司他|糖衣盾牌|CD30蛋白|CAR-T疗法|霍奇金淋巴瘤|肿瘤学|医学健康
同样是瞄准癌细胞表面的标志性蛋白,针对CD19的CAR-T疗法能让80%以上的B细胞淋巴瘤患者实现长期缓解,可靶向CD30的CAR-T在经典霍奇金淋巴瘤面前却屡屡折戟——明明这种癌细胞表面的CD30蛋白含量极高,堪称完美靶点,可CAR-T的完全缓解率始终卡在30%左右。
解放军总医院的研究团队揪出了藏在靶点背后的“隐形凶手”:癌细胞给CD30蛋白披上了一层致密的糖衣盾牌,让CAR-T细胞“看不清、打不准”。更让人意外的是,破解这道盾牌的钥匙,竟是一款早已上市的戈谢病老药。
你可以把CD30蛋白想象成癌细胞身上插着的一面红色旗帜,CAR-T细胞就是盯着旗帜冲锋的战士。但在霍奇金淋巴瘤细胞上,这面旗帜的两个关键位置(Asn101和Asn276)被接上了复杂的N-连接糖链——就像给旗帜裹上了一层厚厚的透明塑料膜。
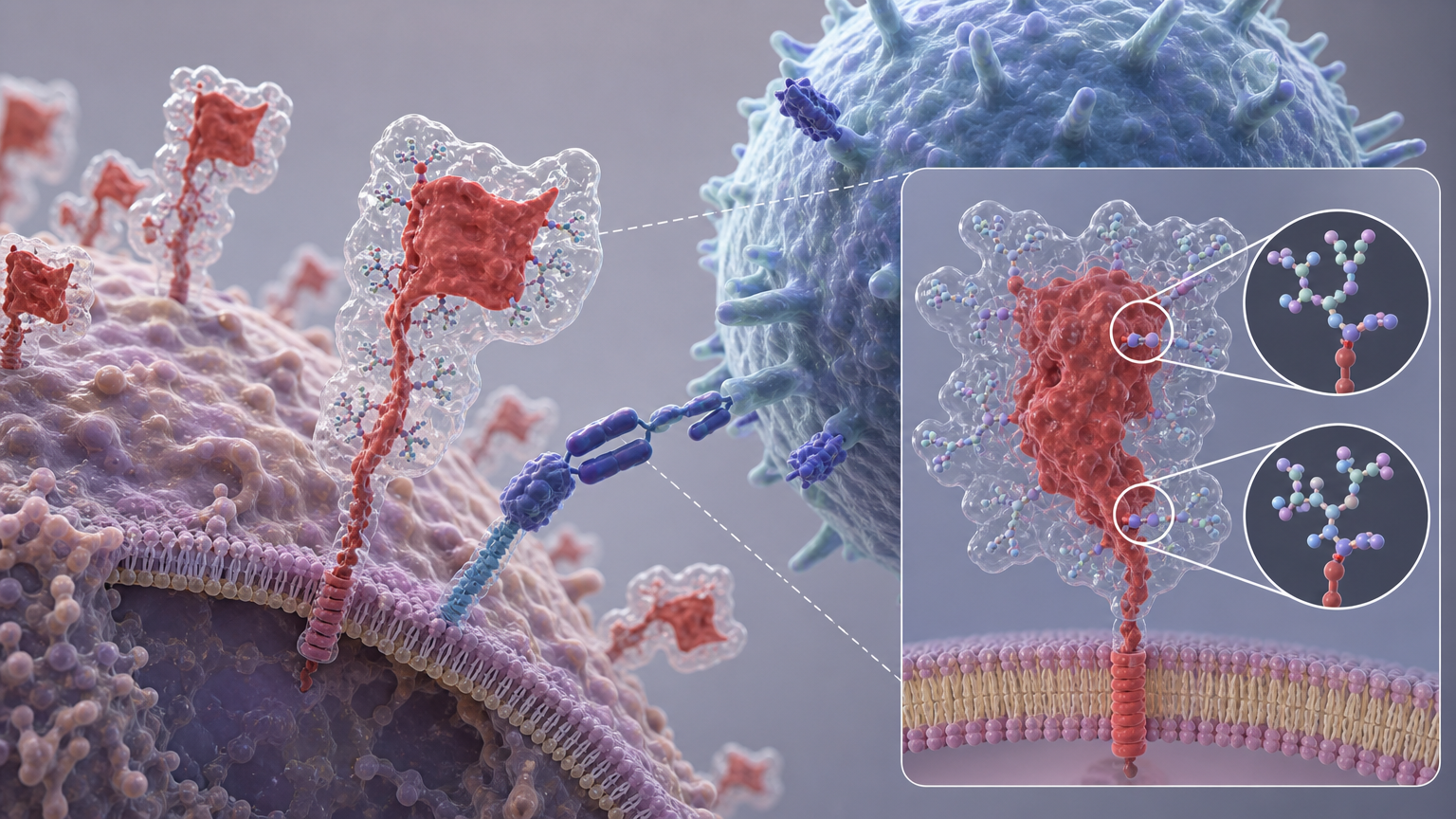
这层膜不影响旗帜的存在,却彻底挡住了战士的视线。研究团队通过CRISPR基因编辑敲除这两个糖基化位点后,CAR-T细胞对肿瘤细胞的识别率直接翻倍,激活程度和杀伤效率提升了3倍以上;而用化学方法去除糖链后,原本对CAR-T毫无反应的癌细胞,也能被快速清除。
真实的机制比这个类比更精确:这些糖链是高度分支的复杂结构,会在CD30蛋白表面形成立体空间位阻,直接阻碍CAR-T细胞表面的受体与CD30的结合位点对接,连免疫突触都无法正常形成——相当于战士的枪根本碰不到目标,自然无法发起攻击。
既然糖衣是核心障碍,能不能安全地把它剪掉?研究团队把目光投向了戈谢病治疗药物艾格司他。这款药原本的作用是抑制糖鞘脂的合成,没想到它能间接影响蛋白质糖基化的末端修饰——精准剪掉CD30糖链末端的唾液酸残基。
就像给塑料膜开了个透气的口子,原本被挡住的CD30结合位点重新暴露出来。实验数据显示,用艾格司他预处理后的霍奇金淋巴瘤细胞,CD30 CAR-T的杀伤效率提升了4倍;而对那些已经敲除糖基化位点的癌细胞,艾格司他则完全没有增强效果——这直接证实了它的作用就是“修剪糖衣”。
在淋巴瘤小鼠模型中,艾格司他联合CD30 CAR-T的治疗方案,让肿瘤体积缩小了80%以上,且没有出现额外的毒性反应。更重要的是,这种策略不止对CAR-T有效:它同样能增强CD30抗体药物偶联物的抗肿瘤活性,证明“去糖盾”是一种通用的增敏思路。
这层糖衣盾牌并非霍奇金淋巴瘤独有。研究发现,CD19蛋白的过度糖基化也会抑制CAR-T的疗效,PD-L1的糖基化则能增强它与PD-1的结合能力,进一步巩固免疫抑制的“城墙”。肿瘤细胞通过异常糖基化修饰,给自身穿上隐形斗篷的机制,在多种实体瘤和血液肿瘤中普遍存在。
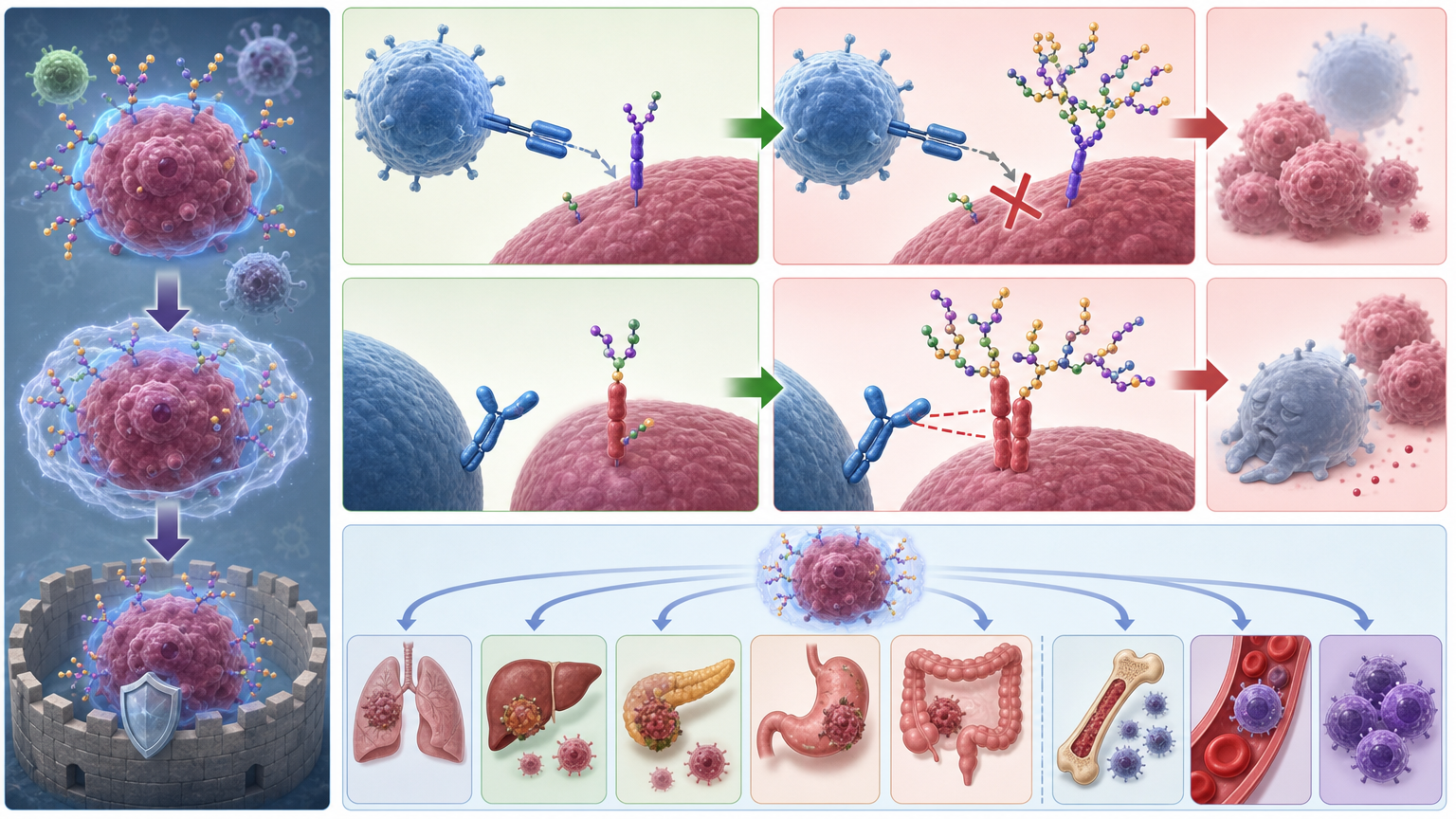
目前已有更精准的工具在研发中:比如DGlyTAC技术,能把脱糖酶和靶向纳米抗体结合,精准去除特定蛋白的糖链;CRISPR基因编辑则可以敲除免疫细胞中的糖基转移酶,降低T细胞的耗竭状态。这些技术和艾格司他这类老药一起,正在构建一套“糖免疫疗法”的全新体系——从“攻击癌细胞”转向“拆除癌细胞的防御工事”。
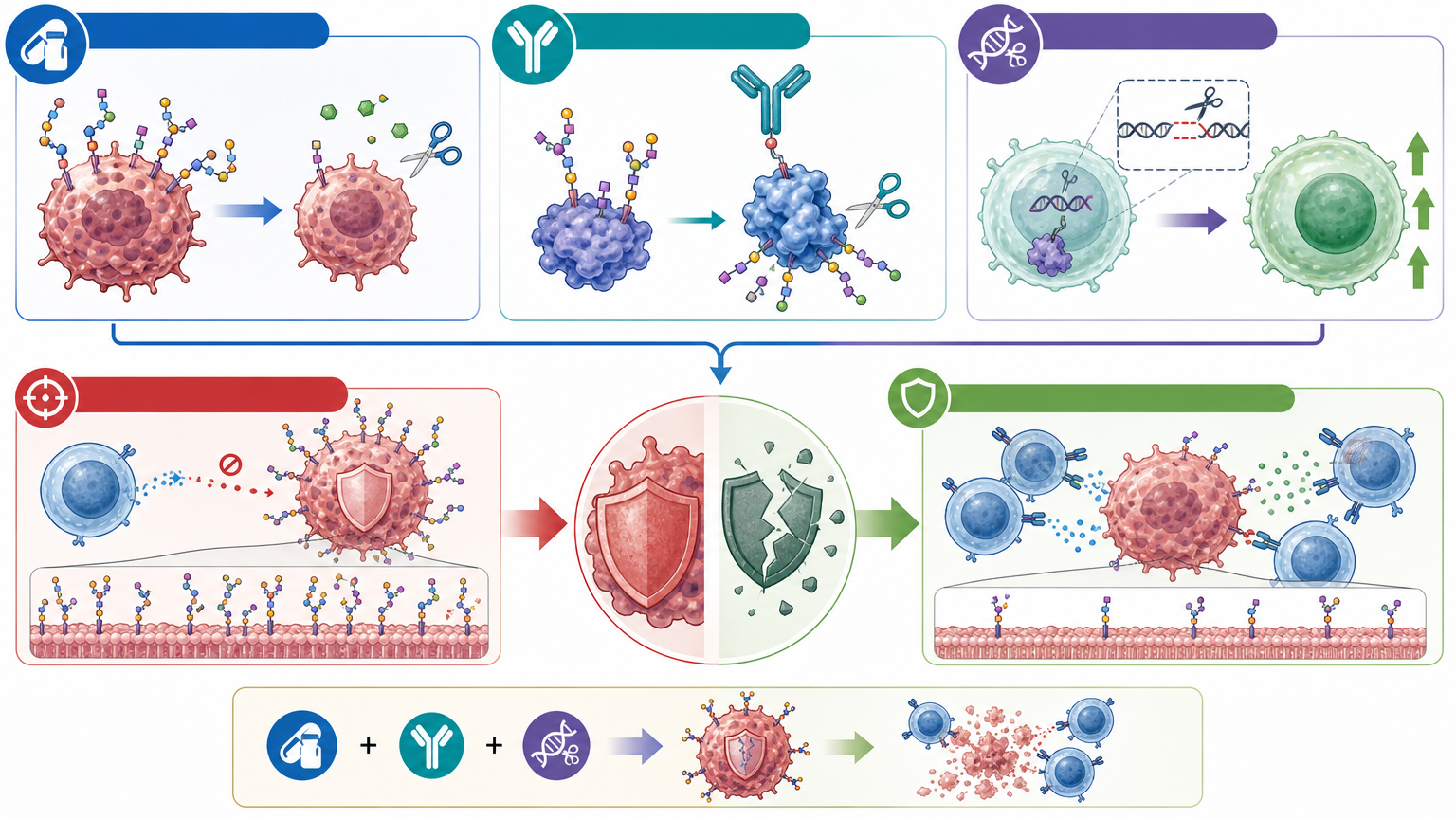
过去十年,CAR-T疗法的优化几乎都聚焦在“让战士更强”——改造CAR结构、提升T细胞活性、优化清淋方案,却很少有人关注“敌人的防御工事”。这次的研究像是给整个领域提了个醒:有时候,破解难题的关键不是制造更锋利的矛,而是找到拆掉盾牌的工具。
糖衣不再是肿瘤的护身符,而是免疫治疗的新靶点。当我们开始读懂癌细胞表面的糖码,那些曾经束手无策的耐药难题,或许会在老药和新技术的碰撞中,找到全新的答案。