对抗知识焦虑,从看懂这条开始
App 下载
氧气感知决定再生:哺乳动物的再生开关被锁住了
人类再生能力|蝾螈再生|氧气感知机制|HIF1A蛋白|再生医学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
人类再生能力|蝾螈再生|氧气感知机制|HIF1A蛋白|再生医学|医学健康
把一只蝾螈的腿切掉,几周后它会长出完整的新腿——骨骼、肌肉、神经一个不少,连疤痕都没有。但如果是人类,伤口只会结疤,再生的事想都别想。几十年来科学家都在纳闷:明明我们和蝾螈共享大半再生相关的基因,为什么偏偏人类的再生能力被彻底封印?直到2026年4月《科学》杂志的一项研究给出了答案:不是基因不行,是我们感知氧气的方式,从根源上关掉了再生程序。
你可以把HIF1A想象成细胞里的“氧气温度计”——它是一种专门感知氧气浓度的蛋白质。当周围氧气充足时,这个“温度计”会被迅速拆解,像没用的草稿纸一样被细胞降解;一旦氧气浓度降低,HIF1A就会稳定下来,钻进细胞核里按下再生的启动键。
这个过程的精准度堪比精密仪器:正常氧浓度下,HIF1A的两个关键脯氨酸残基会被PHD酶羟基化,就像给它贴了个“销毁标签”,随后VHL蛋白会识别这个标签,把HIF1A送进蛋白酶体彻底分解,整个过程半衰期不到5分钟。但当氧浓度降到水环境的水平(约12%),PHD酶的活性会急剧下降,HIF1A得以幸存,进而激活超过60个与再生相关的基因——包括促进血管生成的VEGF、调控糖酵解的代谢酶,以及让细胞恢复迁移能力的骨架蛋白。
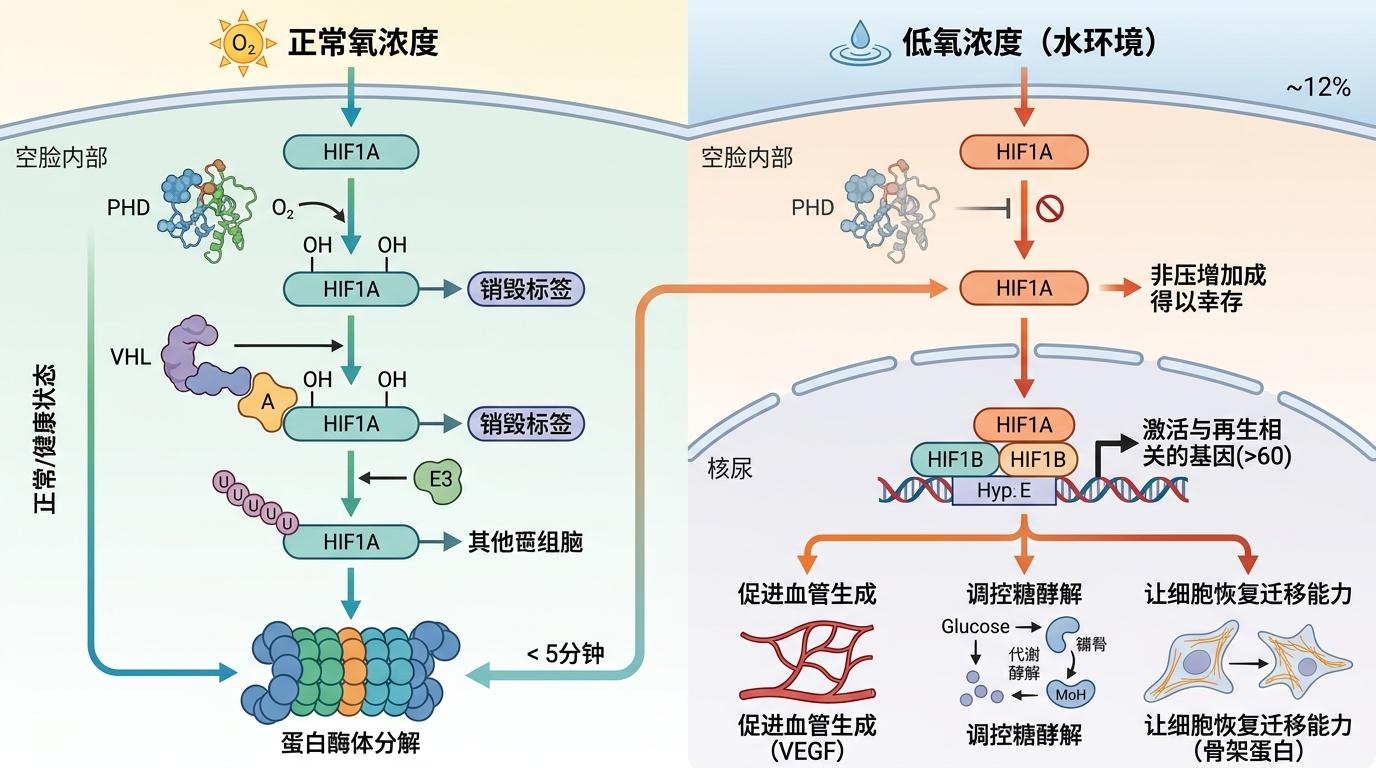
研究团队做了个直白的对比:把蛙类蝌蚪和小鼠胚胎的截肢肢体分别放在低氧和高氧环境中培养。结果显示,低氧环境下的小鼠胚胎肢体不仅伤口闭合速度快了3倍,皮肤细胞还会拉长形态、重组肌动蛋白骨架,像两栖动物的再生细胞一样开始迁移。更关键的是,即使在高氧环境中,只要用药物稳定住HIF1A,小鼠细胞也能启动再生程序。
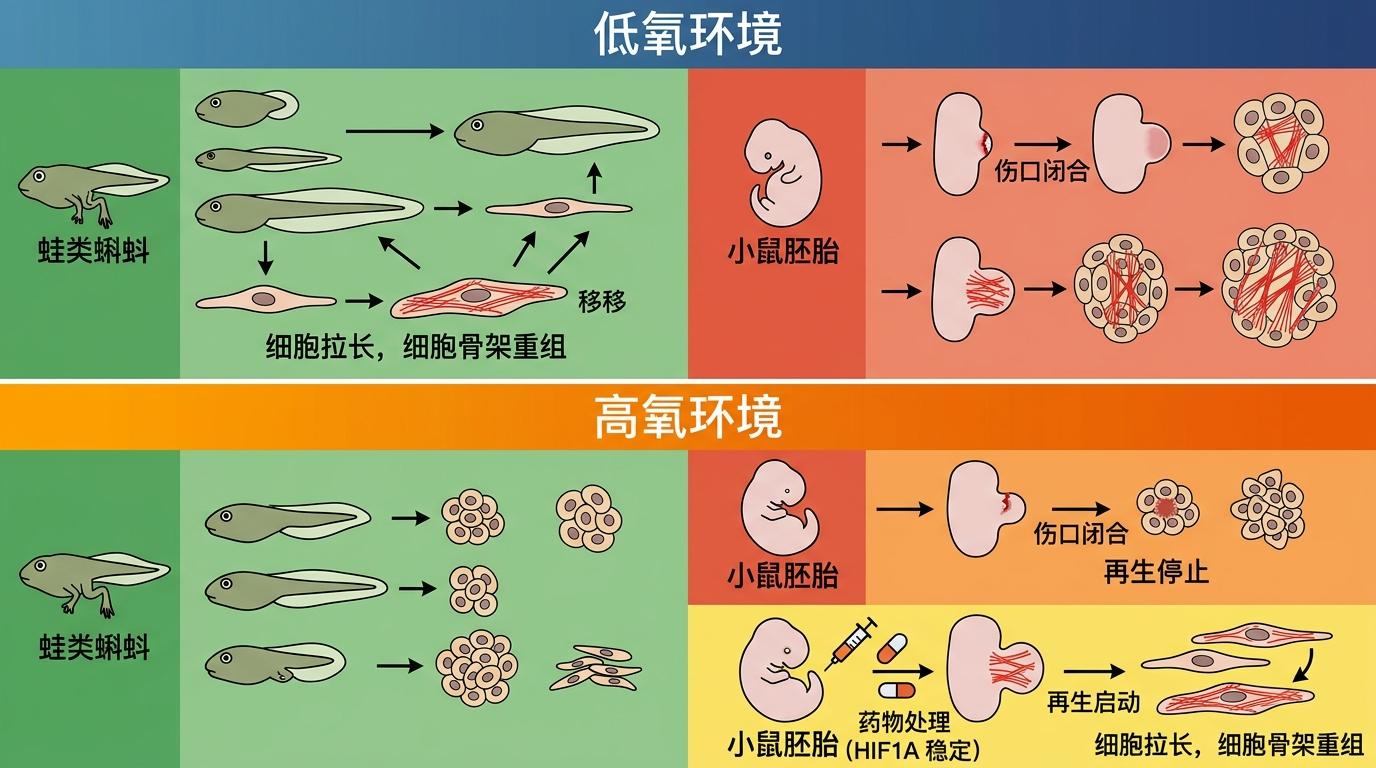
低氧环境激活的不只是HIF1A,它还会彻底改写细胞的“生存模式”——把依赖氧气的氧化磷酸化,切换到不需要氧气的糖酵解。
你可以把糖酵解理解成“应急发电站”:正常情况下细胞用氧气“烧”葡萄糖发电,效率高但依赖氧气;糖酵解则直接把葡萄糖分解成乳酸,虽然效率只有前者的1/18,但胜在速度快、不挑环境,还能顺便为细胞增殖提供核苷酸、脂质等原材料——这正是再生最需要的。研究人员观察到,低氧环境下的小鼠细胞,糖酵解相关酶的活性提升了4倍,乳酸浓度也随之升高,而乳酸本身就能促进细胞周期运转,像燃料一样推动再生。
更隐蔽的变化发生在表观遗传层面。低氧会抑制依赖氧气的JmjC组蛋白去甲基酶,让组蛋白上的甲基化标记积累,稳定染色质结构;同时,糖酵解产生的乙酰辅酶A会增加组蛋白乙酰化,让再生相关基因的染色质变得松散易激活。简单说,低氧就像给细胞的再生基因拆了封条,而高氧环境下,这些基因永远被紧紧封在 chromatin 里。
蛙类蝌蚪则展现出了“作弊”能力:它们的细胞天生就低表达那些降解HIF1A的基因,不管氧气浓度高低,HIF1A都能保持稳定。就算把它们放在远高于空气氧浓度的环境中,蝌蚪的再生程序也不会中断——因为它们的“氧气温度计”本来就调得很迟钝。
这项研究最让人兴奋的地方,不是解释了“为什么”,而是给出了“怎么办”的方向。
目前已经有针对HIF1A的药物进入临床试验,比如PHD抑制剂FG-4592,它能通过抑制PHD酶的活性,在高氧环境下也稳定HIF1A,已经被用于治疗慢性肾病导致的贫血。在伤口愈合领域,研究人员正在测试局部使用HIF1A稳定剂的效果——比如在糖尿病足溃疡患者的伤口上涂抹凝胶,模拟低氧环境,促进再生而非瘢痕形成。
另一个方向是“智能氧气递送系统”。传统的高压氧治疗已经被用于促进慢性伤口愈合,但它的问题是无法精准控制局部氧浓度。现在科学家正在开发能根据伤口微环境动态释放氧气的生物材料,比如对pH或ROS敏感的纳米气泡,当伤口处于炎症状态时自动释放氧气,炎症消退后则减少供氧,避免过度氧化导致瘢痕。
当然,现在还远没到“断肢再生”的地步。成年哺乳动物的再生还面临着免疫系统、细胞衰老等多重障碍,比如MRL小鼠虽然能再生部分组织,但也无法长出完整的肢体。但至少我们知道了,人类的再生能力不是消失了,只是被氧气感知机制暂时锁住了——而我们已经找到了开锁的钥匙。
从水生到陆生,脊椎动物为了适应更高氧的环境,付出了再生能力的代价——这是进化的选择,也是我们必须面对的现实。但这项研究让我们看到,进化的选择并非不可逆转。
我们总以为再生是某种“超能力”,但其实它一直藏在我们的细胞里,只是需要一个正确的开关。氧感知重塑再生,锁在基因里的能力可被唤醒。未来某一天,当我们不小心割伤手指,或许不再需要等待结疤,而是能看着伤口慢慢长出新的组织——就像亿万年前我们的祖先在水里做的那样。