对抗知识焦虑,从看懂这条开始
App 下载
不用抽T细胞改完再回输,CAR-T直接在体内造
自身免疫病|癌症治疗|中国初创公司|细胞基因治疗|体内CAR-T技术|新药研发|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
自身免疫病|癌症治疗|中国初创公司|细胞基因治疗|体内CAR-T技术|新药研发|医学健康
想象一下:不用从胳膊上抽走几百毫升血,不用在实验室里花两三周改造免疫细胞,不用等细胞扩增完再输回体内——一针打进去,你的身体自己就能造出精准杀怪的CAR-T细胞。2026年春天,一家中国初创公司完成5000万美元融资,把这个听起来像科幻的场景推到了临床阶段。更重要的是,这项技术不止能治癌症,还能给那些被自身免疫病缠了十几年的人,递去一根新的救命稻草。为什么这种「体内造CAR-T」的思路,能让全球药企砸上百亿美元疯抢?
你可以把传统CAR-T疗法理解成「定制武器」:先从患者体内把T细胞——也就是免疫系统里的「士兵」——抽出来,送到体外工厂里装上能识别癌细胞的「瞄准镜」(CAR嵌合抗原受体),再把训练好的士兵扩增几十万倍,最后输回患者体内杀敌。这套流程虽然有效,但太麻烦了:光是细胞改造扩增就要两三周,急着救命的晚期患者可能等不起;而且「一人一批」的定制模式,让一次治疗成本能飙到百万元级别。
体内CAR-T则是把「工厂搬进了体内」——用一个包裹着CAR基因的「快递盒」,直接把「瞄准镜」的设计图纸送到患者体内的T细胞手里。目前主流的「快递盒」是脂质纳米颗粒(LNP),一种能骗过免疫系统、精准钻进T细胞的微小脂质球。它裹着的mRNA就是设计图纸,T细胞拿到后,自己就能合成CAR蛋白,变身成能精准杀靶的CAR-T细胞。
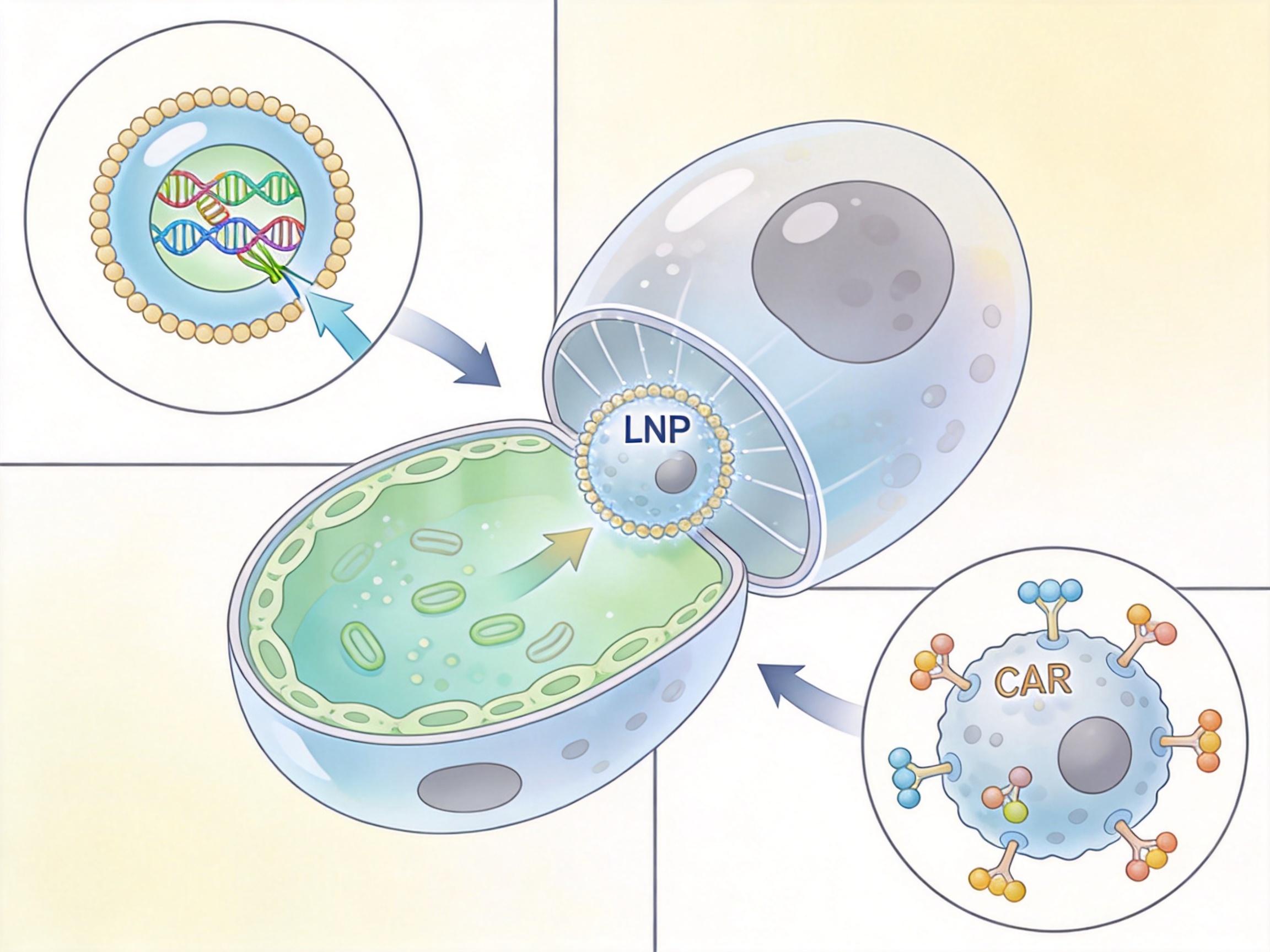
这个过程省掉了体外培养的所有步骤,从打针到起效可能只需要几天;而且「快递盒」可以像普通药物一样批量生产,成本能降到传统CAR-T的一半甚至更低。更关键的是,mRNA会在细胞里自然降解,CAR蛋白的表达是暂时的——这对自身免疫病患者来说是个福音:他们不需要永久抑制免疫系统,只要在病情活跃期「按需激活」CAR-T细胞,清除掉作乱的免疫细胞就行。
过去十年,CAR-T的光芒都集中在癌症治疗上,但体内CAR-T的最大潜力,可能在那些被忽略的自身免疫病领域。
比如系统性红斑狼疮患者,免疫系统会不分敌我地攻击自己的关节、肾脏和皮肤。传统的免疫抑制剂是「无差别攻击」,一边压下作乱的免疫细胞,一边也把正常的免疫防线打垮了,患者很容易感染、甚至患上癌症。而体内CAR-T能精准瞄准作乱的B细胞——这种细胞会产生攻击自身的抗体——就像狙击手一样,只打掉坏人,不连累无辜。
从已有的临床数据看,针对CD19靶点的体内CAR-T,能在几周内把患者体内的致病B细胞清除90%以上,而且因为mRNA的表达是暂时的,几个月后新的健康B细胞会重新生长,相当于给免疫系统做了一次「温和重置」。更重要的是,这种疗法支持重复给药:如果患者病情复发,再打一针就能重新激活CAR-T细胞,不用再经历传统CAR-T那种复杂的流程。
当然,这条路也不是一帆风顺。目前最大的难题是「快递盒」的精准度:怎么确保LNP只钻进T细胞,不跑到肝脏、肾脏这些正常器官里?科学家的解决办法是给LNP装上「导航」——在脂质球表面贴上能识别T细胞表面CD3蛋白的抗体片段,就像给快递写上了精准地址,能把mRNA送到指定的「车间」里。
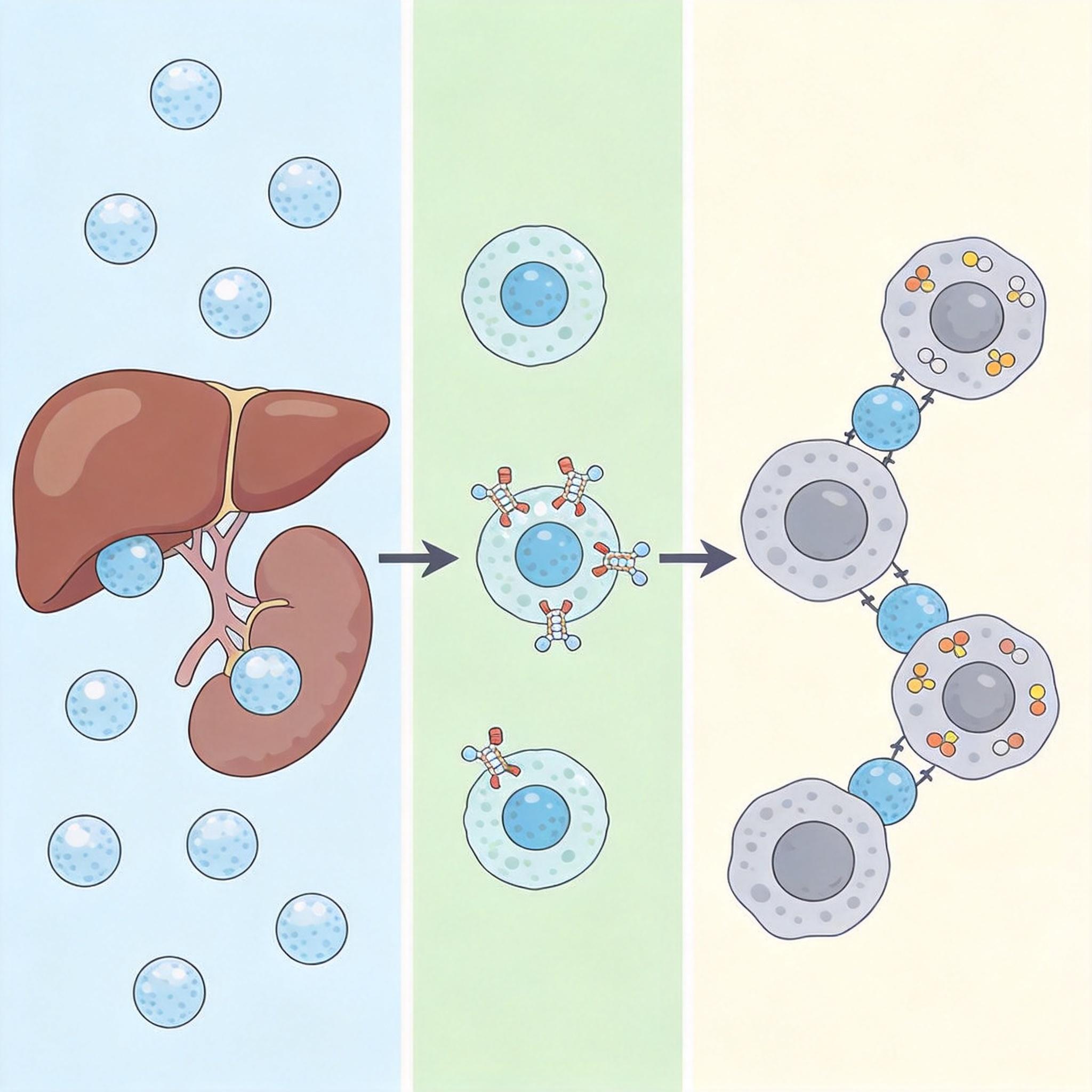
2025年以来,全球药企已经砸了超过140亿美元收购体内CAR-T公司,中国的研发管线也占到了全球的一半。但热闹的资本背后,这项技术还有三道坎要跨。
第一道是递送效率。目前LNP能改造的T细胞还只有不到10%,要达到治疗效果,可能需要更高的转染效率——这意味着要优化LNP的脂质配方,或者找到更精准的T细胞靶向分子。
第二道是长期安全性。虽然mRNA不会整合到基因组里,比病毒载体更安全,但反复注射LNP会不会引发免疫反应?体内生成的CAR-T细胞会不会攻击正常组织?这些问题都需要更多的长期临床数据来回答。
第三道是监管的跟上。传统CAR-T是「细胞产品」,而体内CAR-T更像「基因药物」,现有的监管框架还没有完全适配这种新疗法。比如怎么定义产品的质量标准?怎么监测体内CAR-T细胞的活性和持久性?这些都需要监管机构和药企一起摸索。
从抽血、改造、回输的「体外定制」,到一针激活的「体内制造」,CAR-T疗法的进化,本质上是让治疗更「贴近」患者——不用等、不用承受体外培养的风险,甚至能像吃感冒药一样按需给药。
未来的某天,可能红斑狼疮患者不用再天天吃免疫抑制剂,只要每半年打一针体内CAR-T,就能像正常人一样生活;晚期癌症患者不用再等两三周的细胞培养时间,当天就能用上救命的疗法。
好的治疗,应该是让患者忘记治疗本身。 体内CAR-T的意义,不止是技术的突破,更是让「精准医疗」从实验室里的概念,变成每个患者都能触碰到的希望。