
4 天前

4 天前
一位52岁的乳腺癌患者,在完成手术和化疗后,开始服用芳香化酶抑制剂——这是防止肿瘤复发的关键一步。但仅仅半年,她就开始频繁感到腰背酸痛,爬两层楼梯都要歇三次,体检报告显示腰椎骨密度下降了12%,肌肉量比治疗前少了8斤。这不是个例:每两位接受内分泌治疗的激素受体阳性乳腺癌患者中,就有一位会遭遇骨量流失、肌肉萎缩的困境,甚至有人因为难以忍受副作用提前停药,反而给肿瘤复发留了机会。有没有一种办法,既能守住治疗效果,又能留住骨骼和肌肉的健康?
你可以把低强度振动(LIV)想象成给骨骼和肌肉做“被动运动按摩”——它用30Hz左右的高频微震,模拟肌肉自然收缩时产生的机械刺激,既不会像高强度运动那样给虚弱的身体添负担,又能精准激活骨肌的修复机制。
在模拟乳腺癌患者雌激素剥夺状态的小鼠实验里,这种每天20分钟的振动展现出了清晰的效果:年轻小鼠单独接受振动后,腰椎骨小梁的体积和连接密度显著提升,破骨细胞数量减少了21%,成骨细胞活性提高了34%,前肢抓力比对照组强了17%;它们的肌肉纤维变粗,脂肪堆积速度慢了近40%,葡萄糖耐量也得到改善。
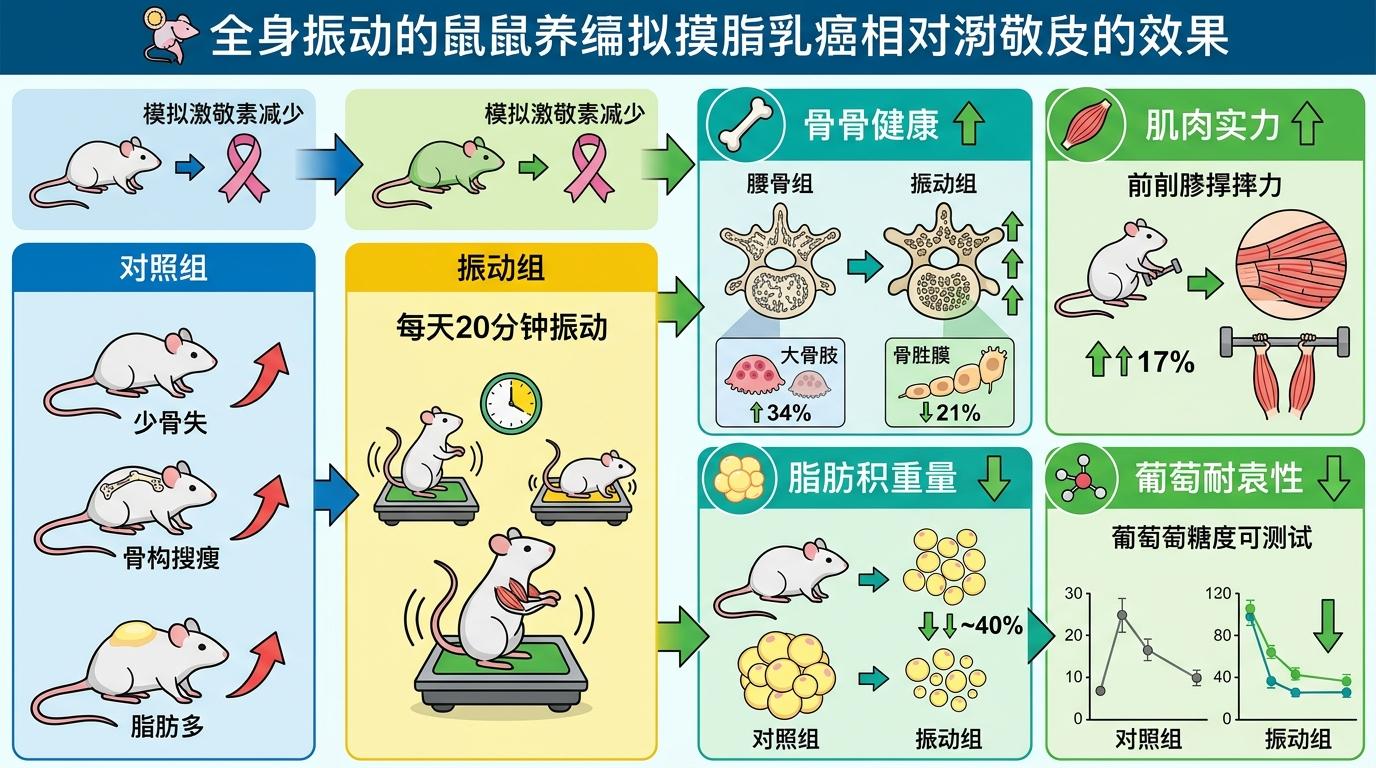
但真实的机制比按摩更精确:振动通过激活骨骼和肌肉细胞表面的机械感受器,触发PI3K/Akt/mTOR信号通路——这条通路就像细胞的“生长开关”,能促进蛋白质合成,抑制肌肉萎缩相关的FoxO1因子活性,同时调节骨髓干细胞的分化方向,让它们更多地变成成骨细胞,而不是脂肪细胞。
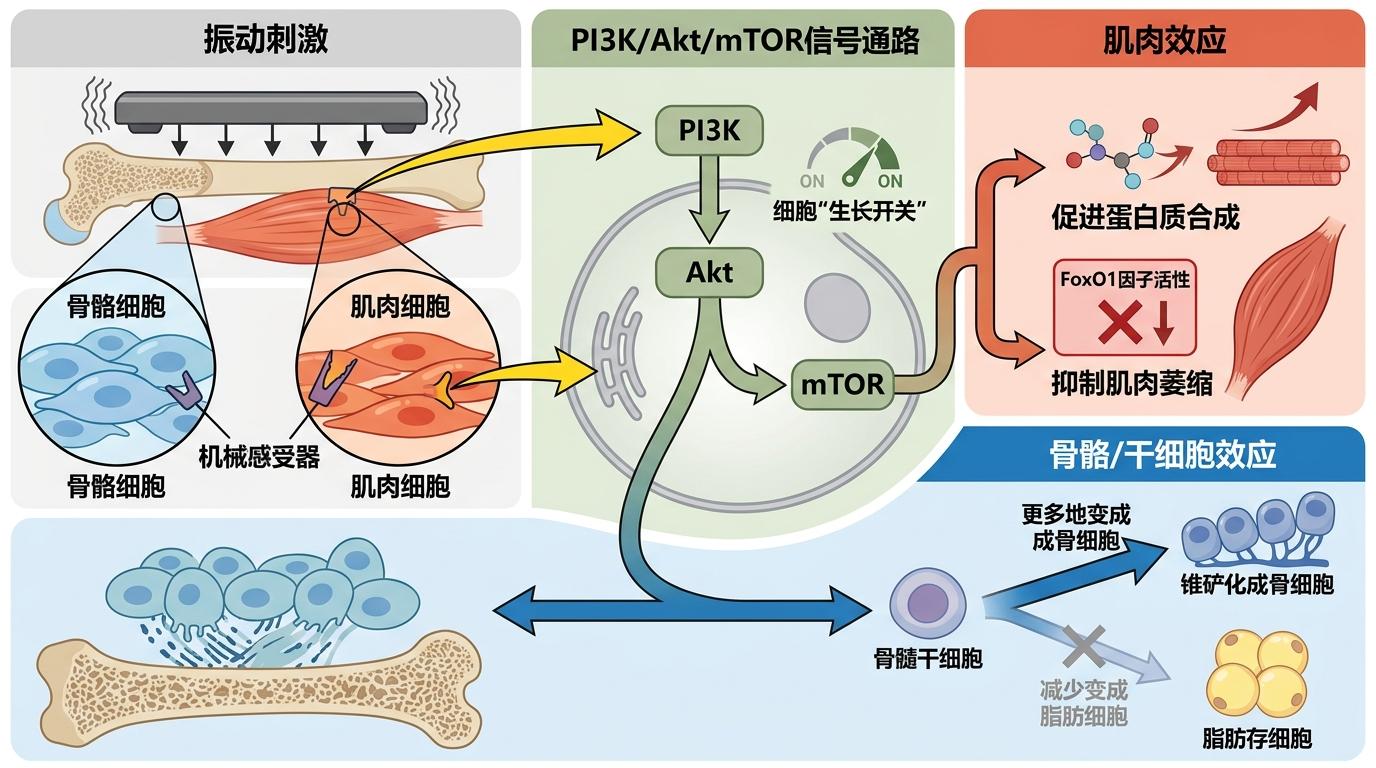
当研究对象换成骨骼已经发育成熟的小鼠时,单独振动的效果开始减弱——就像已经定型的房子,单靠摇晃没法加固地基。但当振动和唑来膦酸联用时,结果超出了预期。
唑来膦酸是临床常用的抗骨吸收药物,它像“胶水”一样附着在骨表面,抑制破骨细胞的骨吸收作用。单独使用时,它能让成熟小鼠的骨密度恢复到接近正常水平,但骨小梁的结构和骨骼的抗折强度仍有欠缺。而振动+唑来膦酸的联合组,全身骨密度比单独用药组又高了9%,腰椎骨小梁的厚度增加了18%,骨骼的极限承载力提升了43%——相当于给房子不仅补了砖,还加固了钢筋。
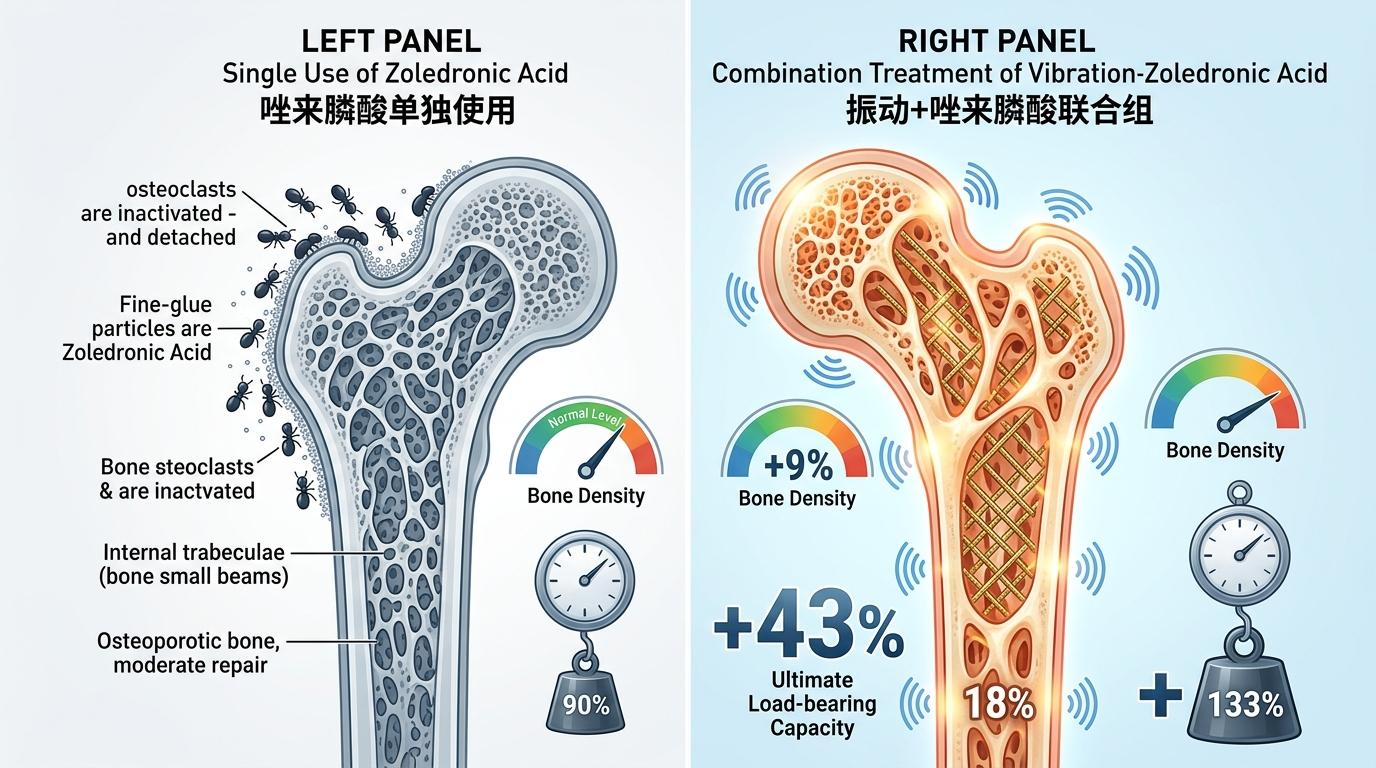
更重要的是这种协同的机制:唑来膦酸守住了骨量的“基本盘”,而振动则激活了骨形成的“主动力”,两者一个“防流失”一个“促生成”,同时还能改善肌肉的抗疲劳能力,减少骨髓脂肪堆积。这一结果直接指向了临床应用的核心:对于骨骼成熟的乳腺癌患者,联合治疗可能是比单一手段更有效的选择。
目前FDA已经批准了针对骨质减少症的低强度振动设备,但要真正走进乳腺癌患者的治疗方案,还有几个关键问题需要解决。
首先是标准化。振动的频率、振幅、每天的时长,这些参数的细微变化都可能影响效果,目前还没有针对乳腺癌患者的统一治疗规范——就像同样的按摩手法,力度和时长不对,效果可能大打折扣。其次是长期安全性,虽然低强度振动在动物实验和小样本临床试验中显示出良好的安全性,但长期使用对心血管、神经系统的潜在影响还需要大规模真实世界数据的验证。
更现实的是患者的依从性。每天20分钟的振动看起来简单,但对于正在接受治疗、身心疲惫的患者来说,坚持下来并不容易。未来或许可以结合可穿戴设备和智能提醒,让这种物理干预更方便融入日常生活。
对于乳腺癌患者来说,治疗从来不是“消灭肿瘤”这一个单一目标,而是在延长生命的同时,尽可能保留生活的质量——能稳稳地走路,能抱动孙子,能正常地工作和社交。低强度振动联合唑来膦酸的研究,正是朝着这个方向迈出的一步:它用非药物的温和方式,弥补了内分泌治疗的短板,也为患者提供了一种更友好的选择。
治疗的本质,是让医学适应人,而不是让人适应医学。当我们开始关注“活着”之外的“生活质量”,那些曾经被忽略的细节,就会变成改变治疗格局的关键。
点击充电,成为大圆镜下一个视频选题!