对抗知识焦虑,从看懂这条开始
App 下载
黏在脂肪上的巨噬细胞,成了减肥新靶点
肥胖|胰岛素抵抗|脂肪组织|黏附相关巨噬细胞|中南大学|代谢内分泌疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
肥胖|胰岛素抵抗|脂肪组织|黏附相关巨噬细胞|中南大学|代谢内分泌疾病|医学健康
当你为腰上的游泳圈发愁时,脂肪里正发生一场隐秘的攻防战——过去我们总把脂肪里的巨噬细胞当成“炎症帮凶”,认定它们是催生胰岛素抵抗、拖垮代谢的罪魁祸首。但中南大学的研究团队在脂肪细胞表面,揪出了一群被完全忽略的“卧底”——黏附相关巨噬细胞(ARMs),它们不仅不搞破坏,还会紧紧贴在脂肪细胞上“干活”,甚至能逆转肥胖带来的代谢紊乱。
为什么这群不起眼的细胞能左右我们的体重?它们到底在脂肪里做了什么?
你可以把脂肪组织想象成一个堆满油桶的仓库,脂肪细胞是一个个胀得圆滚滚的油桶,而ARMs就是守在油桶边的清道夫——它们不像其他巨噬细胞那样在仓库里闲逛,而是直接贴在油桶上。过去科学家分离脂肪细胞时,总把这些黏在油桶上的清道夫当成“杂质”洗掉,直到这次研究团队特意把它们留下来,才发现了它们的本事。
ARMs的核心武器是小窝蛋白-1(CAV-1)——一种像“黏合剂”和“收纳盒”的蛋白:它先帮ARMs牢牢粘在脂肪细胞表面,再让ARMs“偷取”脂肪细胞的mRNA,相当于拿到了油桶的“使用说明书”,从而学会更高效地处理脂质。在肥胖小鼠体内,ARMs的数量能占到脂肪巨噬细胞的70%以上,是脂肪组织里扩增最快的细胞群,就像仓库里油桶越堆越多,清道夫也跟着加了班。
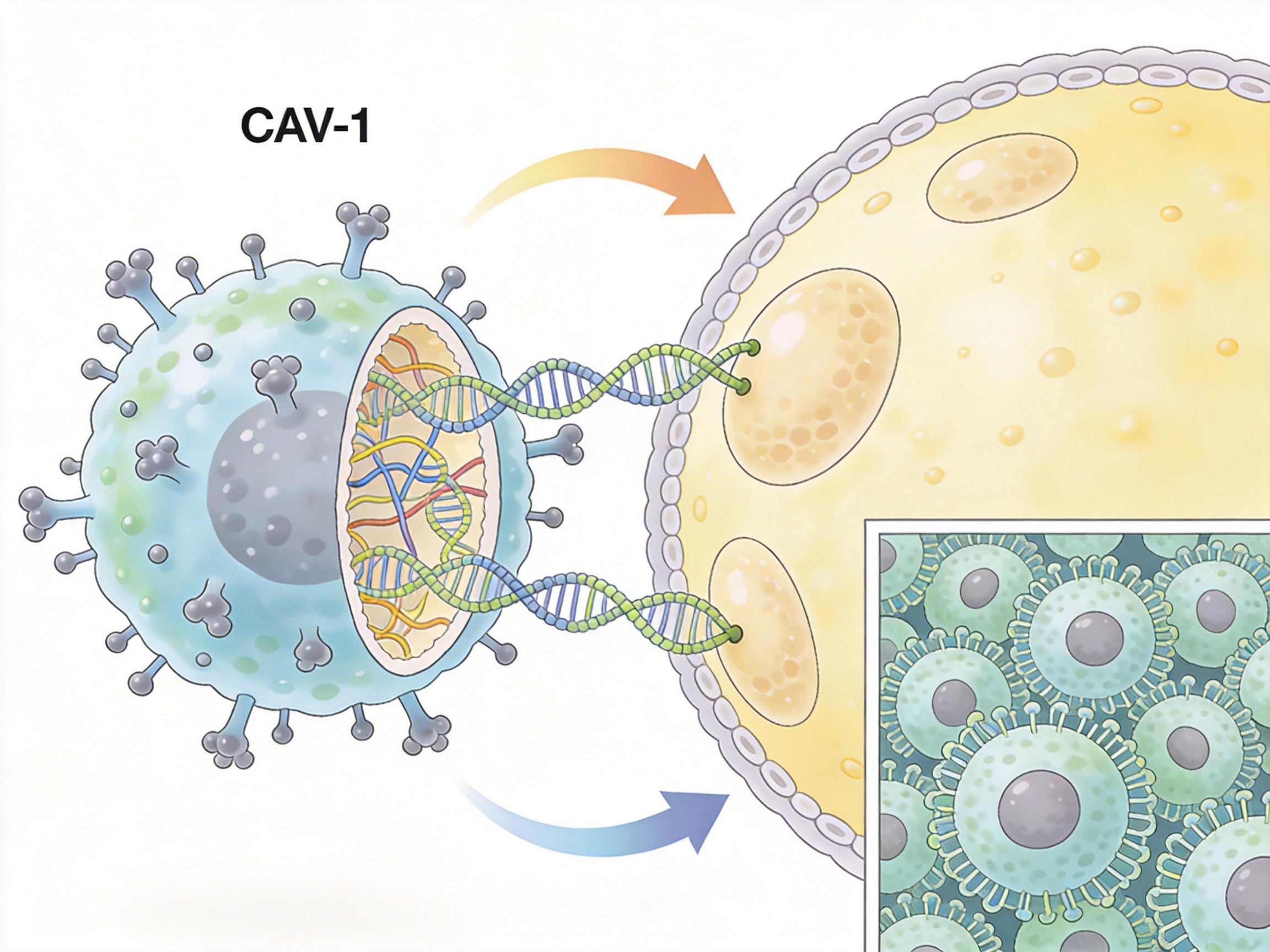
更关键的是,一旦敲除巨噬细胞里的CAV-1,ARMs会立刻“罢工”:黏附能力下降,细胞内的脂质含量骤减,原本被它们盯着的脂肪细胞会疯狂胀大,脂肪组织像吹气球一样扩张,小鼠的血糖也彻底失控。
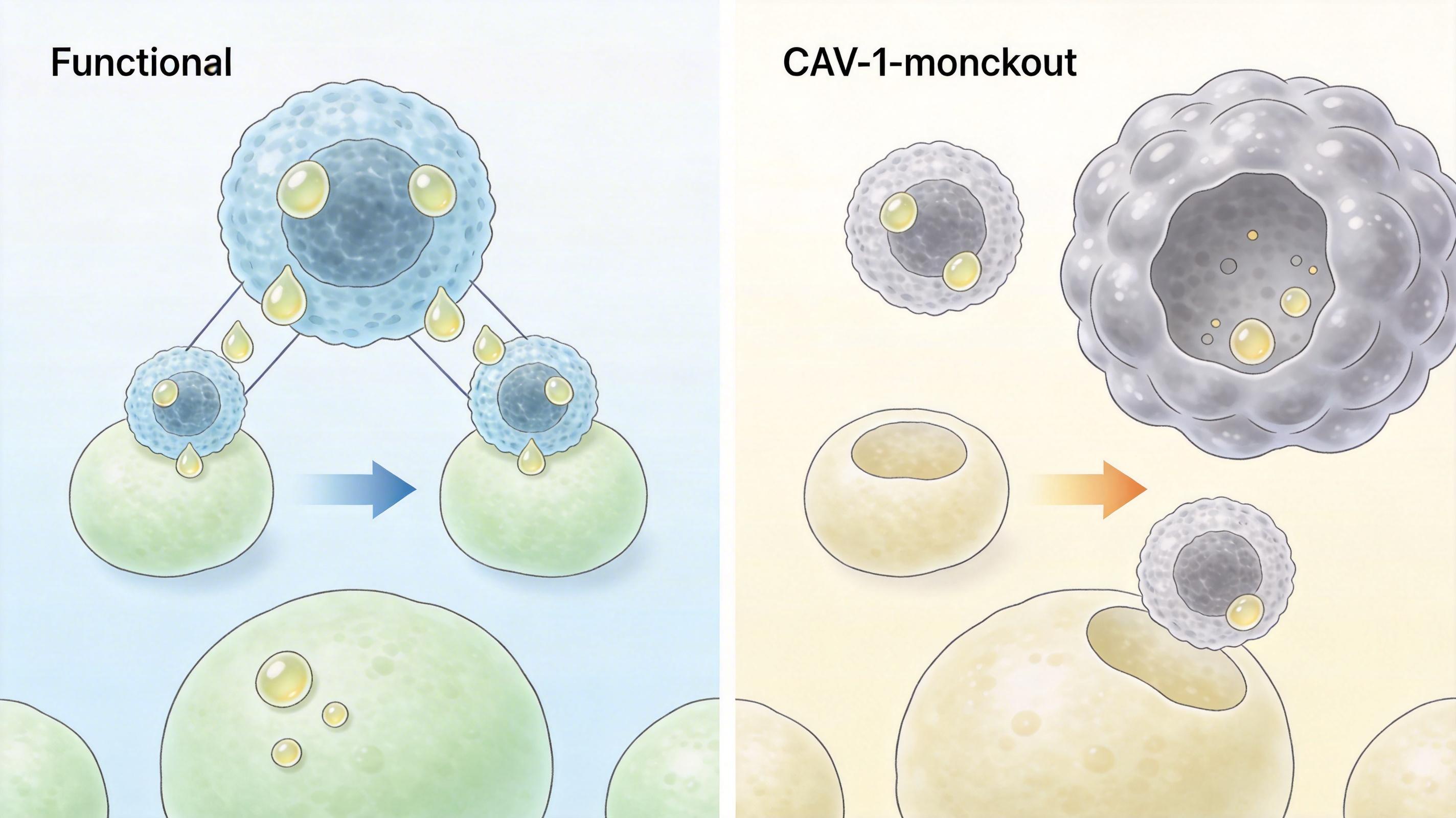
过去我们对脂肪巨噬细胞的认知,一直困在“M1促炎、M2抗炎”的二元框架里——肥胖时M1型巨噬细胞增多,释放炎症因子搞乱代谢,M2型则负责收拾残局。但ARMs的出现,直接打破了这个简单的划分。
它不是单纯的“抗炎卫士”,而是脂肪细胞的“代谢合伙人”:通过直接黏附,ARMs能把脂肪细胞里过量的脂质“抢”过来自己处理,相当于帮脂肪细胞减负,避免它们因过度肥大而坏死。研究团队做了个实验:把瘦小鼠的ARMs注射到肥胖小鼠的脂肪组织里,原本对胰岛素毫无反应的肥胖小鼠,竟然慢慢恢复了代谢能力——就像给堆满垃圾的仓库,空投了一批专业清道夫。
我认为,这是本次研究最有价值的突破:它让我们意识到,脂肪里的巨噬细胞不是只会引发炎症的“破坏者”,它们中存在一群精准调控代谢的“管理者”。之前我们试图用抗炎药物治疗肥胖代谢病效果不佳,恰恰是因为不分好坏地抑制了所有巨噬细胞,反而误伤了ARMs这类“好人”。
ARMs成为治疗靶点的潜力很诱人,但我们得先冷静下来看清现实:目前的研究都还停留在小鼠实验阶段,从实验室到临床,还有几道关键的坎要跨。
首先是特异性的问题。CAV-1不是ARMs独有的蛋白,它在脂肪细胞、内皮细胞里都有表达,直接靶向CAV-1可能会误伤其他细胞,引发意想不到的副作用。比如之前的研究显示,全身敲除CAV-1的小鼠会出现脂肪萎缩,反而患上另一种代谢病。
其次是递送的难题。怎么把体外培养的ARMs精准送到脂肪组织里?怎么保证它们在人体内还能保持“瘦小鼠来源”的代谢功能?这些都是未来要解决的技术问题。不过也不用太悲观——研究团队已经证实,ARMs不仅存在于小鼠体内,在人类脂肪组织里也能找到它们的踪迹,这意味着它的调控机制在人和小鼠之间是保守的,为后续的临床转化打下了基础。
当我们把肥胖单纯当成“吃太多动太少”的问题时,其实忽略了脂肪里这群微观生命的复杂博弈。ARMs的发现,就像给我们打开了一扇新的窗户——原来脂肪组织不是一个被动的“能量仓库”,而是一个由免疫细胞、脂肪细胞相互协作的动态系统。
“代谢的答案,藏在细胞的黏附中。”这句话或许能概括这次研究的核心:我们不必总是想着“消灭脂肪”,有时候找到那些帮脂肪“正常工作”的细胞,反而能更温和地解决代谢问题。未来某一天,当我们把健康的ARMs送进体内,或许就能让膨胀的脂肪组织重新恢复秩序——而这,正是科学最动人的地方:在微观的角落里,找到改变宏观世界的钥匙。