1 个月前

1 个月前
你可能没听过KRAS,但它是结直肠癌里最顽固的“隐形杀手”——约40%的患者体内都有这个突变基因。它不仅驱动肿瘤疯长,还能让癌细胞在免疫系统眼皮底下“隐身”,连如今最火的PD-1免疫疗法,对携带KRAS突变的微卫星稳定型结直肠癌也束手无策,这类患者占了结直肠癌总数的绝大多数。
一直以来,科学家只知道KRAS突变会导致免疫治疗耐药,却摸不透它到底靠什么招数躲避免疫系统的攻击。直到苏州大学和苏州系统医学研究所的团队,在《自然·代谢》上捅破了这层窗户纸:KRAS突变的癌细胞,居然靠一种“化学修饰”直接废掉了免疫细胞的武功。这到底是怎么回事?
要理解这个机制,得先把癌细胞和免疫细胞的关系比作一场战争:CD8+T细胞是冲锋陷阵的“杀手”,专门识别并清除癌细胞;而KRAS突变的癌细胞,就是会搞“化学战”的狡猾对手。
正常情况下,细胞靠分解葡萄糖获取能量,但KRAS突变的癌细胞会启动一种叫“有氧糖酵解”的异常代谢——哪怕氧气充足,也疯狂消耗葡萄糖产生大量乳酸,就像一个只烧煤不供暖的锅炉房。这个过程的关键开关,就是TRIP6蛋白:KRAS突变会激活下游的ERK1/2激酶,给TRIP6蛋白“打上磷酸化标记”,让它失去对ENO2酶的抑制作用。ENO2是糖酵解的关键酶,一旦解绑,就会开足马力生产乳酸,把肿瘤微环境变成“乳酸池”。
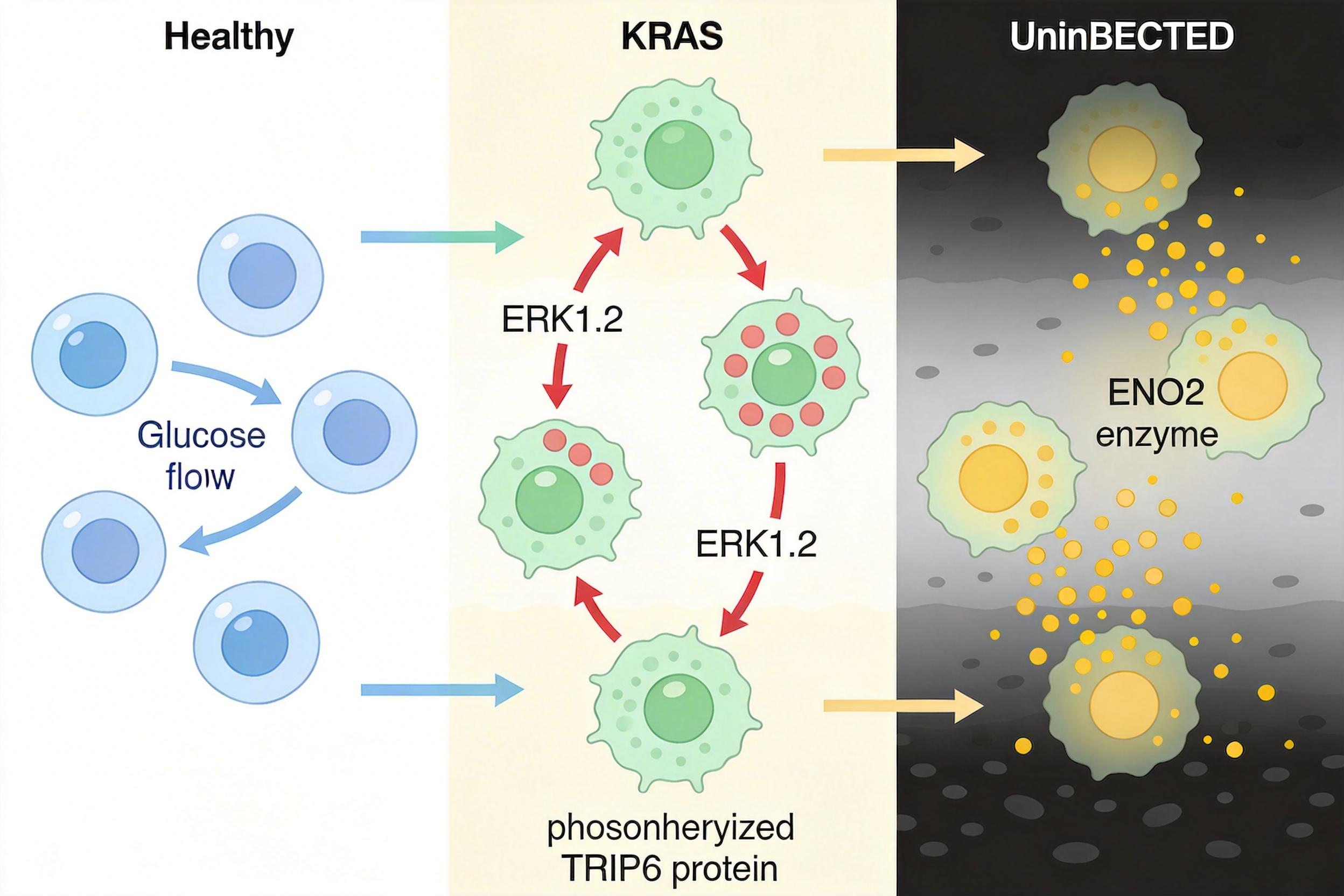
你可以把这个过程想象成:KRAS突变是按下了癌细胞的“代谢加速键”,TRIP6的磷酸化是拆掉了限速牌,ENO2就是踩到底的油门,最终让癌细胞源源不断地向外排放乳酸——这不是代谢废物,而是专门对付免疫细胞的“化学武器”。
过去我们以为,乳酸只是让肿瘤微环境变酸,间接抑制免疫细胞活性,但这次的研究发现了更直接的机制:乳酸会对CD8+T细胞表面的CD44蛋白进行“乳酸化修饰”——简单说,就是给CD44蛋白“贴了个乳酸标签”。
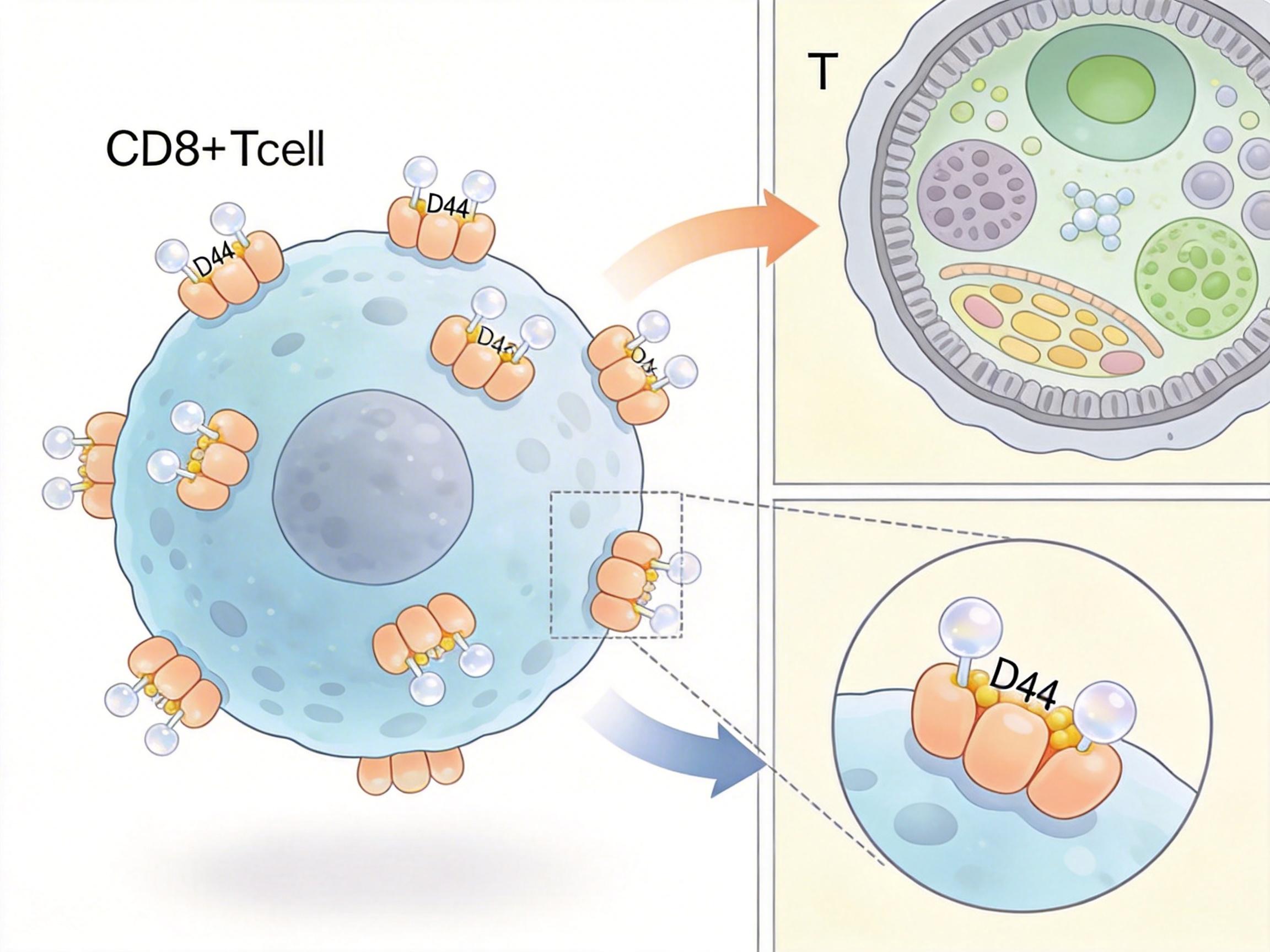
CD44蛋白是T细胞的“导航系统”和“信号开关”,它需要和肿瘤微环境里的透明质酸结合,才能激活AKT信号通路,让T细胞增殖、活化,产生杀伤癌细胞的能力。但乳酸化修饰会破坏CD44和透明质酸的结合,就像把导航仪的天线掰断,T细胞不仅找不到癌细胞,连自身的活化信号也断了,最终变成一群失去战斗力的“废兵”。
研究团队做了一个关键实验:给小鼠注射能阻断TRIP6磷酸化的PT6肽,结果发现癌细胞的乳酸产量大幅下降,CD8+T细胞的AKT信号通路重新激活,原本对PD-1疗法耐药的肿瘤,居然开始被免疫细胞清除——这个TRIP6-ENO2-CD44乳酸化轴,就是KRAS突变癌细胞躲避免疫攻击的核心密码。
我认为,这个发现最有价值的地方,是打破了“代谢只影响微环境”的固有认知,证明代谢产物能直接通过蛋白修饰调控免疫细胞功能,这为癌症免疫治疗开辟了全新的靶点方向。
目前针对KRAS突变的治疗,主要集中在直接抑制KRAS蛋白本身,比如针对G12C突变的索托拉西布,但这类药物只覆盖少数突变亚型,还容易出现耐药。而这次发现的乳酸化轴,不管KRAS是哪种突变亚型,只要它启动了异常糖酵解通路,就可能成为靶点。
在小鼠模型中,PT6肽联合PD-1抑制剂的治疗方案,让KRAS突变肿瘤的生长速度大幅减缓,甚至出现完全消退。更重要的是,这个策略针对的是癌细胞的代谢弱点和免疫抑制机制,不会像直接靶向KRAS那样容易出现靶点突变耐药。
不过,从实验室到临床还有很长的路要走:比如如何把PT6肽改造成适合人体的药物,如何精准阻断乳酸化修饰而不影响正常细胞的代谢,这些都是需要解决的问题。但至少,我们终于找到了一把钥匙,能打开KRAS突变结直肠癌免疫治疗耐药的锁。
当我们把癌症看成一场免疫系统和癌细胞的战争,就会发现:癌细胞的“隐身术”往往不是靠强大的武力,而是靠钻免疫系统的空子——从代谢乱流到蛋白修饰,每一个细微的分子变化,都可能成为免疫逃逸的突破口。
“代谢不止是能量,更是信号”,这句话正在被越来越多的研究证实。这次对乳酸化轴的发现,不仅给KRAS突变结直肠癌患者带来了新希望,更让我们意识到:癌症治疗的下一个突破,可能藏在那些被我们忽略的“代谢细节”里。
未来的癌症治疗,或许不再是单纯的“杀死癌细胞”,而是通过调控代谢和免疫的平衡,让免疫系统重新夺回战场的主动权。
点击充电,成为大圆镜下一个视频选题!