对抗知识焦虑,从看懂这条开始
App 下载
AI造出抗癌“导弹”:精准锁定癌细胞,免疫疗法获重大突破
Science杂志|免疫疗法|癌细胞识别|pMHC分子|T细胞|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
Science杂志|免疫疗法|癌细胞识别|pMHC分子|T细胞|肿瘤学|医学健康
在人体复杂的免疫系统中,T细胞扮演着“巡警”的角色,不知疲倦地在全身巡逻,检查每个细胞出示的“身份证”——一种被称为肽-主要组织相容性复合体(pMHC)的分子。癌细胞的“身份证”上,会展示一些由基因突变产生的异常肽段。理论上,T细胞一旦发现这种异常,就应立即清除威胁。然而,癌细胞极其狡猾,它们的异常标记往往与正常细胞的标记仅有细微差别,导致T细胞“眼神不好”,要么视而不见,要么错杀无辜,这正是癌症免疫治疗长期面临的“识别困境”。
2025年7月24日,顶级学术期刊《科学》(Science)以前所未有的“背靠背”形式,同时刊发了三篇重磅研究,宣告人工智能(AI)已为这一困境带来了革命性的解决方案。来自华盛顿大学的诺奖得主David Baker团队、丹麦技术大学的Timothy P. Jenkins团队以及斯坦福大学的K. Christopher Garcia团队,不约而同地利用生成式AI,成功设计出全新的蛋白质分子。这些“人工受体”如同被赋予了“火眼金睛”的智能导弹,能够以极高的精度识别并结合癌细胞表面的独特标记,为精准癌症免疫治疗开辟了全新路径。
这三项研究的核心成果惊人地一致:
要理解这一突破的意义,必须先了解“癌症身份证”的构造。细胞表面的MHC分子好比一个“展示架”,它上面搭载的肽段则是“展品”。健康的细胞展示的是正常的“自身肽”,而癌细胞则会展示突变的“肿瘤肽”。
传统的CAR-T疗法,如同给T细胞装上了一副“通用眼镜”,能识别一些广泛存在于癌细胞表面的蛋白质,但在实体瘤中,这类通用靶点稀少,且常存在于少量正常组织中,导致“脱靶效应”。更理想的策略是识别MHC呈递的肿瘤肽,因为这些肽段来源于细胞内部,揭示了癌症最核心的突变信息,靶点库也因此扩大了数百倍。
然而,这条路困难重重。首先,每个人的MHC“展示架”型号(即HLA分型)多达成千上万种,且肿瘤“展品”也因人而异,导致寻找能精准识别特定“展品+展架”组合的天然T细胞受体如同大海捞针。其次,最关键的挑战在于,设计的受体必须只看“展品”(肽),不理“展架”(MHC),因为“展架”在健康细胞上普遍存在。传统筛选方法耗时、昂贵且成功率极低,严重制约了个性化免疫治疗的发展。
此次突破的关键,在于一种名为RFdiffusion的生成式AI模型。它的工作方式,颠覆了传统的蛋白质设计范式。如果说传统方法是“众里寻他千百度”,那么AI则是“神笔马良”,直接“画”出我们想要的东西。
RFdiffusion的灵感源于DALL-E等图像生成AI。研究人员给它一个目标——癌细胞的pMHC复合物结构,AI便从一团随机的原子“噪声”云开始,通过数百步的“去噪”过程,逐步“雕刻”出一个全新的、能在三维空间中与目标完美互补的蛋白质骨架。这个过程完全摆脱了对自然界现有蛋白质模板的依赖。
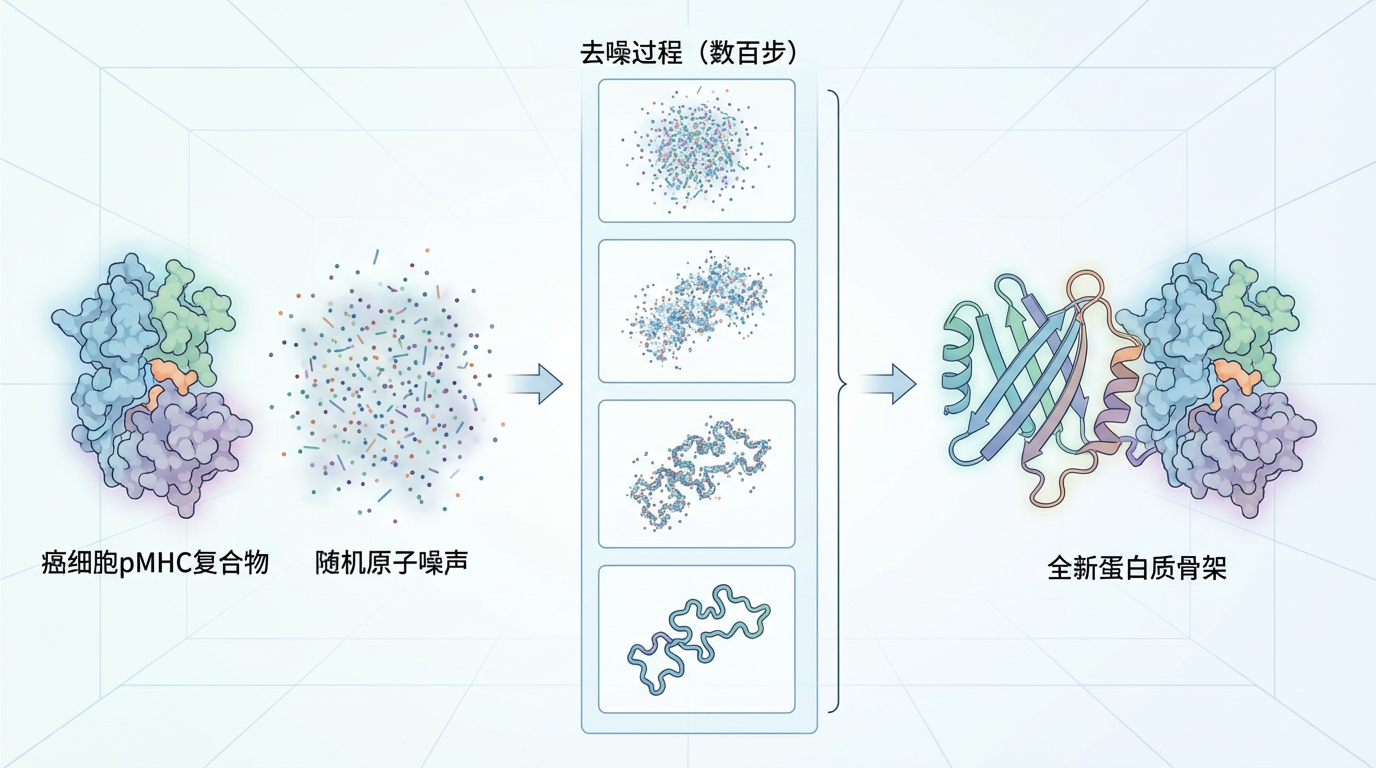
骨架诞生后,另一款AI工具ProteinMPNN接力上场,为这个骨架“填充”上最合适的氨基酸序列,确保它能稳定折叠。最后,被誉为“结构预测之神”的AlphaFold则扮演“质检员”的角色,检验最终设计的蛋白质序列是否真能形成预想中的结构并与靶点结合。
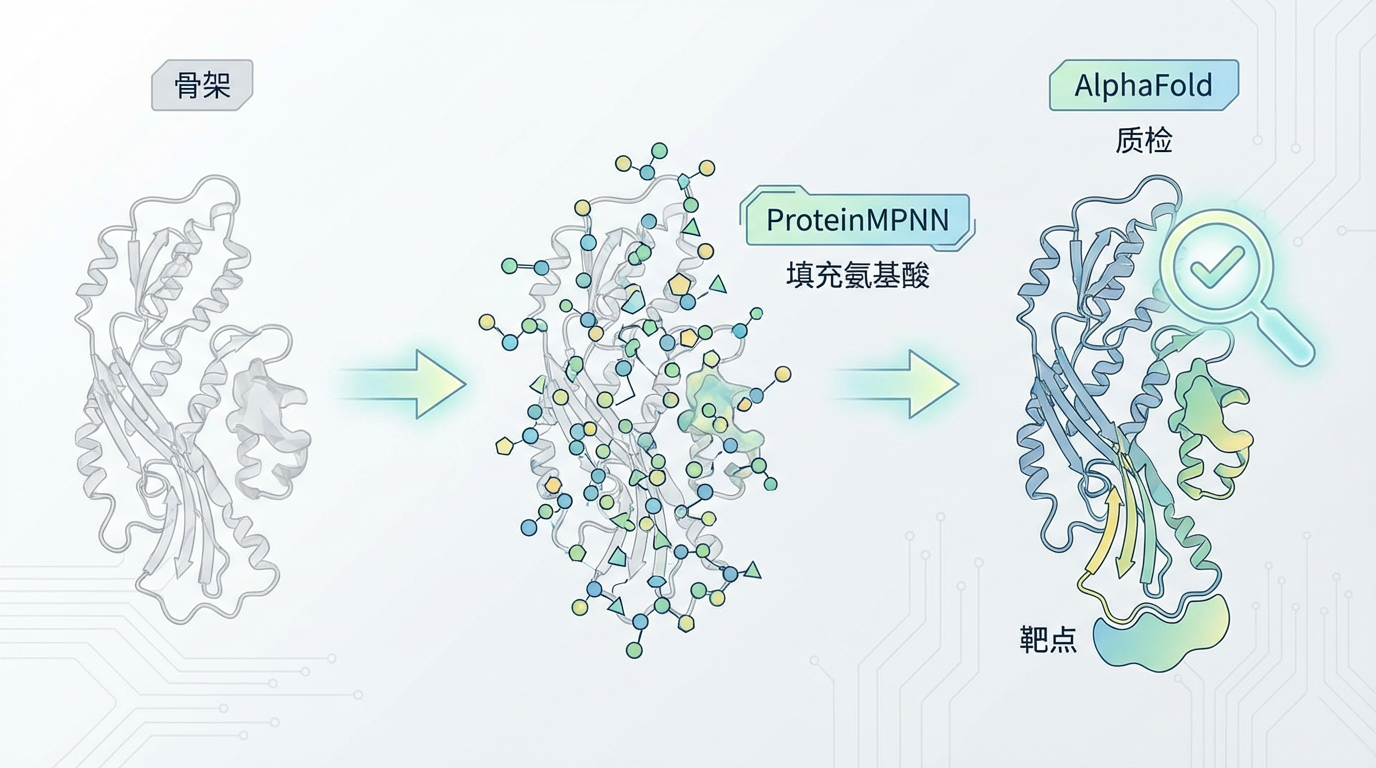
这一“设计-填充-检验”的AI流水线,将过去需要数年摸索的蛋白质设计过程,缩短到了惊人的几周甚至几天。
AI设计的“分子导弹”不仅速度快,其性能更是达到了前所未有的高度。
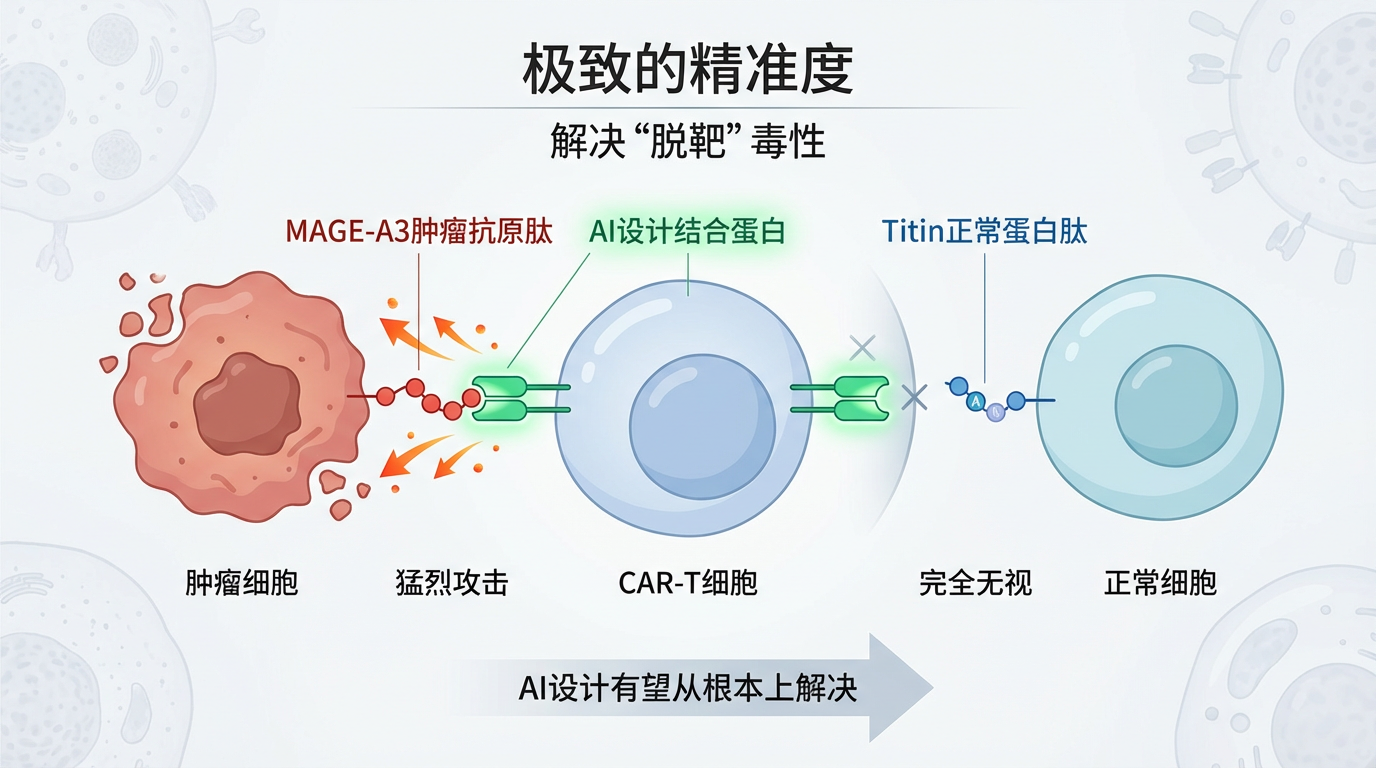
强大的结合力:这些从头设计的蛋白与靶点的结合亲和力达到了纳摩尔甚至皮摩尔级别,远超许多天然存在的受体,确保了“导弹”一旦锁定目标便能牢牢结合。
可靠的杀伤功能:实验证明,装备了AI设计蛋白的CAR-T细胞,在体外实验中能够高效、特异性地清除携带相应肿瘤标志物的靶细胞,杀伤效率最高可达80%以上,而对无关细胞则“秋毫无犯”。
更令人兴奋的是,该技术平台具有极强的延展性。研究人员甚至在没有靶标实验结构的情况下,仅依靠AlphaFold预测的结构作为蓝图,就成功设计出了功能性的结合蛋白,这意味着AI可以为大量“未知结构”的靶点快速开发靶向药物。
《科学》杂志同日刊发三篇论文的盛况,标志着一个领域的范式转变。AI驱动的蛋白质设计,正将癌症免疫治疗从“经验筛选”时代,推向“智能创造”时代。
这一突破的深远影响体现在多个层面:
药物研发的“民主化”:过去只有少数顶尖实验室能承担的TCR筛选工作,如今任何具备计算能力的团队都可以快速设计和迭代。这有望催生一个庞大的、覆盖各类常见肿瘤抗原和HLA类型的“现成”结合蛋白库。
真正的个性化治疗:对于每一位癌症患者,理论上都可以通过对其肿瘤进行测序,识别出独特的“新抗原”,然后利用AI在数周内为其量身定做一套CAR-T疗法。这曾是科幻小说里的情节,如今正成为触手可及的现实。
超越癌症:该技术同样适用于病毒感染等其他疾病。AI设计的蛋白可以引导免疫系统精准清除被病毒感染的细胞,为艾滋病、慢性肝炎等顽疾提供新的治疗思路。
当然,从实验室的成功走向临床应用,仍有漫长的道路要走,包括严格的临床试验验证、规模化生产工艺的建立以及应对复杂的监管审批。但毫无疑问,最关键的科学瓶颈已经被打破。我们不再仅仅是训练免疫细胞,而是为它们锻造前所未见的“神兵利器”。这场由AI引领的生物学革命,正为人类战胜癌症的漫长征途,点亮一盏无比璀璨的希望之灯。