
1 个月前

1 个月前
14岁的男孩躺在病床上,左腿膝盖的肿块已经突破皮肤——这是骨肉瘤,儿童和青少年最凶险的原发骨肿瘤。他接受了标准化疗,肿块却还在疯长。医生试过PD-1抑制剂,这是如今癌症治疗的“明星药”,但对他的肿瘤几乎无效。
不是药不好,是骨肉瘤太“特殊”:它像个基因拼接的怪物,每一个患者的肿瘤都长得不一样,还会把免疫系统挡在门外。过去30年,这种病的转移患者5年生存率始终停留在20%左右,连医生都觉得无力。直到上海的研究团队,给这些“不听话”的肿瘤,建了一个1:1的“孪生实验室”。
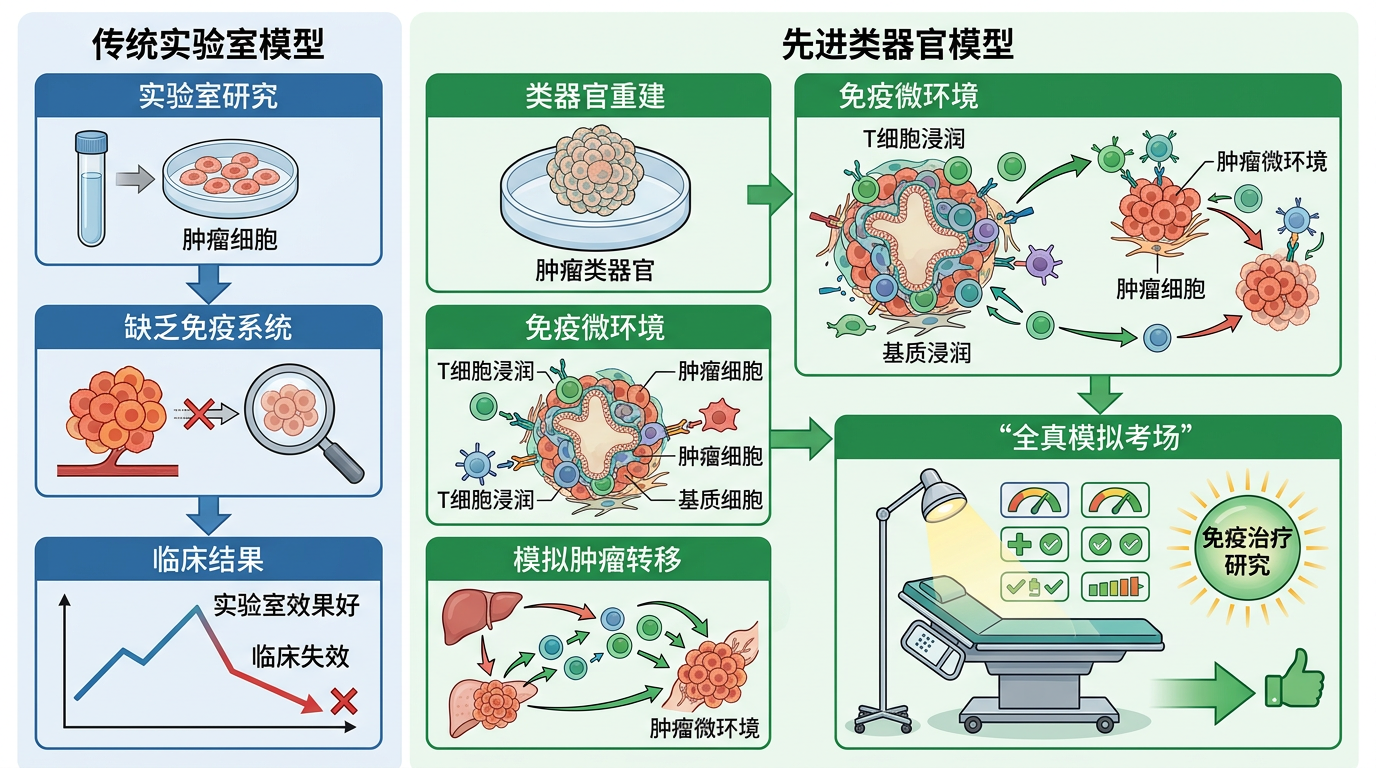
你可以把过去的肿瘤研究模型,看成两种不合格的“替身演员”:一种是把患者肿瘤细胞种在免疫缺陷小鼠身上的PDX模型,它能模拟肿瘤的生长,但小鼠没有人类的免疫系统,没法测试免疫治疗的效果;另一种是类器官模型,虽然能在试管里长出肿瘤的结构,却留不住肿瘤周围的免疫细胞,像个没有“背景板”的舞台。
这次上海团队的突破,是把这两个模型“焊”在了一起——他们从患者体内取出肿瘤细胞,用“自组装”技术快速拼成毫米级的类器官,同时保留了对应的PDX模型,形成一个“互动式生物样本库”。简单说,就是给每个患者的肿瘤做了两个“替身”:一个在小鼠身上长,用来模拟肿瘤的真实生长;一个在试管里活,用来测试各种药物的效果。
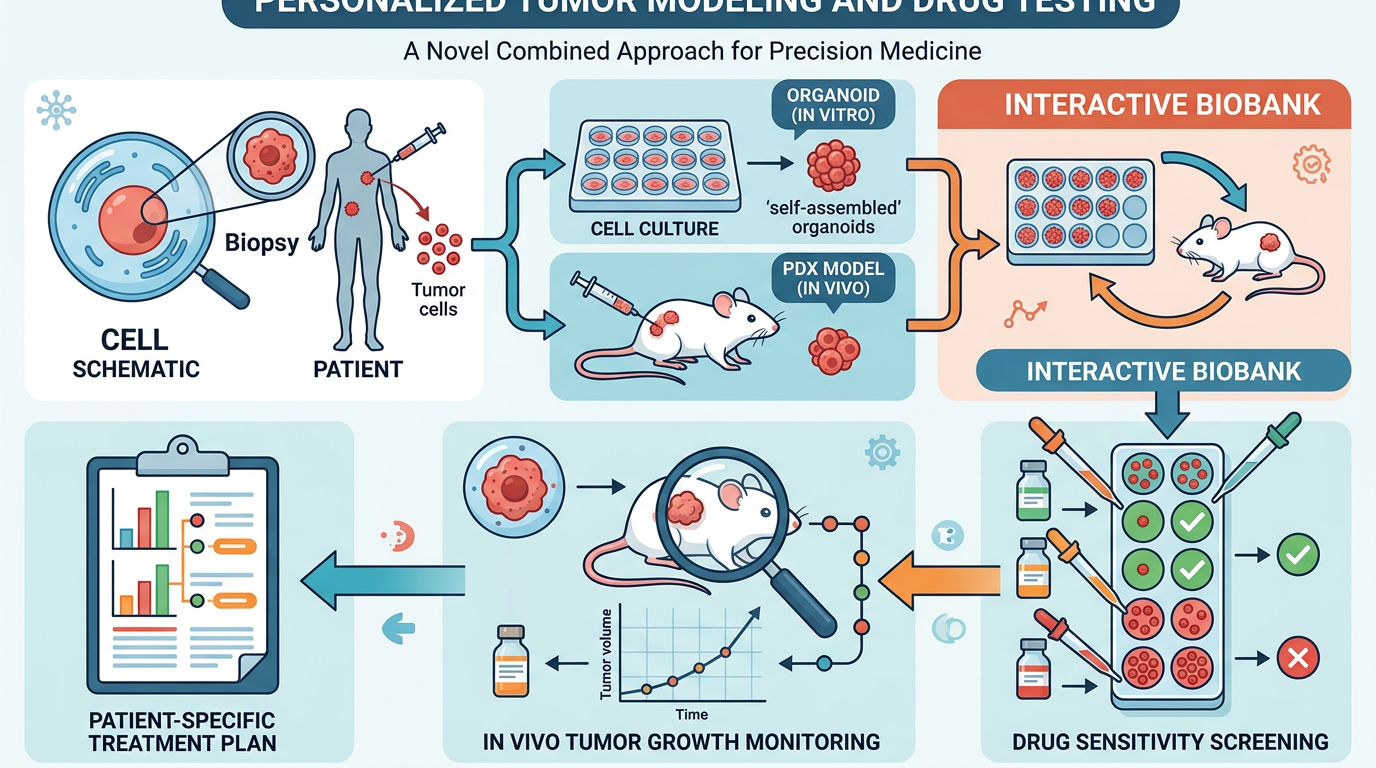
这个“替身”有多像?他们用显微镜看,类器官的细胞排列、蛋白标记和患者的肿瘤一模一样;测基因,90%以上的突变都被保留了;甚至把类器官再种回小鼠体内,还能长出和原发肿瘤一样的肿块。更关键的是,他们还在类器官里“种”进了患者的免疫细胞——那些原本被肿瘤挡在门外的T细胞,终于能在这个“孪生实验室”里和肿瘤正面交手了。
骨肉瘤之所以对PD-1抑制剂不敏感,是因为它是个“冷肿瘤”——肿瘤周围几乎没有能杀伤癌细胞的CD8+T细胞,就像一座没有守军的城池,免疫药根本找不到目标。
研究团队在这个“孪生实验室”里发现,有一种骨肉瘤患者,体内的Chr9p21.3基因片段缺失了——这种缺失会让肿瘤变得更“冷”,PD-1抑制剂几乎完全无效。但他们同时发现,这种缺失的肿瘤有个“命门”:PRMT5蛋白的活性异常。
他们用一种叫APRN2169的PRMT5抑制剂,和PD-1抑制剂一起给类器官“吃药”,结果让人震惊:原本躲在外面的CD8+T细胞,像潮水一样涌进了肿瘤内部;这些T细胞开始分泌细胞毒素,把癌细胞一个个杀死;在小鼠模型里,联合用药让肿瘤缩小了70%以上,而单独用PD-1抑制剂,肿瘤几乎没变化。
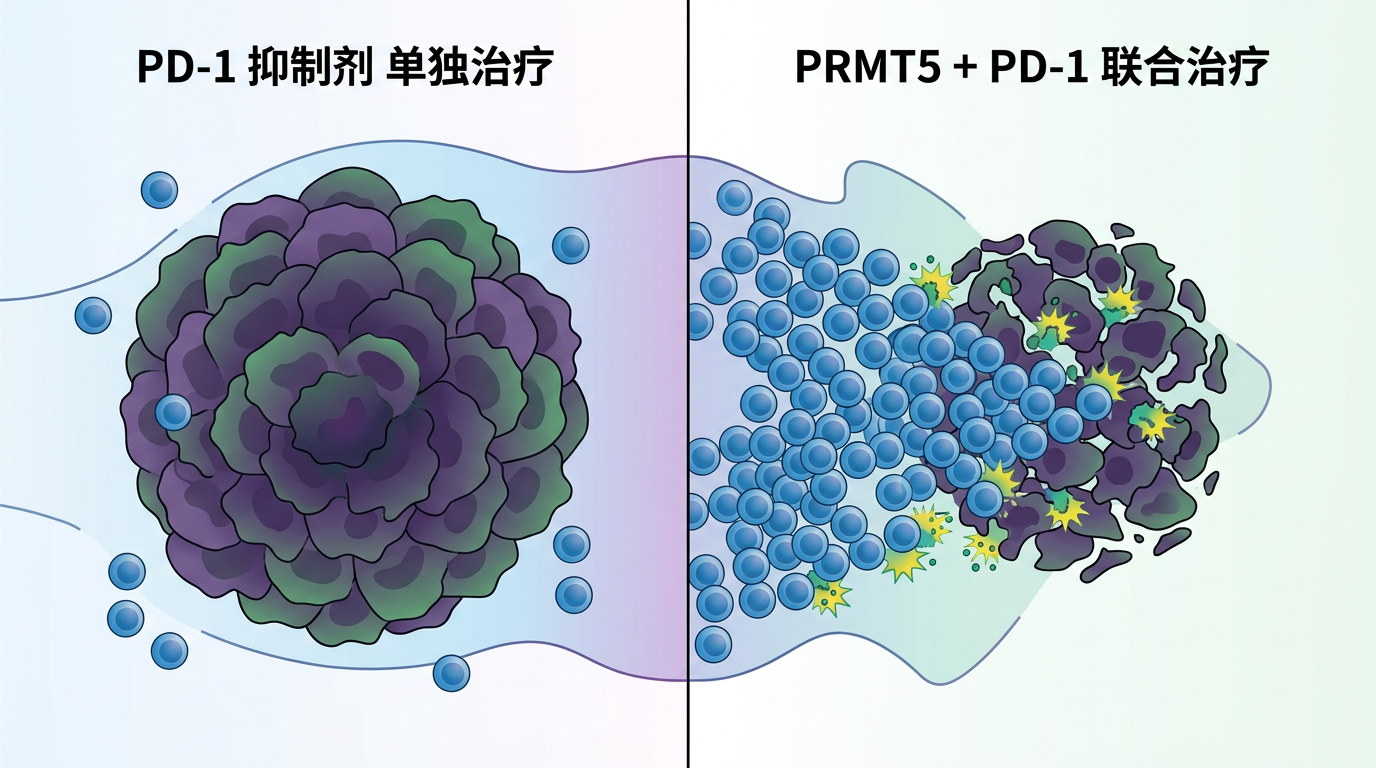
我认为,这才是这项研究最有价值的地方——它不是找到了一种新的“神药”,而是找到了一种“精准配对”的方法:先通过基因检测,找出那些Chr9p21.3缺失的患者,再用PRMT5抑制剂把“冷肿瘤”加热,最后用PD-1抑制剂发动攻击。这就是“基因型分层+免疫联合”的个体化治疗范式,简单说就是“给对的人,用对的药”。
这项研究的意义,不止于骨肉瘤。
罕见病的研究一直面临一个困境:患者太少,样本难得,很难做大规模的临床试验。而这个“PDX-类器官互动式生物样本库”,相当于把每个患者的肿瘤都“永久保存”了下来——即使患者去世了,他的肿瘤还能在实验室里继续生长、被研究。
更重要的是,这个模型解决了免疫治疗研究的核心难题:如何在实验室里模拟患者真实的免疫微环境。过去,很多免疫药在实验室里效果很好,一到临床上就失效,就是因为模型里没有免疫系统。而现在,研究团队能在类器官里重建T细胞浸润,甚至能模拟肿瘤转移后的免疫环境,这相当于给免疫治疗的研究,建了一个“全真模拟考场”。
当然,这项研究也有局限:目前只验证了Chr9p21.3缺失这一种亚型的骨肉瘤,还有很多其他亚型的患者,需要更多的研究来找到他们的“命门”。而且,从实验室到临床,还有很长的路要走——APRN2169这种药,还需要经过临床试验的验证,才能真正用到患者身上。
那个14岁的男孩,或许还在等待有效的治疗方案。但这项研究,给了他和成千上万的骨肉瘤患者一个新的希望。
我们总说,精准医疗是未来的方向,但精准医疗不是一句空话——它需要科学家给每一种肿瘤,都建一个这样的“孪生实验室”;需要医生给每一个患者,都做一次精准的基因检测;需要药企,为这些罕见的亚型,开发对应的药物。
精准的本质,是看见每一个独一无二的患者。
未来的癌症治疗,或许不再是“一种药治所有人”,而是“一个患者一套方案”。而这个“孪生实验室”,就是通往未来的第一块铺路石。
点击充电,成为大圆镜下一个视频选题!