对抗知识焦虑,从看懂这条开始
App 下载
肠道细菌分泌的酶,能给免疫治疗“开外挂”
PD-L1蛋白|癌症免疫逃逸|结直肠癌|fpPRPS酶|普拉梭菌|肿瘤学|微生物组学|生命科学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
PD-L1蛋白|癌症免疫逃逸|结直肠癌|fpPRPS酶|普拉梭菌|肿瘤学|微生物组学|生命科学|医学健康
2026年4月的一个实验室深夜,上海交通大学的团队盯着显微镜下的图像——那些原本躲在肠道里的普拉梭菌,居然能让结直肠癌细胞的“隐身斗篷”失效。更关键的是,它不是直接攻击癌细胞,而是通过分泌一种叫fpPRPS的酶,掐断癌细胞的能量供应,让免疫细胞重新认出敌人。
结直肠癌是全球第三大癌症,每年夺走近百万条生命,免疫治疗对很多患者来说效果寥寥。但这次的发现,让人们第一次看清:肠道里最常见的益生菌,居然藏着能破解癌症免疫逃逸的钥匙。问题是,它到底是怎么做到的?
你可以把癌细胞想象成一个狡猾的入侵者,它会在细胞膜上贴满PD-L1蛋白——这就像给免疫细胞递了一张“别打我”的通行证,让负责攻击的CD8+T细胞失去战斗力,陷入“耗竭”状态。这就是为什么很多免疫治疗会失败:癌细胞的隐身术太成功了。
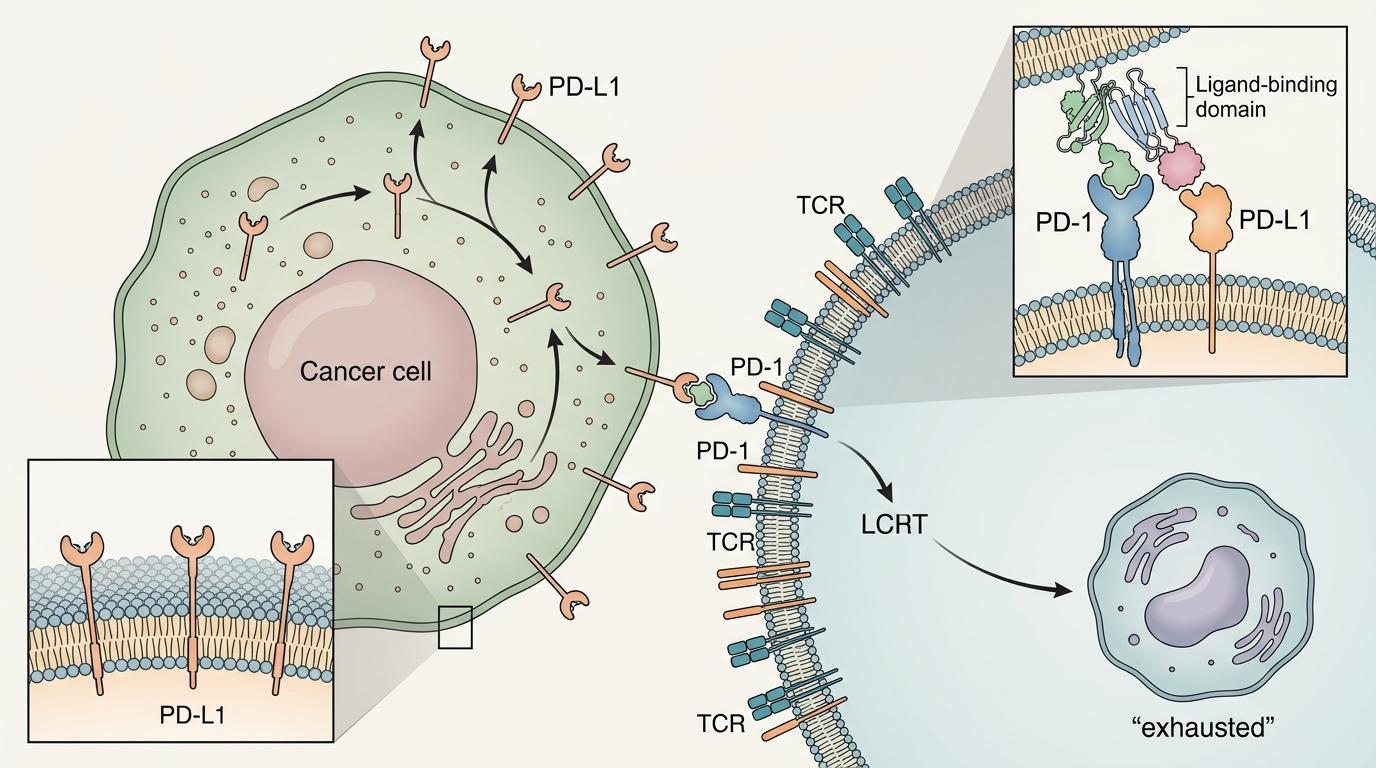
而普拉梭菌分泌的fpPRPS酶,走了一条完全不同的路。它不直接破坏PD-L1,而是先耗尽癌细胞里的ATP——也就是细胞的“能量货币”。就像断了入侵者的电,让它连制造和运输“通行证”的力气都没有。
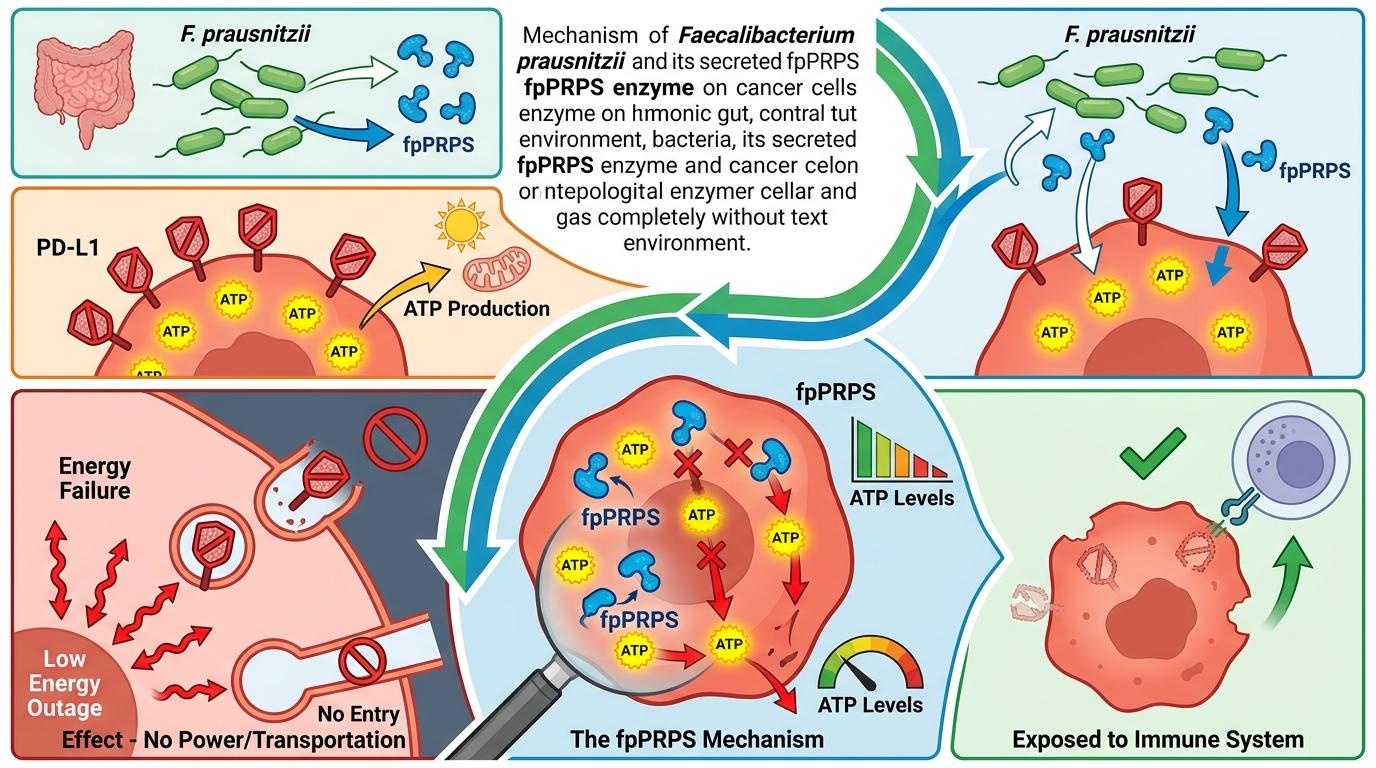
具体的机制可以拆成三步:
当癌细胞的PD-L1含量下降,CD8+T细胞就会从耗竭状态苏醒,重新发起攻击。
动物实验已经给出了漂亮的结果:给患结直肠癌的小鼠同时注射fpPRPS和抗PD-1抗体,肿瘤体积缩小的幅度是单独用免疫治疗的两倍多,CD8+T细胞的数量也翻了一番。但从老鼠身上的成功,到真正用到患者身上,还有几道绕不开的坎。
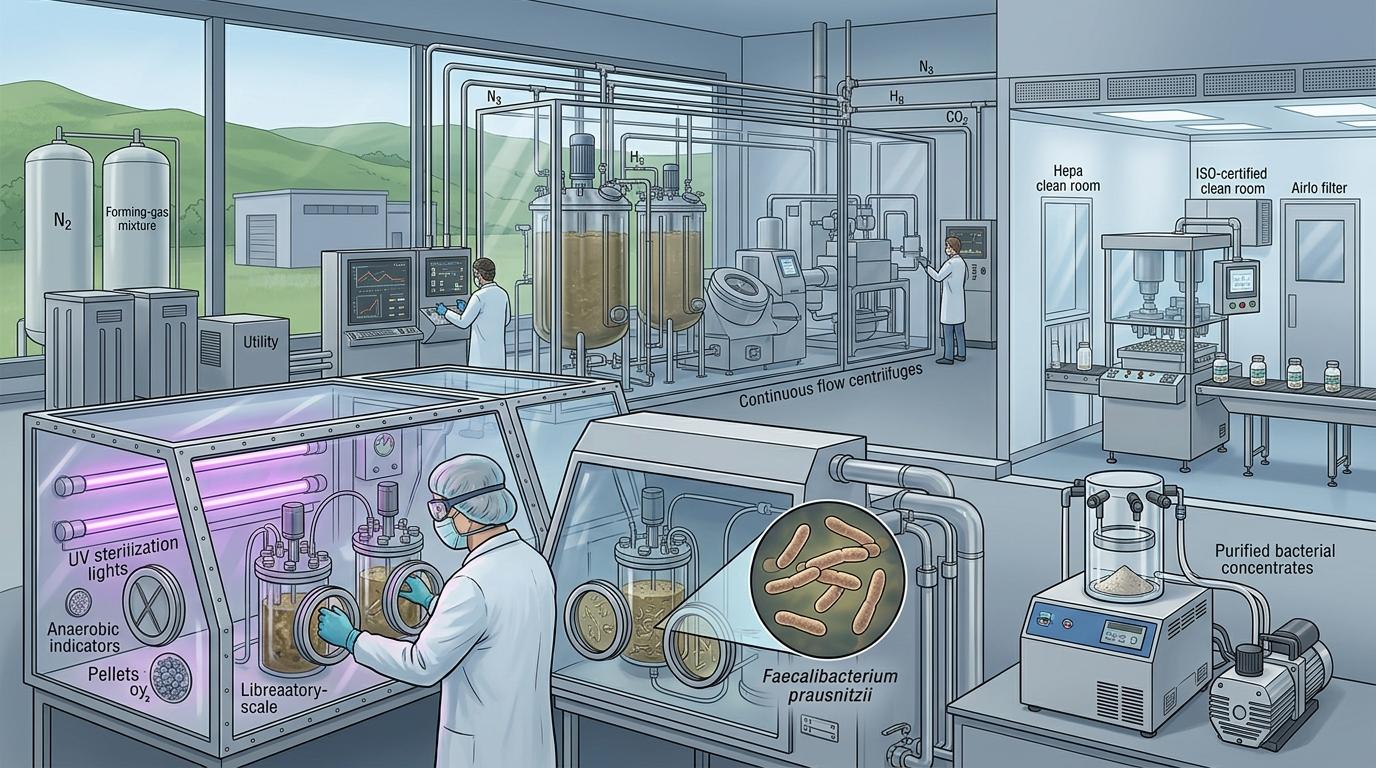
首先是普拉梭菌本身的特性——它是极端厌氧菌,对氧气极其敏感。就像见光死的吸血鬼,从培养、提纯到做成能口服的制剂,每一步都要在严格无氧的环境下进行,成本高不说,还很难保证活性。目前的实验室提纯技术,还没法大规模生产稳定的fpPRPS制剂。
其次是个体差异的问题。每个人的肠道菌群都像独一无二的指纹,普拉梭菌在有的人肠道里本来就多,有的人却几乎没有。这意味着,补充fpPRPS的效果可能因人而异,需要先给患者做菌群检测,再定制治疗方案——这对精准医疗的要求极高。
更关键的是安全性。虽然动物实验里没发现明显的副作用,但人体的免疫系统比小鼠复杂得多。fpPRPS会不会打乱肠道里的菌群平衡?会不会引发过度免疫反应?这些都需要大规模的临床试验来验证。
其实,普拉梭菌早就不是肠道里的无名之辈。它是肠道里含量最高的益生菌之一,能产生丁酸盐这种抗炎物质,维持肠道屏障的稳定。之前的研究就发现,普拉梭菌的减少和结直肠癌、肠炎等疾病密切相关,补充它能增强免疫治疗的效果,但没人知道具体是哪种成分在起作用。
这次发现的fpPRPS,让人们第一次看清了“菌-癌”对话的具体分子机制——原来细菌不仅能通过代谢产物影响肠道环境,还能分泌酶直接调控癌细胞的代谢。这相当于打开了一扇新的大门:除了普拉梭菌,肠道里还有成千上万种细菌,它们会不会也藏着类似的“抗癌武器”?
比如,已经有研究发现,另一种肠道菌阿克曼氏菌能增强黑色素瘤的免疫治疗效果,还有的细菌能调节肿瘤微环境里的免疫细胞。未来,我们或许能从肠道菌群里筛选出更多的“抗癌分子”,甚至通过基因工程改造细菌,让它们精准分泌治疗酶。
当我们把目光从手术刀、化疗药转向肠道里的微生物时,才发现人体从来不是一个单独的“个体”——我们和肠道里的万亿细菌共生,它们影响着我们的健康,甚至能决定癌症治疗的成败。
fpPRPS的发现,不是找到了一种万能的抗癌药,而是给我们指了一条新的路:与其和癌细胞硬碰硬,不如利用共生的力量,重新唤醒我们的免疫系统。毕竟,最好的医生,可能一直就在我们的肠道里。
肠道菌群,是藏在体内的抗癌盟友。