对抗知识焦虑,从看懂这条开始
App 下载
新冠致听力损失,竟绕开了炎症直接伤神经
内耳切片|螺旋神经节神经元|感音神经性听力损失|新冠病毒|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
内耳切片|螺旋神经节神经元|感音神经性听力损失|新冠病毒|感染性疾病|医学健康
2026年4月的一个实验室清晨,华中科技大学的研究者们盯着显微镜下的小鼠内耳切片,终于确认了那个悬在全球数千万新冠康复者心头的猜测——新冠病毒真的能钻进耳朵里。此前,已有流行病学数据敲过警钟:每1000名感染新冠的青壮年里,就有3到4人会突发感音神经性听力损失,风险是未感染者的3.4倍。但没人能说清,病毒是怎么绕过呼吸道,悄悄啃噬听觉的关键神经的。这一次,他们不仅找到了病毒的入侵痕迹,还揪出了一条完全不同于炎症风暴的隐秘损伤路径。
你可以把内耳想象成一套精密的收音系统:耳蜗里的毛细胞负责捕捉声波,而螺旋神经节神经元(SGNs)就是连接毛细胞和大脑的「信号中转站」——它把声波转换成电信号,再一路传去听觉中枢。一旦这些神经元受损,哪怕毛细胞完好,大脑也收不到声音。
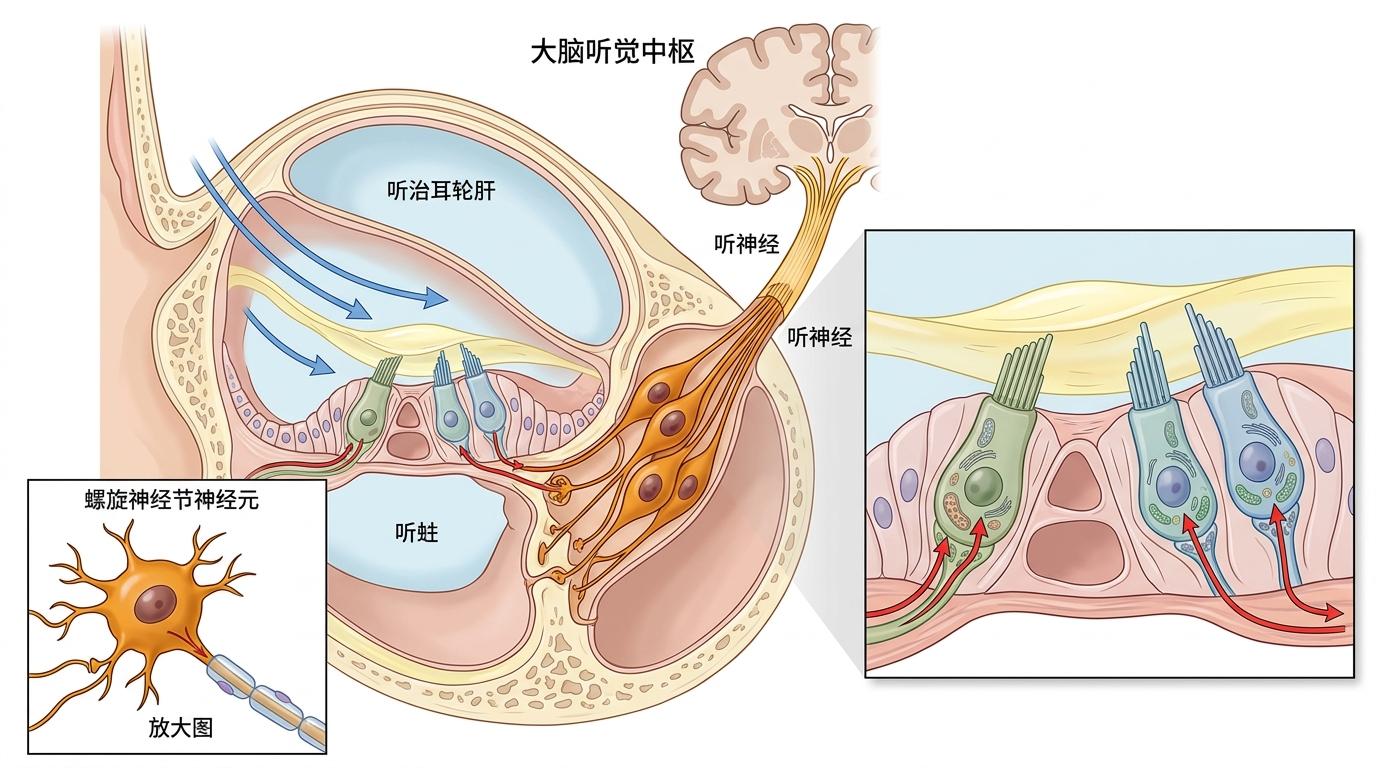
研究者用4种新冠毒株(原始株、Delta、BA.1、BA.2)感染表达人类ACE2受体的K18-ACE2小鼠后,在所有小鼠的内耳里都找到了病毒的踪迹,且病毒精准瞄准了螺旋神经节神经元。更关键的是,这些神经元的死亡并非来自炎症细胞的攻击——实验室检测显示,小鼠内耳几乎没有明显的炎症浸润。
真正的凶手藏在细胞内部:病毒的刺突蛋白(S蛋白)进入神经元后,会直接抑制mTOR信号通路。你可以把mTOR通路理解为细胞的「代谢总开关」,它管着细胞的生长、蛋白合成和存活。当这个开关被按下,细胞会启动应急机制,一种叫G3BP1的蛋白会异常聚集形成应激颗粒——原本这是细胞应对压力的自我保护,但新冠病毒让这种保护变成了自杀:应激颗粒的异常聚集会触发细胞内的「相分离」,就像油水分离一样,细胞内的关键物质被打乱,最终导致神经元凋亡。
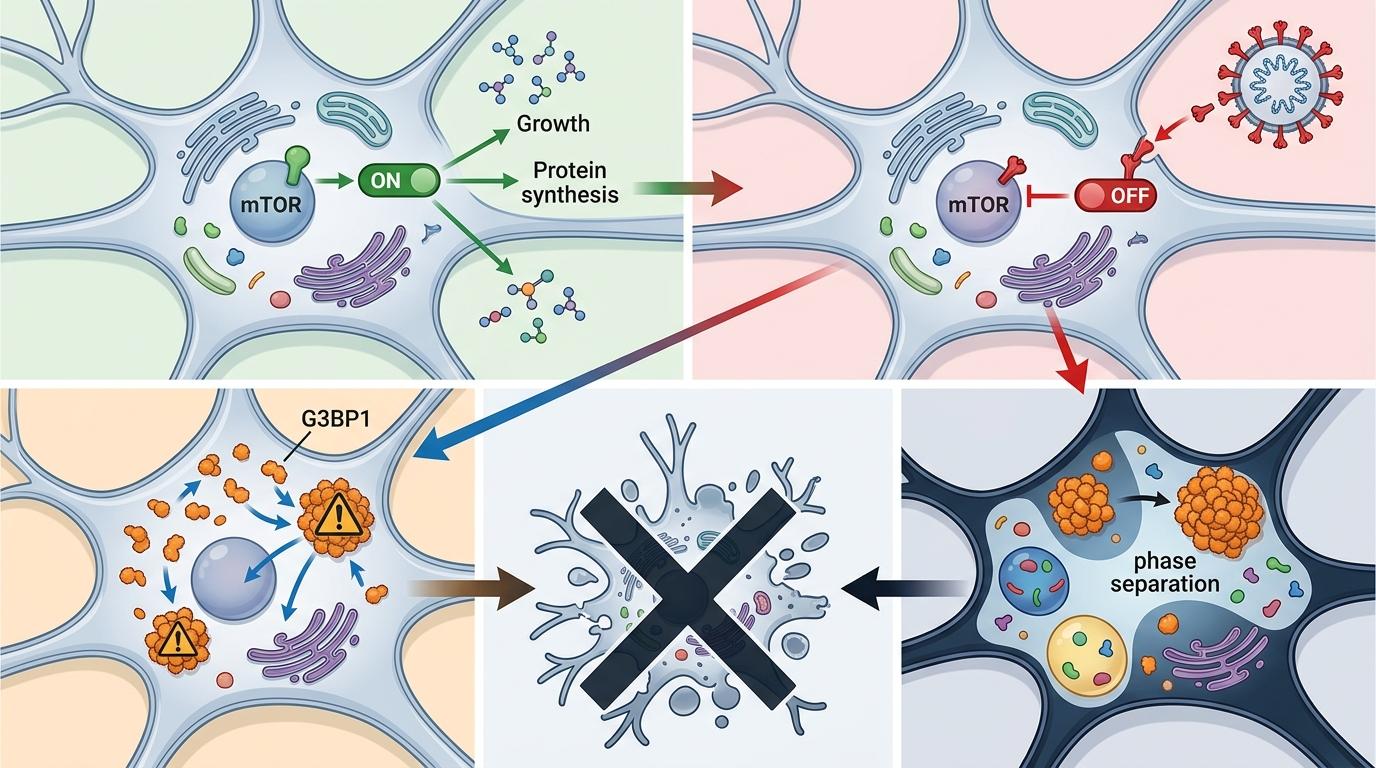
过去临床治疗新冠相关听力损失,一直沿用突发性耳聋的方案——用糖皮质激素抗炎。但根据这项研究,这种方法可能打错了靶子。
因为新冠导致听力损失的核心路径,是病毒直接对神经元的分子级破坏,和炎症风暴无关。研究者做了一组对照实验:当他们单独在细胞中过表达新冠刺突蛋白时,同样会出现mTOR通路抑制、应激颗粒异常聚集和细胞凋亡,全程没有任何炎症因子参与。这意味着,靠抗炎来治疗这类听力损失,就像用灭火器去修短路的电线——方向完全不对。
更值得警惕的是,4种毒株都能触发这条通路,且原始株和Delta株的损伤更严重。这说明无论病毒怎么变异,只要刺突蛋白的结构没发生根本性改变,就可能继续威胁内耳神经元。而目前的疫苗主要针对病毒的感染性,还无法直接阻断这种细胞内的分子损伤。
这项研究虽然找到了核心机制,但距离临床应用还有几道关卡。首先,人类内耳的结构比小鼠更复杂,病毒是否真的能通过同样的路径感染人类螺旋神经节神经元,还需要更多临床样本验证——毕竟人类内耳组织极难获取,目前的证据主要来自小鼠模型和干细胞类器官。
其次,针对mTOR通路或应激颗粒的靶向药物,还需要解决特异性问题。mTOR通路是细胞的核心通路,直接抑制它可能会影响其他正常细胞的功能;而如何精准打散异常的应激颗粒,同时不破坏细胞正常的应激反应,也是个待解的难题。
另外,疫苗相关的听力损失风险也需要更严谨的评估。目前的数据显示,疫苗相关听力损失发生率约为1.26例/10万剂次,远低于感染新冠后的风险,但仍需长期监测,明确其是否也和这条分子通路有关。
当我们终于把新冠的威胁从肺部拓展到耳朵,从炎症风暴深入到细胞内的分子开关,才发现这场病毒带来的健康影响,比我们想象的更隐秘、更持久。那些感染后突然听不到高频声音的年轻人,那些被耳鸣纠缠的长新冠患者,他们的痛苦终于有了科学的解释。
病毒不会只攻击我们最显眼的器官,它总能找到身体里最脆弱的「暗门」。这场关于耳朵的研究,不仅为听力损失的治疗点亮了新方向,也提醒我们:面对病毒,我们需要的不只是对抗感染的疫苗,更需要深入细胞内部的「分子盾牌」。
看不见的损伤,才是最需要警惕的。