
3 个月前

3 个月前
在现代医学的殿堂里,CAR-T等T细胞免疫疗法无疑是皇冠上最耀眼的明珠之一。它将患者体内的免疫T细胞改造成“生物导弹”,精准猎杀癌细胞,为许多绝望的血液肿瘤患者带来了生命的奇迹。然而,这场胜利是“昂贵”的。每一剂高达百万的费用、长达数周的“私人定制”生产周期、以及战斗中T细胞自身的疲惫与耗竭,都为这项革命性疗法筑起了一道高墙,让普通患者望而却步。
我们身体里最精锐的免疫部队——T细胞,终究是血肉之躯。它们在与癌细胞的殊死搏斗中会力竭、数量会衰减。如何为这场生命保卫战提供一支永不疲惫、源源不断的“超级军队”?这不仅是临床医生面临的难题,更是全球科学家们竞相破解的密码。直到2026年1月16日,一束光从北京大学的实验室里射出,似乎照亮了答案。
这一天,北京大学邓宏魁教授团队在国际顶尖期刊《Cell Research》上发表了一项颠覆性研究。他们宣布,仅用一套“化学鸡尾酒”配方,就成功将已经终末分化、身经百战的人类T细胞“一键重置”,逆转为具有无限潜能的多能干细胞(hT-CiPS细胞)。
这不啻于现代生物学的“炼金术”。研究显示,这种新方法的效率惊人,每孔实验中都能产生数百个干细胞集落,远超以往依赖基因编辑的传统方法。更关键的是,这些由T细胞“返老还童”而来的干细胞,完整地保留了其前身——T细胞的“记忆”:那个名为T细胞受体(TCR)的、独一无二的“敌人识别码”。这意味着,当这些干细胞被重新分化为T细胞时,它们将是一支崭新、年轻、且目标明确的免疫大军,其识别敌人的精准度高达99.8%。
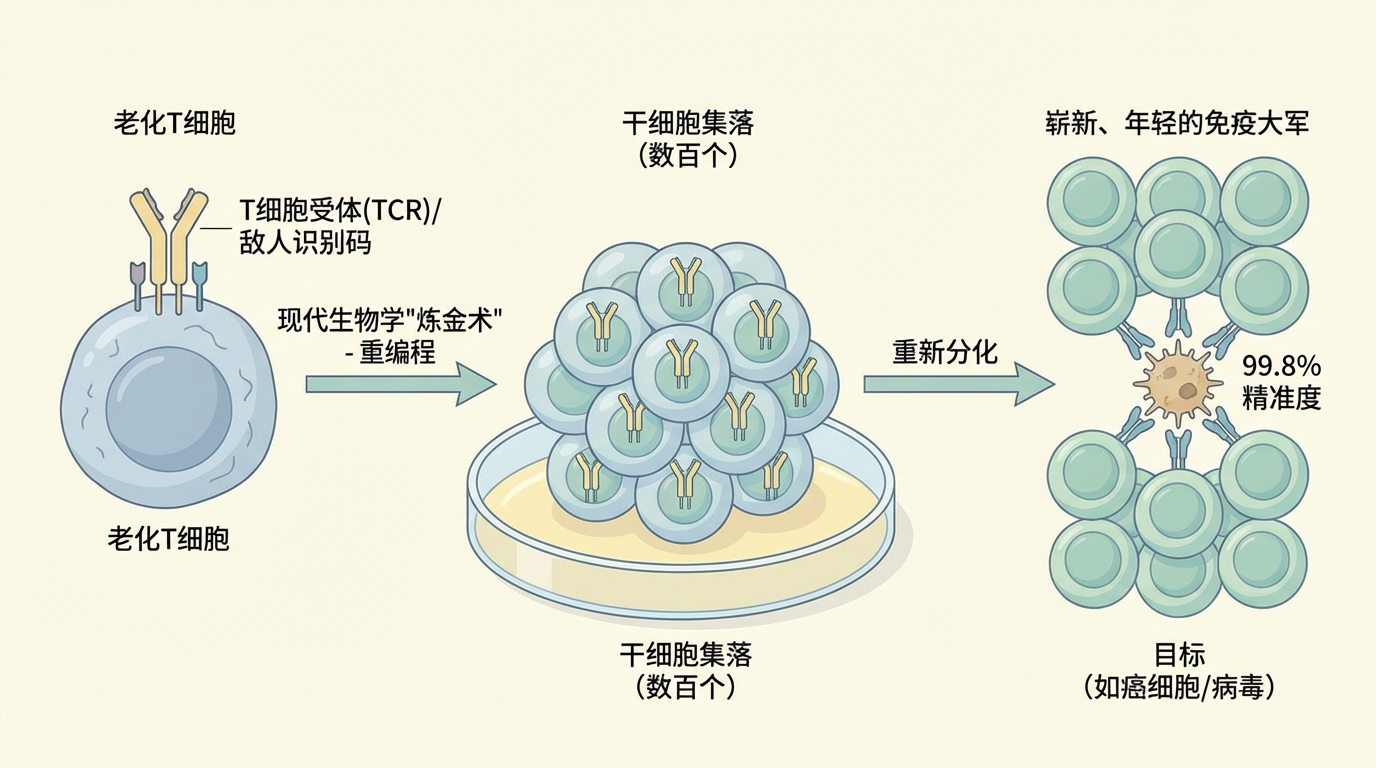
这项由邓宏魁团队开创的化学平台,为“现货型”(off-the-shelf)T细胞的工业化规模生产铺平了道路,预示着免疫疗法和再生医学的一个全新时代的到来。
要理解这一突破的意义,我们需要将时钟拨回到2006年。那一年,日本科学家山中伸弥通过植入四种特定的转录因子(“山中因子”),成功将体细胞诱导为多能干细胞(iPSC),一举摘得诺贝尔奖。这把“基因手术刀”打开了细胞重编程的大门,但病毒载体带来的基因整合风险,如同一柄悬在临床应用之上的达摩克利斯之剑。
邓宏魁,这位长期深耕于干细胞领域的中国科学家,则选择了另一条更具挑战也可能更安全的道路——化学重编程。他坚信,生命的本质是化学过程,那么操控细胞命运的钥匙,也一定隐藏在小分子化合物的无穷组合之中。这个信念引领他的团队走过了十余年的探索之路:
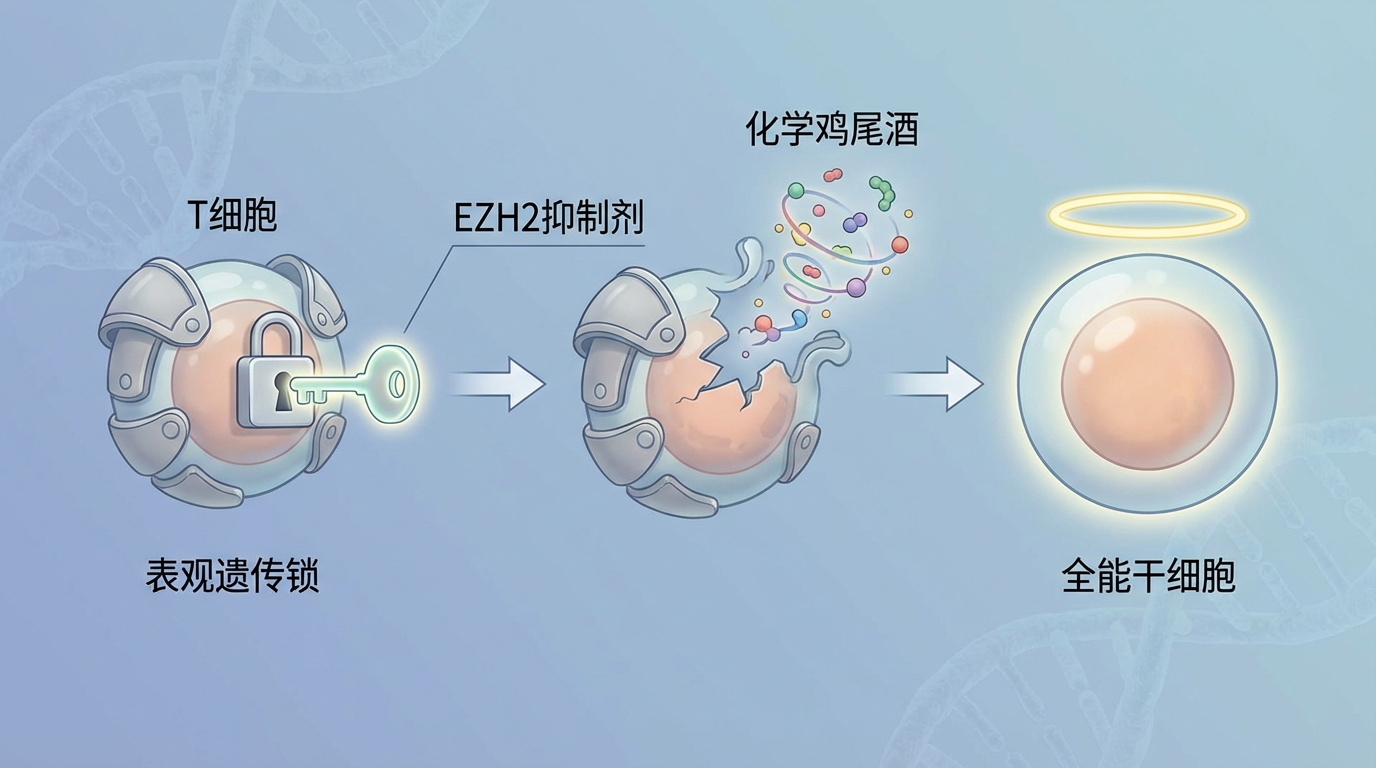
他们发现,T细胞的身份被一套强大的表观遗传“锁”牢牢固定。而解开这把锁的关键,是一种名为EZH2的组蛋白甲基转移酶抑制剂。正是这个小分子,像一把钥匙,撬开了T细胞坚固的身份壁垒,让后续的化学“鸡尾酒”得以发挥作用,引导细胞逆转时光,重返生命最初的全能状态。
邓宏魁团队的突破,其核心价值在于将T细胞疗法从一种昂贵的“手工作坊式”服务,推向了“工业化流水线”生产的黎明。
技术角度:更安全、更高效、更多样
经济角度:从“天价”到“平价”的可能 目前,CAR-T疗法之所以昂贵,很大程度上源于其高度个体化的制备流程。而“现货型”T细胞的出现,将彻底改变这一格局。通过工业化量产,细胞疗法的成本有望大幅降低,从少数人的“奢侈品”,变为多数患者可及的常规治疗选项。
当然,任何一项实验室的重大突破,距离真正应用于临床都还有漫长的道路要走。hT-CiPS细胞的长期安全性、基因组稳定性、以及在人体内的真实表现,都需要经过严格的临床试验来验证。邓宏魁团队也已明确表示,计划于2027年启动相关的I期临床试验。
同时,这项技术也引发了更深层次的思考。当我们能够用化学小分子如此精准、高效地“擦除”和“重写”细胞的身份时,我们究竟掌握了一种怎样的力量?它不仅将重塑癌症治疗,也将在器官再生、抗衰老、自身免疫性疾病治疗等领域掀起波澜。
从约翰·格登的蛙卵核移植,到山中伸弥的“基因魔法”,再到邓宏魁的“化学炼金术”,人类在理解和操控细胞命运的道路上步履不停。这一次,化学重编程T细胞的成功,不仅为无数患者带来了新的希望,更让我们瞥见了那个细胞命运可被精准编辑的未来——一个再生医学与免疫疗法真正实现工业化、普惠化的新纪元。
点击充电,成为大圆镜下一个视频选题!