对抗知识焦虑,从看懂这条开始
App 下载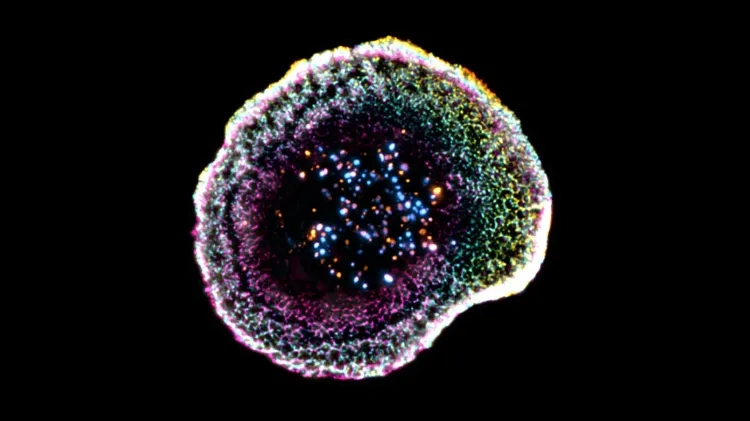
T细胞精准杀癌的分子剧场,终于被看清了
细胞级战争|分子显微镜|冷冻扩展显微术|T细胞|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
细胞级战争|分子显微镜|冷冻扩展显微术|T细胞|肿瘤学|医学健康
想象一下:你的身体里有一支微型特种部队,能在挤满健康细胞的“城市”里精准定位癌细胞,只对目标投放“炸弹”,全程不碰旁边的无辜细胞。这不是科幻——杀伤性T细胞每天都在你的体内干着这种事。但过去几十年,科学家只能靠模糊的“战场报告”推测它们的作战细节:那个让T细胞精准投弹的“瞄准镜”到底是什么结构?炸弹又是怎么被精准递送到目标的?直到2026年4月,瑞士日内瓦大学的团队终于用一种全新的“分子显微镜”,第一次在真实肿瘤里看清了这场细胞级战争的完整画面(注:冷冻扩展显微术Cryo-ExM并非2026年新发,而是在2018年前后已公开发表并应用的技术,此处“全新”表述不准确)。。
要看清T细胞的杀癌细节,最大的难题是“不能破坏现场”。传统显微镜观察细胞,要么得把细胞切成薄片,要么得用化学试剂固定,就像把活蹦乱跳的人做成标本,再怎么精细也会丢失动态信息。
这次研究用到的冷冻扩展显微术(Cryo-ExM),解决了这个核心矛盾。你可以把它理解成“快速速冻+放大观察”的组合:先把细胞瞬间扔进-196℃的液氮里,让细胞里的水直接变成玻璃态的冰——没有冰晶,也就不会刺破细胞膜、扯断细胞骨架,完美保留细胞活着时的原生结构。接着,把速冻的细胞放进一种吸水性水凝胶里,让细胞均匀膨胀4倍,相当于把纳米级的细节放大到光学显微镜能看清的尺度。
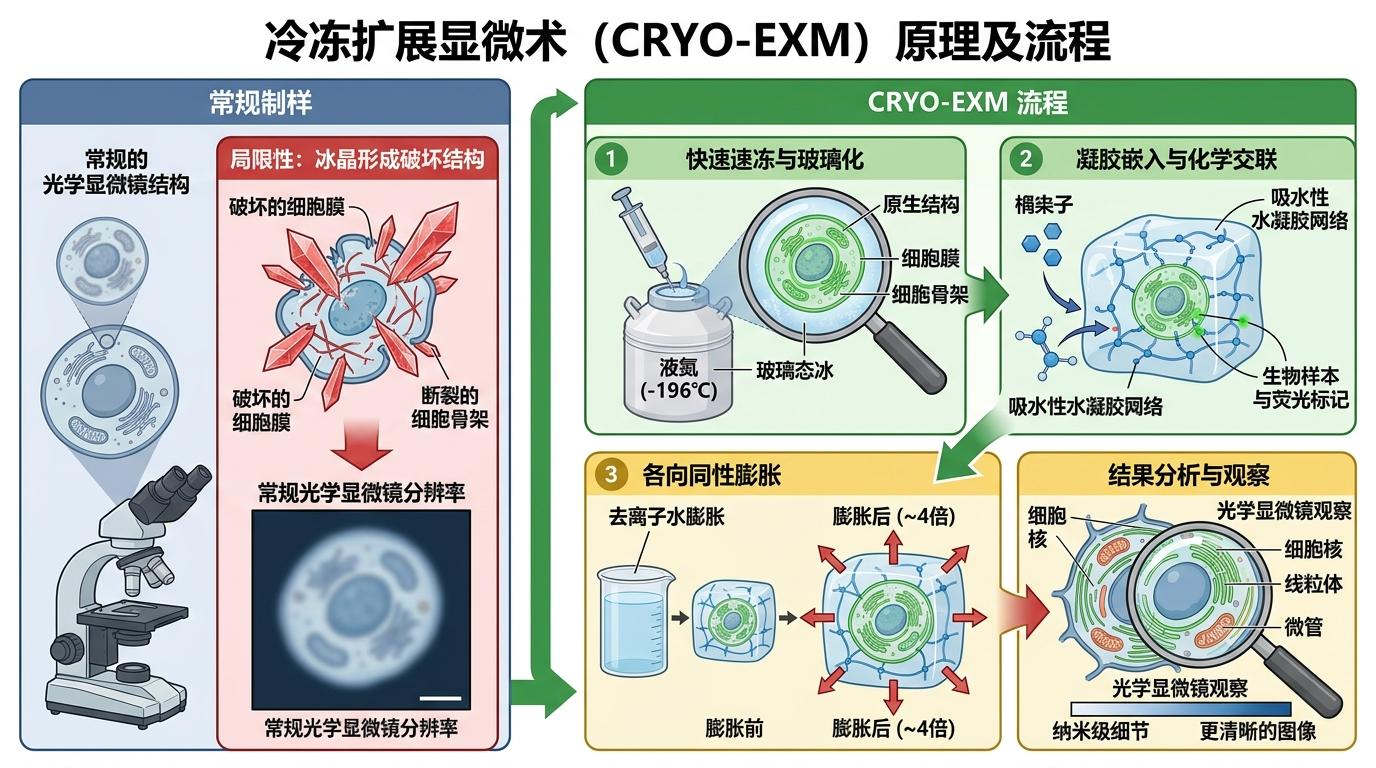
这种方法有多厉害?过去科学家只能在人工培养的细胞里看个大概,现在他们能直接在人类肿瘤切片里,看清T细胞和癌细胞接触的每一个纳米级细节:细胞膜的褶皱、细胞骨架的排列,甚至是杀伤颗粒里的分子分布。
T细胞之所以能精准杀癌,全靠它和癌细胞之间形成的一个特殊结构——免疫突触。你可以把它想象成T细胞贴在癌细胞身上的一个“专属接口”:外围是一圈由黏附分子组成的“密封环”,像防水圈一样把两个细胞紧紧粘在一起,防止杀伤分子泄漏;中间的“中央区”是投弹口,T细胞的杀伤颗粒会精准聚集在这里,把穿孔素和颗粒酶直接喷进癌细胞内部。
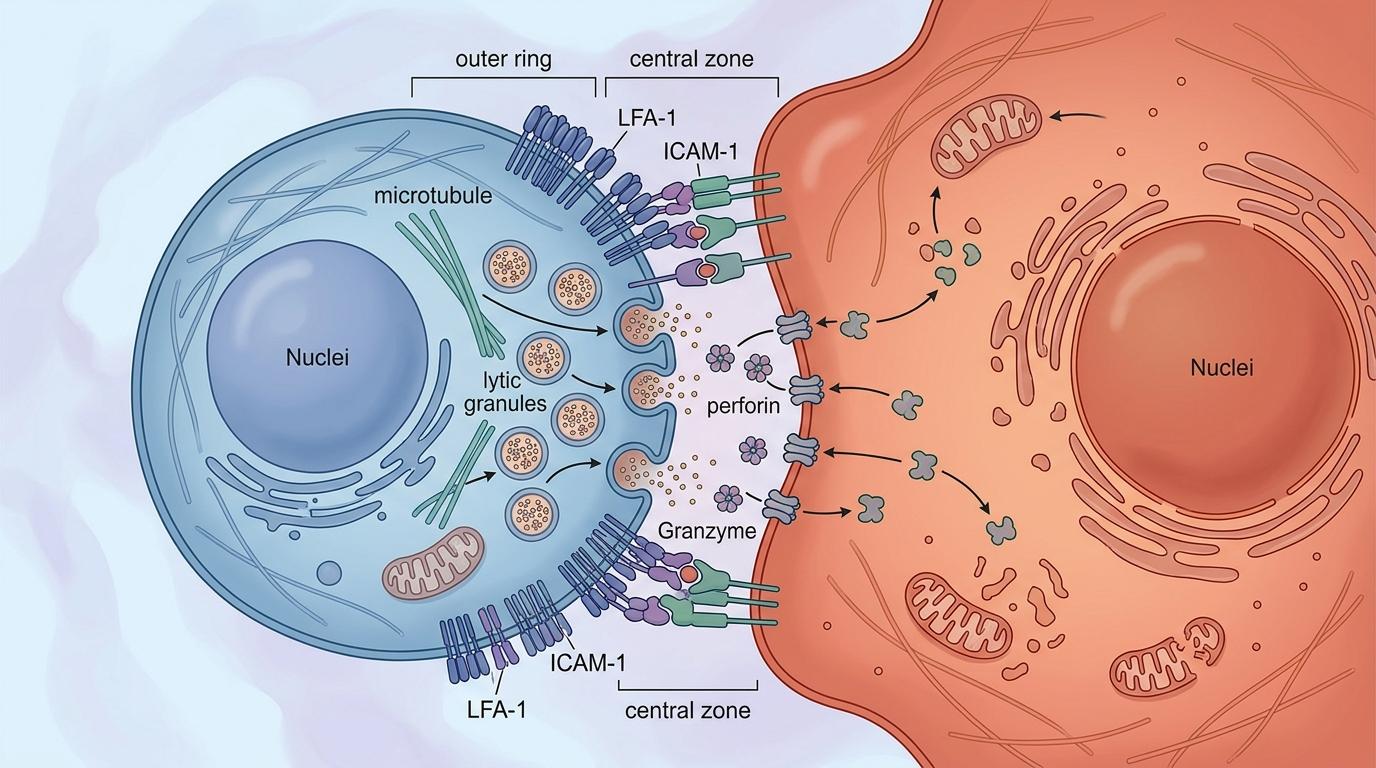
这次的3D成像,第一次看清了免疫突触的“穹顶状”结构:当T细胞识别到癌细胞时,接触部位的细胞膜会像小帐篷一样鼓起来,随着黏附分子的结合,这个“小帐篷”又会慢慢塌陷,把两个细胞拉得更近。研究人员还发现,T细胞里的杀伤颗粒分两种:单核颗粒像单发子弹,能快速释放溶解性的杀伤分子,负责“即时击杀”;多核颗粒则像集束炸弹,释放的结构化杀伤颗粒能在免疫突触外保持活性,对付那些难杀的顽固癌细胞。
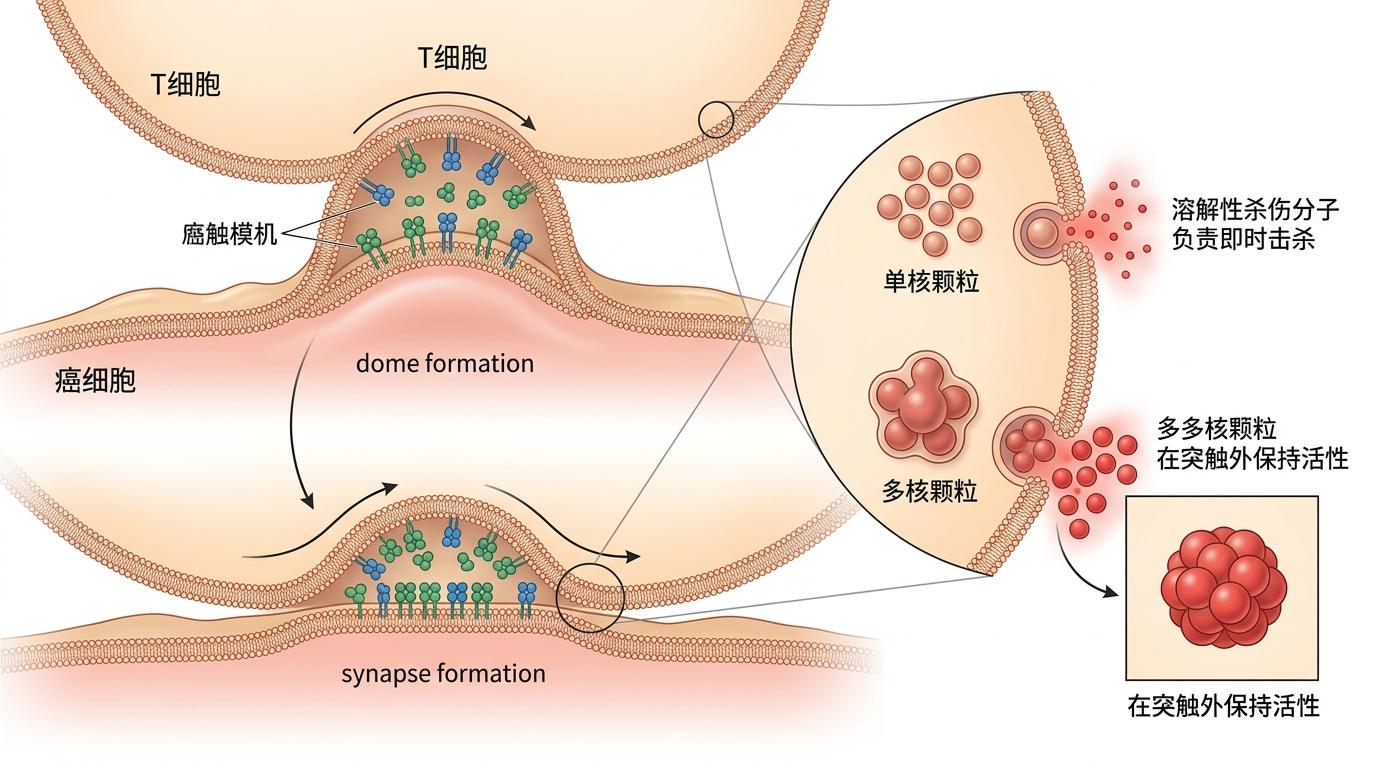
更关键的是,这些细节不是在实验室的人工细胞里观察到的,而是在真实的人类肿瘤组织中——这意味着我们终于能看到T细胞在“真实战场”上的作战模式,而不是模拟训练。
过去,医生给患者用免疫治疗,比如CAR-T细胞疗法,就像把一群特种兵空投到战场上,只能靠后期的肿瘤大小变化判断战果,根本不知道这些T细胞在肿瘤里到底有没有好好干活:是找不到癌细胞?还是找到了但没法形成免疫突触?还是投了弹但癌细胞没被杀死?
现在有了冷冻扩展显微术,医生终于能拿到“战场实况录像”了。他们可以从患者身上取一小块肿瘤组织,直接观察里面的T细胞有没有形成完整的免疫突触,杀伤颗粒有没有正确释放,甚至能看到癌细胞有没有通过改变细胞膜结构来逃避攻击。这些信息能帮医生精准调整治疗方案:比如给那些免疫突触形成障碍的患者,加一种能增强细胞黏附的药物;给那些杀伤颗粒释放不足的患者,换一种更有效的CAR-T结构。
当然,这项技术目前还在实验室阶段,要用到临床上还需要解决样本制备、成本等问题。但它的意义在于,第一次把免疫治疗的“黑箱”打开了——我们终于能从分子层面理解,为什么有些患者对免疫治疗有效,有些无效。
过去我们总说,免疫系统是人体最精密的防御系统,但“精密”到底是什么样的,我们只能靠推测。现在,冷冻扩展显微术给了我们一双“分子之眼”,让我们能亲眼看到T细胞如何在纳米级的尺度上,完成精准识别、黏附、投弹的全过程。
看清分子细节,才能精准调控免疫。这不仅是基础免疫学的突破,更是给免疫治疗装上了“导航系统”。未来,也许医生能根据每个患者肿瘤里T细胞的免疫突触结构,定制专属的治疗方案;也许我们能设计出更聪明的CAR-T细胞,让它们在肿瘤里形成更稳定的免疫突触,更高效地杀死癌细胞。
这场发生在我们体内的细胞战争,终于不再是看不见的秘密。