对抗知识焦虑,从看懂这条开始
App 下载
潜伏95%人体内的病毒,终于遇到对手
移植后淋巴增殖性疾病|鼻咽癌|B淋巴细胞|人源化单克隆抗体|EB病毒|感染性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
移植后淋巴增殖性疾病|鼻咽癌|B淋巴细胞|人源化单克隆抗体|EB病毒|感染性疾病|医学健康
你大概率是它的携带者——EB病毒,一种全球95%成年人都感染过的γ-疱疹病毒。它可能在你小时候通过一次共用餐具、一个亲吻悄悄潜入,然后躲进免疫细胞里潜伏几十年,偶尔引发传染性单核细胞增多症,更可能在你免疫力低下时,诱发鼻咽癌、淋巴瘤甚至移植后淋巴增殖性疾病。过去几十年,人类对它几乎束手无策:疫苗只能降低轻症风险,抗病毒药对潜伏的病毒无效,免疫抑制的移植患者更是随时面临它的致命反扑。直到最近,一组人源化单克隆抗体,终于在这场持续了半个世纪的攻防战里,撕开了一道缺口。
EBV的狡猾,在于它能精准撬开两种人类细胞的大门:B淋巴细胞和上皮细胞。这两把“锁”的钥匙,是病毒表面的gp350和gp42蛋白。 你可以把gp350想象成病毒的“敲门砖”——它先和B细胞表面的CD21受体结合,让病毒牢牢贴在细胞上;而gp42则是“开门的密码”,它会对接B细胞表面的HLA-II分子,触发病毒包膜和细胞膜的融合,让病毒的遗传物质趁机溜进去。更棘手的是,gp42还能切换模式:当它和病毒表面的gH/gL复合物结合时,会反过来抑制病毒感染上皮细胞,帮病毒实现“精准靶向”。
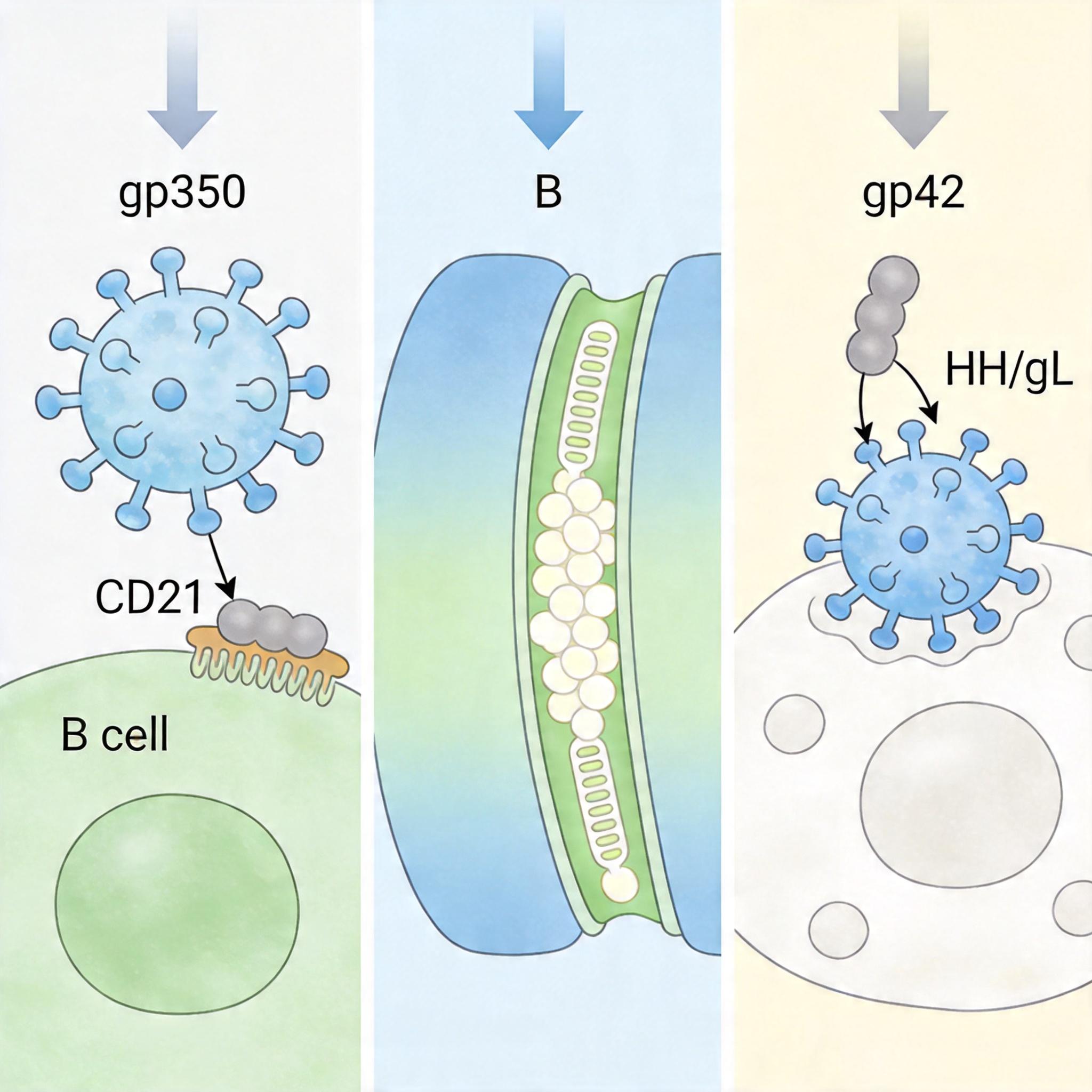
过去的疫苗只盯着gp350,就像只抢了敲门砖却没夺下密码,病毒还是能找到其他方式开门。而这次的研究,直接瞄准了gp42这个核心密码。科学家从EBV感染者体内筛选出的单克隆抗体6G7,能精准结合gp42的C端区域,阻断它和HLA-II分子的对接——相当于把病毒的密码锁给焊死了。 在人源化小鼠实验里,注射了6G7的小鼠完全没出现病毒血症,对照组却有83%的小鼠死于EBV诱发的淋巴瘤。
这组抗体的出现,给移植患者等高危人群带来了希望,但要真正走进临床,还有三道坎要跨。 第一道坎是病毒的逃逸能力。EBV的基因组会不断突变,要是它改一改gp42的结构,让抗体认不出来,之前的努力就白费了。研究团队发现,6G7识别的是gp42上一个高度保守的区域——相当于锁芯最核心的部分,病毒很难轻易改动,但长期来看,还是得联合多个靶点的抗体,比如同时瞄准gp350和gH/gL,才能不给病毒留空子。 第二道坎是免疫耐受。EBV在人体内潜伏几十年,免疫系统早就对它产生了部分耐受,怎么让抗体既能有效识别病毒,又不会被免疫系统当成“自己人”忽略?这次的人源化抗体解决了这个问题——它们完全由人类抗体基因编码,不会引发人体的排异反应,还能绕过病毒的免疫逃逸机制。 第三道坎是成本和可及性。单克隆抗体的生产工艺复杂,价格昂贵,要是真的用于移植患者的常规预防,普通家庭根本负担不起。目前研究团队已经在推进健康成人的安全性试验,未来还得优化生产工艺,降低成本,才能让更多人受益。 更值得警惕的是,EBV不仅会诱发癌症,还和多发性硬化症等自身免疫疾病有关。这次的抗体只解决了病毒入侵的问题,对于已经潜伏在细胞里的病毒,以及病毒引发的免疫紊乱,还没有有效的应对办法。
除了抗体治疗,科学家还在基于gp42等靶点开发新一代疫苗。和传统的gp350疫苗不同,新一代疫苗采用了纳米颗粒技术——把gp42、gH/gL等多个病毒蛋白组装成一个纳米颗粒,就像把几把病毒的钥匙挂在一个盾牌上,让免疫系统能同时识别多个靶点。

在小鼠实验里,这种纳米颗粒疫苗诱导产生的中和抗体滴度,比传统的gp350单体疫苗高了几十倍,还能同时阻断EBV感染B细胞和上皮细胞。更重要的是,它能激活细胞免疫,让T细胞也参与到抗病毒的战斗中,而不仅仅依靠抗体。
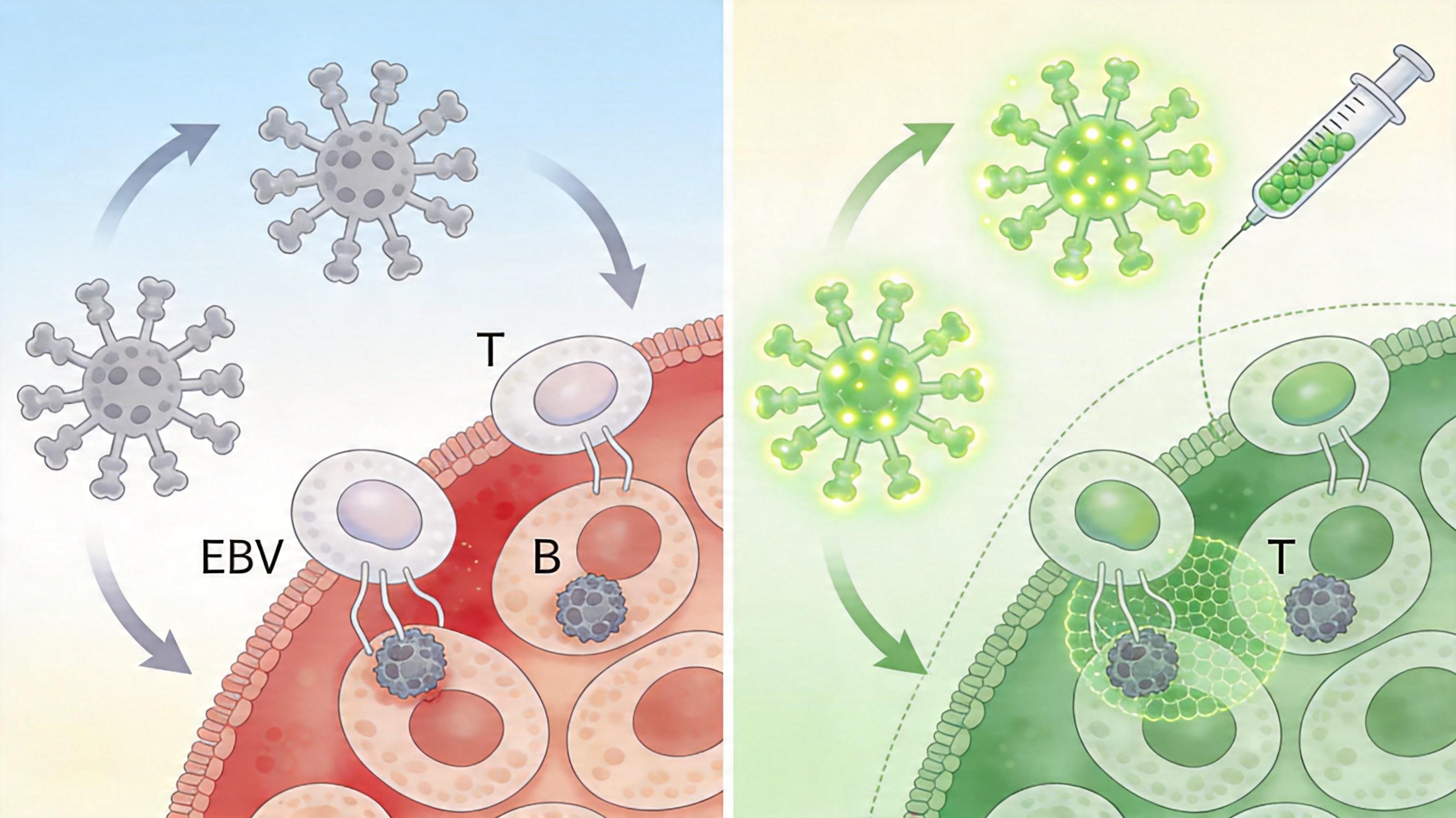
不过,疫苗的研发还面临一个难题:EBV只感染人类,没有理想的动物模型来模拟人类的感染过程。目前科学家只能用人源化小鼠或者感染EBV同源病毒的猕猴来做试验,结果的参考性有限。要验证疫苗的真实效果,还得在人体临床试验里慢慢摸索。
对于EBV这种潜伏在全球大多数人身体里的“沉默杀手”,人类的认知还只是冰山一角。这次的抗体突破,不是终点,而是一个新的起点——它让我们终于摸到了病毒的命门,也让我们意识到,对付这种狡猾的病毒,不能只靠单一的手段,得把抗体、疫苗、细胞治疗甚至小分子药物结合起来,打一场“组合拳”。 病毒潜伏半生,人类终觅破局之道。 未来,也许我们能像控制乙肝一样,把EBV的危害降到最低;也许我们能在孩子小时候就接种疫苗,让他们一辈子都不受EBV的威胁。但在此之前,我们还要走很长的路——毕竟,和病毒的战争,从来都不是一蹴而就的。