对抗知识焦虑,从看懂这条开始
App 下载
果蝇失眠的秘密:自闭症基因如何搅乱睡眠
自闭症相关睡眠障碍|NLGN3基因|FOXP基因变异|果蝇模型|神经生物学|睡眠医学|生命科学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
自闭症相关睡眠障碍|NLGN3基因|FOXP基因变异|果蝇模型|神经生物学|睡眠医学|生命科学|医学健康
深夜11点的实验室里,一排培养箱发出均匀的嗡鸣。透过玻璃门,能看到几百只果蝇在试管里爬动——它们本该是睡得最沉的时刻。这些果蝇体内,被科学家嵌入了自闭症患者常见的FOXP基因变异。结果是,它们的睡眠碎成了渣:每小时要醒三四次,总睡眠时间比正常果蝇少了近40%,连白天的小憩都变得断断续续。更奇怪的是,它们的生物钟也乱了,分不清白天黑夜。这不是果蝇的特例:另一组携带NLGN3基因变异的果蝇,也出现了完全不同的睡眠紊乱。这些小小的昆虫,正在帮人类揭开一个藏了几十年的秘密:自闭症和睡眠障碍,到底是不是同一条基因藤上结的两个苦果?
FOXP家族基因曾因和人类语言能力相关而闻名,直到近年才发现,它们还是调控睡眠的关键开关。你可以把FOXP蛋白想象成一个办公室主任,负责给一群和睡眠、生物钟相关的基因“派活”——什么时候让大脑产生睡意,什么时候提醒身体该起床,都得听它调度。
但真实的机制比这更精确:FOXP蛋白是一种转录因子,能直接结合到其他基因的启动子区域,像开关一样控制它们的表达量。当FOXP基因发生变异,这个“主任”就会乱发指令:要么让促睡眠的基因罢工,要么让维持清醒的基因过度活跃。
在果蝇实验里,携带FOXP变异的个体不仅睡眠碎片化,连体内的生物钟基因表达都出现了紊乱——就像钟表的齿轮被掰歪了,走得忽快忽慢。研究团队还发现,这种影响不是全身性的,而是精准地瞄准了大脑里调控昼夜节律的神经元群。
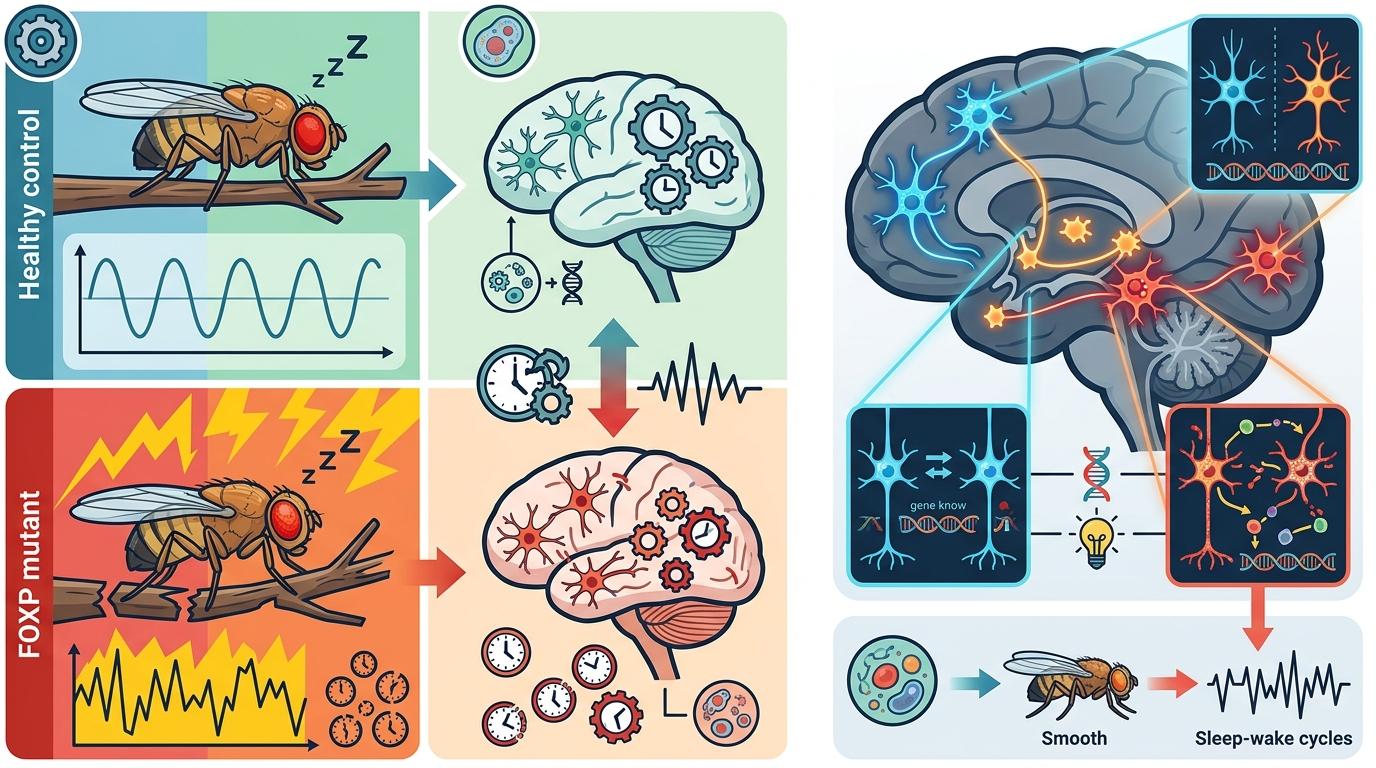
更关键的是,人类和果蝇的FOXP基因序列相似度超过70%。这意味着,果蝇身上发生的睡眠紊乱,很可能就是自闭症患者夜夜难眠的微观缩影。
如果说FOXP是睡眠的“总调度”,那NLGN3就是突触的“装修工”。这种位于神经细胞表面的黏附分子,负责把两个神经元粘在一起,搭建起传递信号的突触——你可以把它想象成连接两个房间的门,门的好坏直接决定了信号能不能顺畅传递。
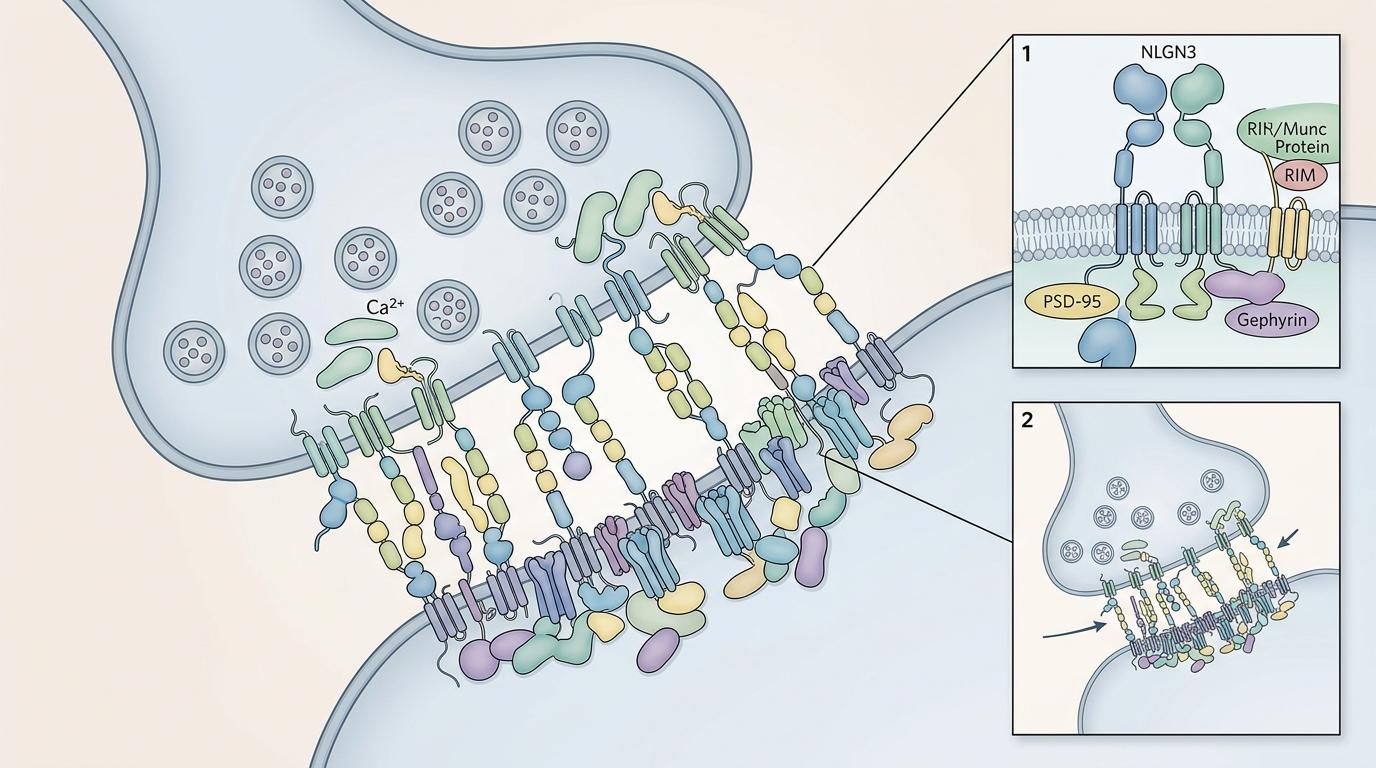
但真实的机制比这更复杂:NLGN3基因的不同变异,会给突触带来完全不同的命运。科学家在果蝇身上测试了三种常见的NLGN3变异,结果让人惊讶:
这些差异直接反映在睡眠上:有的果蝇睡得少但沉,有的果蝇睡得多但频繁惊醒,还有的干脆昼夜颠倒。这种分子层面的多样性,正好解释了为什么自闭症患者的睡眠障碍五花八门——有的入睡困难,有的夜醒频繁,有的白天嗜睡。
值得注意的是,NLGN3变异不仅影响睡眠,还会直接干扰社交行为。在果蝇模型里,缺失NLGN3的个体,会主动和同类保持更远的距离,就像自闭症患者常表现出的社交回避。这也印证了一个核心假说:睡眠障碍不是自闭症的“附加症状”,而是和核心症状共享同一条神经通路的结果。
实验室里的果蝇实验,最终要落回真实世界的困境。在中国,每100个自闭症儿童里,就有50到80个被睡眠问题困扰。他们的睡眠障碍不是“睡不着”这么简单:有的要熬到凌晨两三点才能入睡,有的每晚要醒七八次,有的白天睡十几个小时,晚上却精神百倍。
这些孩子的家长,几乎都过着“昼夜颠倒”的生活。一位母亲在接受调查时说,她已经三年没睡过超过4小时的整觉,白天要陪孩子做康复训练,晚上要起来安抚频繁夜醒的孩子,头发掉了一半,血压也高了。更让人揪心的是,睡眠障碍会反过来加重自闭症的核心症状:睡不好的孩子,会变得更易怒、更孤僻,康复训练的效果也会大打折扣。
目前的干预手段还很有限:行为疗法需要家长付出极大的精力,褪黑素等药物只能缓解部分症状,且长期安全性还在争议中。而果蝇实验带来的最大希望,就是找到精准的治疗靶点——比如针对FOXP变异的生物钟调节剂,或者针对不同NLGN3变异的突触修复药物。
不过,也有一个容易被忽略的事实:不是所有自闭症相关基因都会导致睡眠障碍。科学家在研究中发现,有些基因变异只会影响社交行为,不会干扰睡眠;有些则正好相反。这说明,自闭症和睡眠障碍的关系,比想象中更复杂,不是简单的因果链条,而是一张相互交织的网络。
当我们盯着实验室里的果蝇,看它们在试管里无精打采地爬动时,其实是在凝视成千上万自闭症家庭的夜晚。那些被打乱的睡眠,那些熬红的眼睛,那些无声的疲惫,背后都藏着基因的密码。
从果蝇的睡眠紊乱,到人类的神经回路异常,科学家正在一步步拆解这张复杂的网络。未来的某一天,也许我们能根据每个孩子的基因变异,开出精准的药方:让FOXP变异的孩子重新拥有规律的生物钟,让NLGN3变异的孩子突触恢复正常的连接。
基因藏着因,睡眠映着果。 这不仅是关于睡眠的研究,更是关于如何让自闭症家庭重新拥有安稳夜晚的希望。毕竟,对这些家庭来说,好好睡一觉,就是最珍贵的治愈。