对抗知识焦虑,从看懂这条开始
App 下载
阿尔茨海默病新药:延缓4个月,值30万吗?
药物经济性|Cochrane综述|认知衰退|淀粉样蛋白|阿尔茨海默病新药|神经退行性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
药物经济性|Cochrane综述|认知衰退|淀粉样蛋白|阿尔茨海默病新药|神经退行性疾病|医学健康
当72岁的张阿姨拿着阿尔茨海默病新药处方时,她和女儿算了一笔账:每两周一次静脉输注,每次耗时1小时,全年12次脑部MRI监测,加上近30万元的药费,换来的是认知衰退速度延缓4到6个月——这个时间,刚好够她多记清几次孙子的生日。这不是个例,2024年Cochrane的一项覆盖2万患者的综述,把这类曾被捧为「救命稻草」的抗淀粉样蛋白新药打回了现实:它们能清除脑内的淀粉样斑块,但对患者和家属能感知到的认知改善,「微乎其微」。为什么投入数百亿研发的新药,只换来如此尴尬的结果?
你可以把大脑想象成一个拥挤的快递站:淀粉样蛋白(Aβ)是本该被及时清运的快递包裹,当血脑屏障这个「快递通道」失灵,包裹就会在神经元门口堆成小山——这就是阿尔茨海默病标志性的「淀粉样斑块」。过去20年,这个「淀粉样蛋白假说」是学界的绝对主流,药企砸下数千亿美元,开发能「清走包裹」的抗淀粉样蛋白药物。
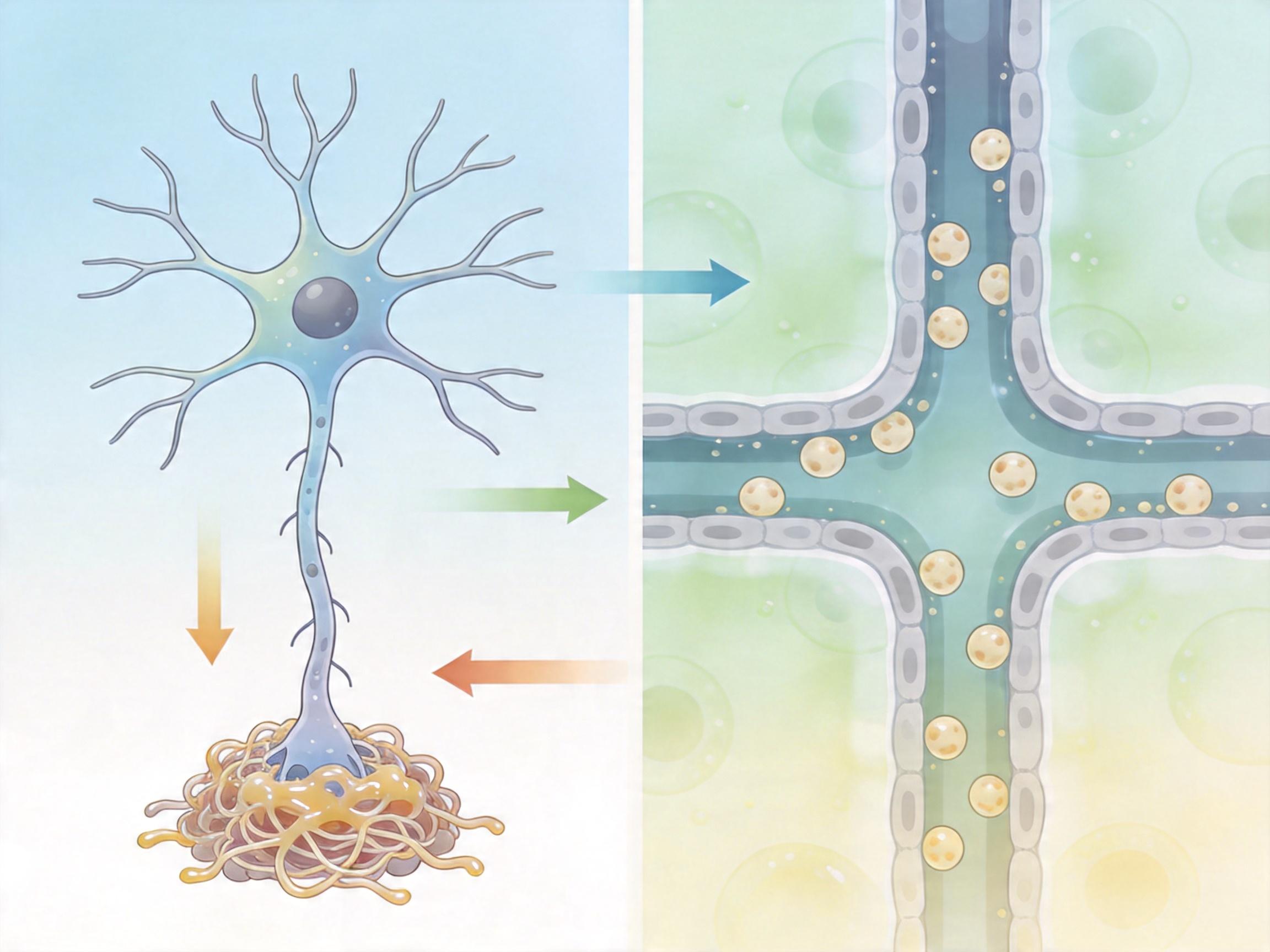
但真实的机制比这复杂得多。
这些药物的核心逻辑是:通过单克隆抗体绑定脑内的淀粉样斑块,激活小胶质细胞这个「清洁工」吞噬斑块。临床试验数据显示,它们确实能把PET影像上的斑块「洗干净」——比如lecanemab能让81%的患者斑块转阴,donanemab的清除率更高达76%。但问题在于,斑块消失了,认知衰退却只是慢了一点点:18个月的治疗,仅能让认知下降速度减缓27%到35%,换算成实际生活,就是多维持4到6个月的独立进食、认人能力。
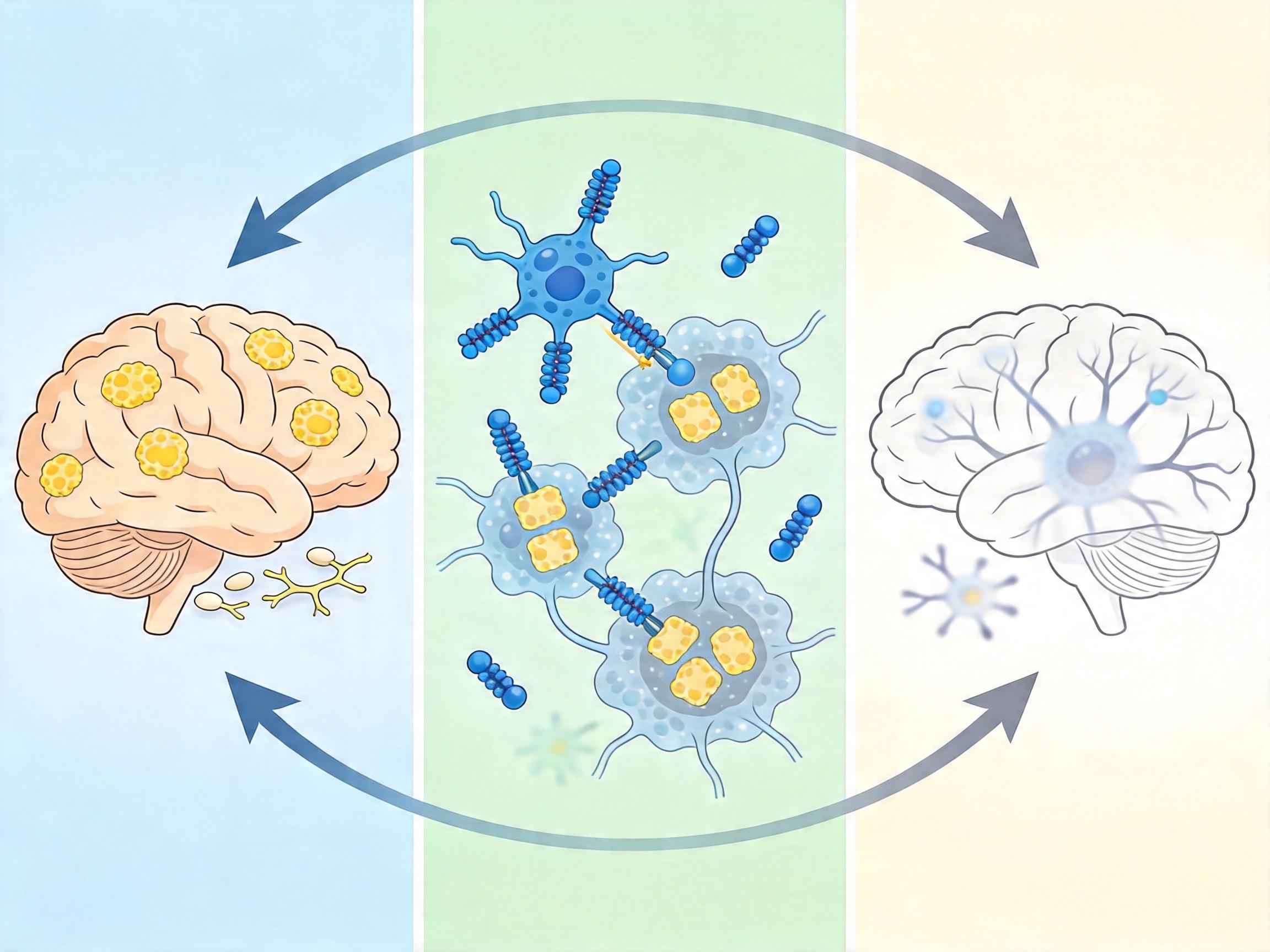
更关键的是,这种改善远没达到「临床意义阈值」——也就是患者和家属能明确感觉到的变化。用CDR-SB认知评分来衡量,患者需要至少1分的改善才能被察觉,但新药带来的平均变化只有0.45分。
新药的尴尬不止于微弱的疗效,还有无法忽视的风险和成本。
最严重的副作用是「淀粉样相关影像异常(ARIA)」——简单说就是脑部水肿或微出血。携带APOE ε4基因(晚发性阿尔茨海默病的主要风险基因)的患者,尤其是纯合子,发生ARIA的概率高达32.6%,其中约3%会出现头痛、意识混乱甚至癫痫的症状。为了监测这种风险,患者每3个月就要做一次脑部MRI,这不仅增加了治疗负担,也让本就脆弱的老人频繁奔波于医院。
成本更是一道难以跨越的坎。在美国,lecanemab年治疗费用约2.65万美元,donanemab约3.2万美元,换算成人民币超过20万。英国NICE最初拒绝将其纳入医保,理由就是「每延缓1年认知衰退,成本高达10万英镑,性价比极低」。即便药企上诉后NICE重启评估,也要求大幅降价才可能纳入公共医疗体系。
更讽刺的是,这些新药只对「轻度认知障碍或早期痴呆患者」有效——而这个阶段的患者,往往还能维持基本生活,家属的治疗意愿未必强烈;当患者发展到中重度,这些药物又完全失去了作用。
新药的争议,本质上是对「淀粉样蛋白假说」的反思:学界终于意识到,阿尔茨海默病不是单一蛋白堆积导致的,而是一场涉及神经炎症、tau蛋白缠结、血管损伤的「多重灾难」。
现在,越来越多的研究开始转向多靶点联合治疗:比如把抗淀粉样蛋白药物和抗tau药物结合,同时清除斑块和神经元内的「蛋白缠结」;或者加入抗炎药物,抑制微胶质细胞的过度激活——毕竟,过度活跃的「清洁工」也会损伤正常神经元。还有研究发现,修复血脑屏障这个「快递通道」,可能比单纯清除斑块更有效:通过激活LRP1等转运受体,让大脑自己恢复清运淀粉样蛋白的能力。
精准医疗也是新的方向。未来医生可能会根据患者的APOE基因型、脑脊液中的tau蛋白水平、甚至肠道菌群,定制个性化治疗方案——比如对APOE ε4纯合子患者,直接跳过抗淀粉样蛋白药物,选择更安全的抗炎或神经保护疗法。
2025年FDA批准的lecanemab皮下注射剂型,算是一个小进步:每周一次的皮下注射,把每次给药时间从1小时缩短到15秒,患者甚至可以在家自行注射,大大降低了治疗负担。但这只是「治标」,真正的突破,可能要等我们彻底搞清楚阿尔茨海默病的「多重致病逻辑」。
张阿姨最终还是放弃了新药,选择了每月几百元的胆碱酯酶抑制剂,和女儿一起做认知训练。她的故事,也是当下阿尔茨海默病治疗的缩影:我们终于找到了能「延缓」疾病的药物,但距离「治愈」还远得很。
慢疾需慢治,精准方有效。比起追求「突破性」的单一药物,或许更重要的是建立一套从早期筛查到个性化干预的完整体系——比如用血液生物标志物在无症状阶段就发现风险,用生活方式干预(运动、饮食、认知训练)延缓发病,用联合药物在早期阶段控制进展。毕竟,对于阿尔茨海默病患者来说,能多记清一次家人的脸,多吃一顿自己盛的饭,就是最实在的「疗效」。