对抗知识焦虑,从看懂这条开始
App 下载
沉睡的基因被唤醒,自闭症治疗迎来精准时代
自闭症患者|精准医疗|基因沉默|ASO分子工具|Angelman综合征|罕见遗传病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
自闭症患者|精准医疗|基因沉默|ASO分子工具|Angelman综合征|罕见遗传病|医学健康
布拉格的会议厅里,Allyson Berent的声音带着哽咽。她展示的视频里,一位被Angelman综合征困住30年的女性,第一次自己拿起勺子吃饭;一个沉默了6年的孩子,清晰地说出了“妈妈”。这些曾被医生判定“永远不可能”的场景,正因为一项精准医疗技术变成现实——科学家没有改写患者的DNA,只是用分子工具“唤醒”了他们体内原本就存在、却被沉默的健康基因。这不是科幻电影的片段,而是2026年国际自闭症研究大会上最触动人心的现场。为什么唤醒一个沉睡的基因,就能改变一个家庭的命运?这背后的科学,正在重新定义自闭症的治疗边界。
你可以把人体的基因想象成一本写满指令的书,而Angelman综合征患者的问题,是其中至关重要的一页——母源UBE3A基因被撕掉了。但他们体内还有另一页父源UBE3A基因,只是被一条叫UBE3A-ATS的“胶带”死死粘住,无法打开。
反义寡核苷酸(ASOs)就是专门撕胶带的工具。这是一种人工合成的短链核酸,能精准找到那条粘住基因的UBE3A-ATS,把它“粘”住失效,让被沉默的父源UBE3A基因重新“翻开”,产生维持大脑正常功能的蛋白。
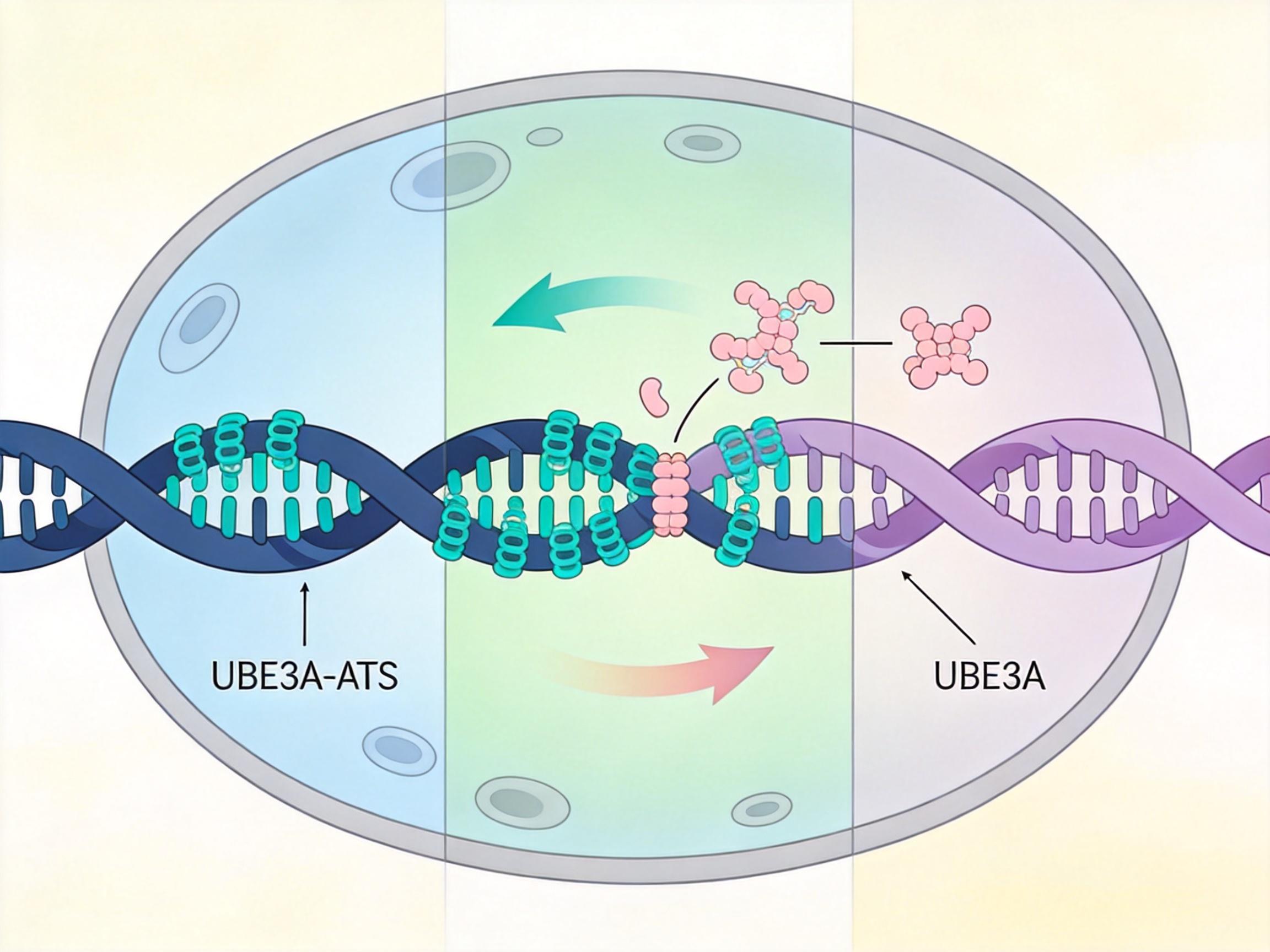
但真实的机制比这个类比更精确:ASOs通过碱基互补配对结合UBE3A-ATS,触发细胞内的降解机制清除这条干扰RNA,同时解除它对父源UBE3A基因的转录抑制。在Angelman综合征小鼠模型中,单次脑室注射ASO后,大脑皮层和海马区的UBE3A蛋白能恢复到正常水平的70%,效果持续数周;临床试验里,患者的癫痫发作频率降低、睡眠周期恢复,甚至成年患者也能获得新的认知能力。
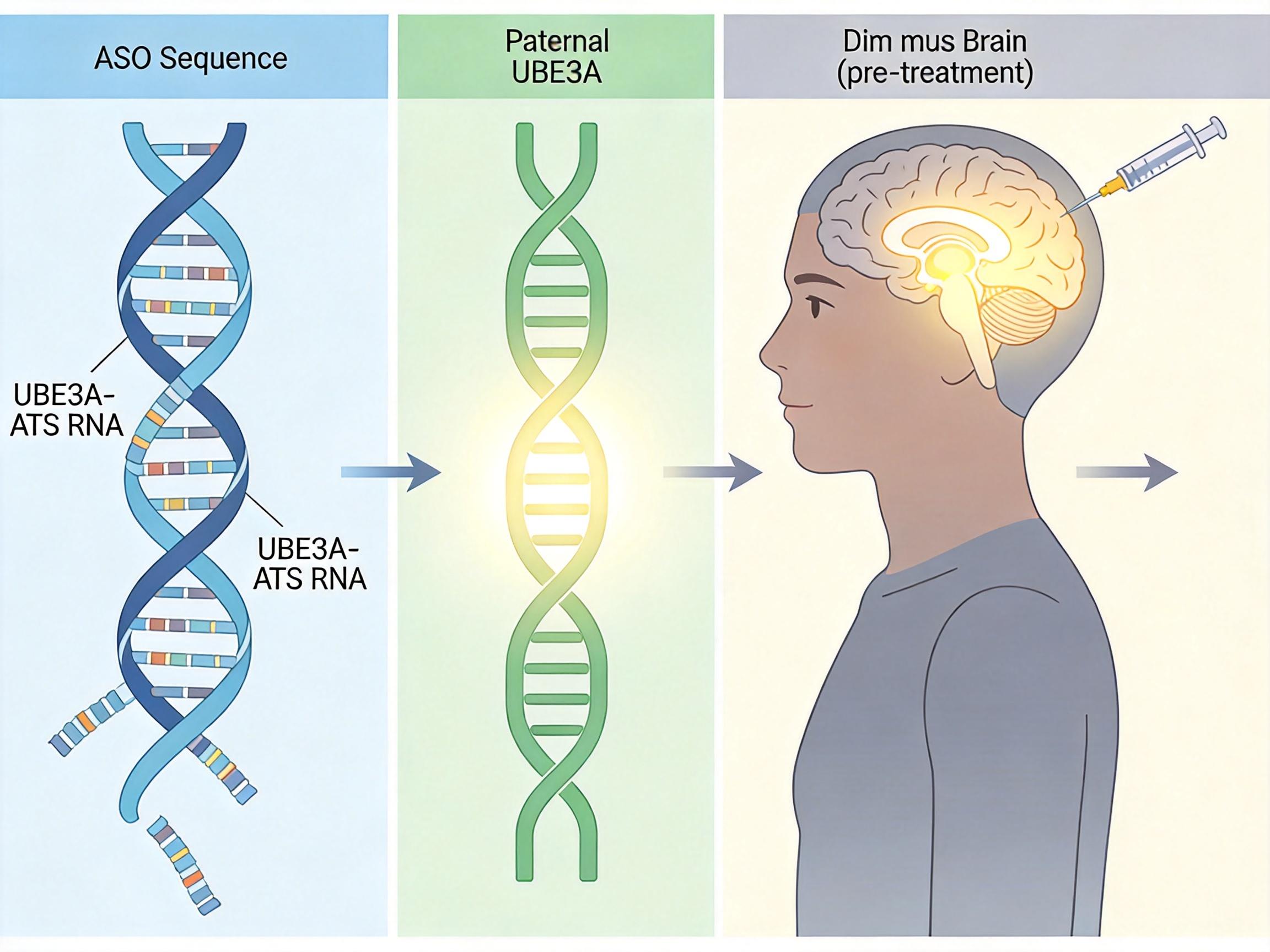
更关键的是,这种疗法不需要改写DNA序列,只需要调节基因的表达状态——这意味着它的风险比传统基因编辑更低,也为更多类似的单基因神经疾病提供了模板。
目前的精准疗法主要惠及那20%携带明确罕见基因变异的自闭症患者,但剩下80%没有明确遗传诊断的患者,难道要被留在门外?
答案是否定的。科学家正在把从单基因疾病中获得的经验,拓展到更广泛的自闭症谱系。表观遗传编辑就是其中的核心方向——它不改变基因本身,而是通过调节DNA的甲基化、组蛋白修饰等“开关”,同时调控多个相关基因的表达。
比如CHD8基因是自闭症的高风险基因之一,它的突变会导致大脑发育异常。研究人员用CRISPR激活系统(CRISPRa),在人类干细胞衍生的脑类器官中精准激活CHD8基因的调控区域,成功让基因表达恢复到正常水平,纠正了神经前体细胞过度增殖的异常。这种方法不仅能用于单基因缺陷,还能针对多基因网络的异常进行调控——自闭症的发病往往不是单个基因出问题,而是一整套神经发育的“程序”紊乱,表观遗传编辑就像给这套程序打了个精准的补丁。
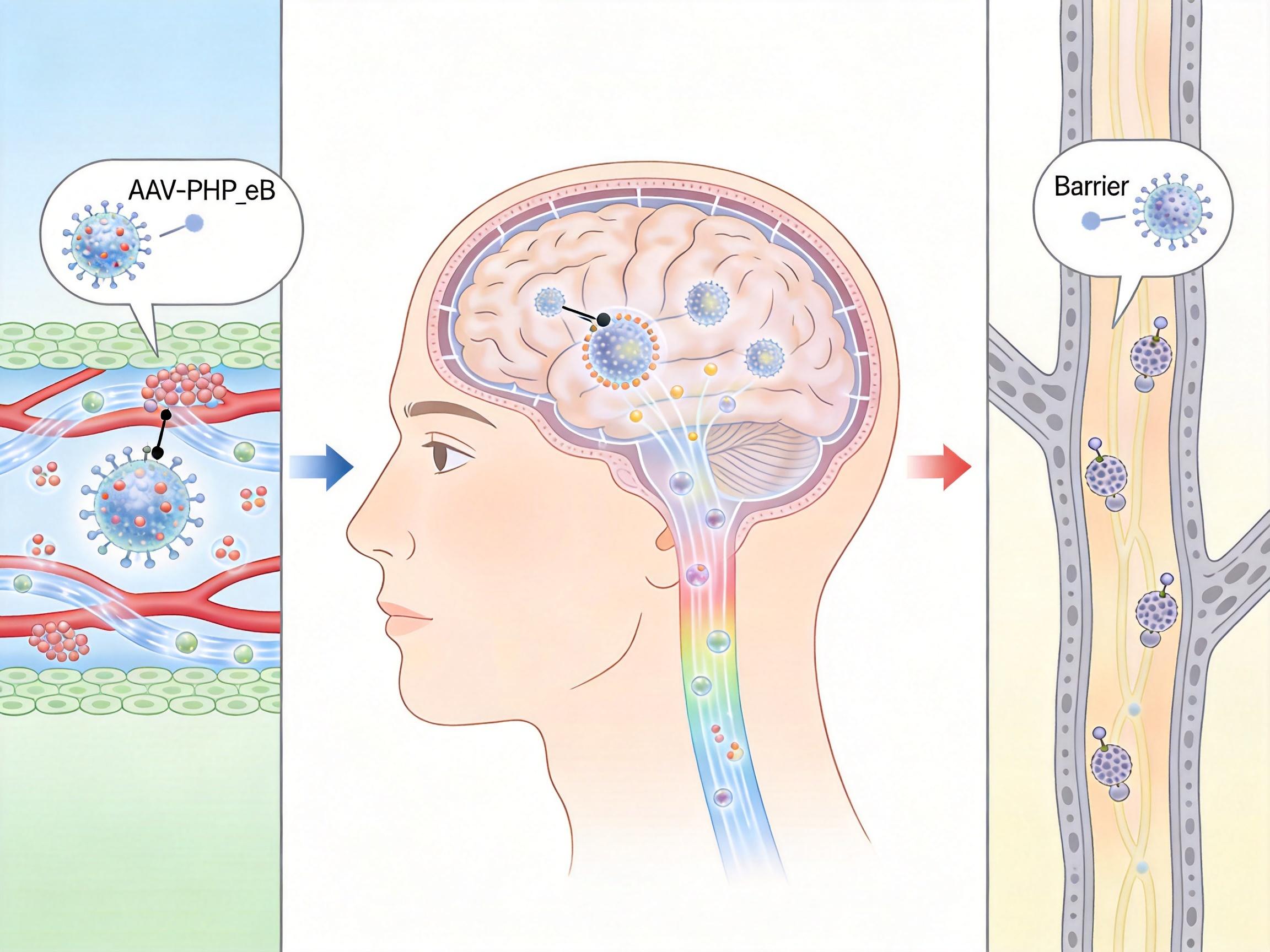
当然,这一切都绕不开一个难题:如何让这些分子工具穿过血脑屏障,精准到达大脑神经元。科学家正在优化AAV病毒载体和纳米颗粒递送系统,比如Caltech团队开发的AAV-PHP.eB载体,能通过静脉注射高效穿越血脑屏障,让全身给药成为可能。但目前这些技术还面临着免疫原性、长期安全性的挑战,距离大规模临床应用还有一段路要走。
精准医疗的美好蓝图背后,是一个个亟待解决的现实问题。最直接的就是费用:目前正在临床试验的ASO疗法,单次给药成本可能超过百万美元,这显然不是普通家庭能承受的。
另一个挑战是临床试验的设计。自闭症患者高度异质性,传统的大规模随机对照试验很难找到足够多的同类型患者。美国FDA推出的“合理机制框架”,允许科学家用自然病程数据、生物标志物替代传统对照,加速超罕见疾病疗法的审批;N-of-1个体化试验设计,也为单个患者的精准治疗提供了监管路径。这些政策正在打破罕见病药物开发的僵局。
但更重要的是,精准医疗不能只停留在“治疗”层面,还要延伸到“预防”和“早干预”。未来,新生儿基因筛查可能会普及,让携带高风险基因的孩子在出现症状前就得到干预;AI算法能结合临床数据、基因信息,为每个患者定制个性化的治疗方案,甚至预测治疗效果。这一切的目标,不是“治愈”自闭症,而是让每个患者都能获得最适合自己的支持,拥有更高的生活质量。
当Allyson Berent在会议厅里展示那些患者的视频时,台下的很多人都哭了——那是等待了几十年的希望,终于照进现实的眼泪。
精准医疗给自闭症治疗带来的,不只是技术的突破,更是一种认知的转变:自闭症不再是一种“无法治愈”的疾病,而是一系列可以被精准干预的神经发育异常。
精准不是少数人的特权,而是所有人的希望。 未来十年,随着技术的普及和政策的完善,更多曾经被“困住”的患者,将有机会重新掌握自己的人生。而这,才是科学最动人的地方——它总在你以为山穷水尽时,打开一扇新的门。