5 天前

5 天前
如果把细胞比作一座工厂,过去我们一直以为车间里的零件全靠随机飘移找工位——就像把一堆螺丝撒在地上,等它们碰巧滚到螺孔里。这是写进了几十年生物学教科书的“常识”。但2026年4月,俄勒冈健康与科学大学的团队推翻了这个常识:细胞里根本不是“无政府状态”,而是有一套像大气环流一样的定向流体“风系统”,能把关键蛋白质以比扩散快50倍的速度,精准吹到细胞运动的最前线。这不仅刷新了我们对细胞运作的理解,更给癌症转移的谜题递了一把新钥匙。为什么有些癌细胞能跑得这么快?答案或许就藏在这股看不见的“细胞风”里。
这个发现始于麻省海洋生物实验室的一堂神经生物学课。研究的主导者加尔布雷斯夫妇正带着学生做常规实验:用激光暂时“漂白”细胞后部的蛋白质,观察它们如何移动。按教科书的剧本,漂白的蛋白质应该慢慢随机扩散,最终均匀分布。但他们看到了完全不同的画面——细胞前缘居然出现了一条额外的暗带。
“我们一开始以为是实验误差,”凯瑟琳·加尔布雷斯回忆,“但重复了好几次,那条暗带都准时出现。” 这条暗带不是别的,正是被一股定向力量快速推到细胞前端的肌动蛋白波——而肌动蛋白,正是细胞伸展、移动和修复组织的核心材料。
为了看清这股“力量”的真面目,他们用上了Janelia研究院的iPALM技术——一种能把光学显微镜分辨率推到15纳米的干涉成像技术,相当于能看清一根头发丝直径的万分之一。iPALM的镜头下,细胞内部的秘密终于显形:细胞前缘有一道由肌动蛋白-肌球蛋白凝聚物构成的“无形屏障”,把细胞分成了前后两个区域;而细胞后部的肌球蛋白收缩,会像挤海绵一样产生水压梯度,驱动细胞质流体定向冲向细胞前端,形成了所谓的“细胞风”。
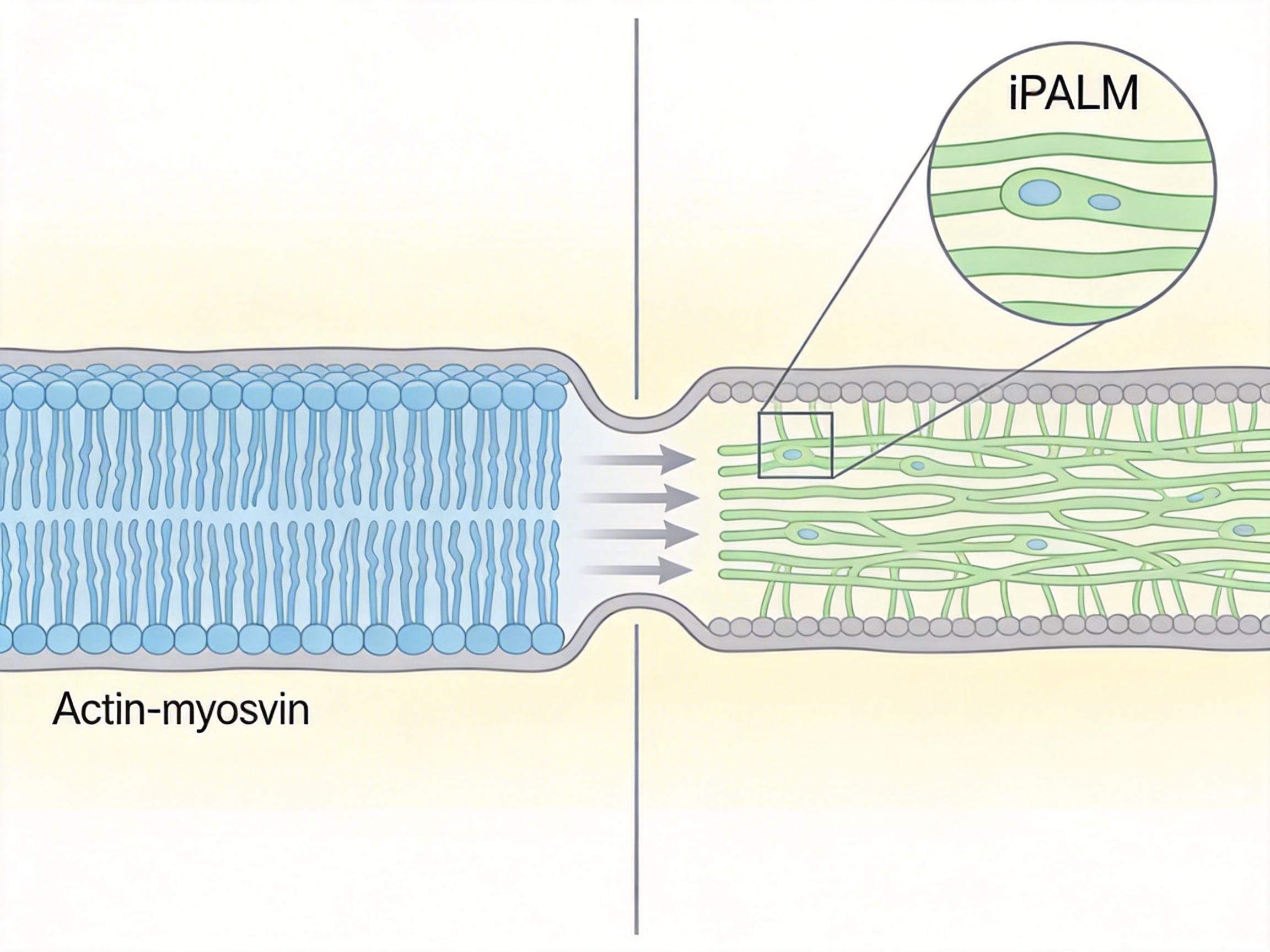
过去我们认为,细胞内的蛋白质运输要么靠随机扩散,要么靠“分子马达”沿着细胞骨架“跑腿”。但这两种方式都有局限:扩散太慢,赶不上细胞快速迁移的需求;分子马达只能点对点运输,效率太低。
“细胞风”的发现补上了这缺失的一环。它是一种“批量运输系统”——不需要识别特定蛋白质,只要在流场里,就能被一股脑儿推到前线。实验数据显示,肌动蛋白单体靠这股风的前向移动速度可达3.6±1.1微米/秒,是单纯扩散速度的50倍。更关键的是,这股风的方向和强度是可控的:细胞可以通过调整后部肌球蛋白的收缩力,改变流体的流速和方向,精准把蛋白质送到需要伸展或修复的位置。
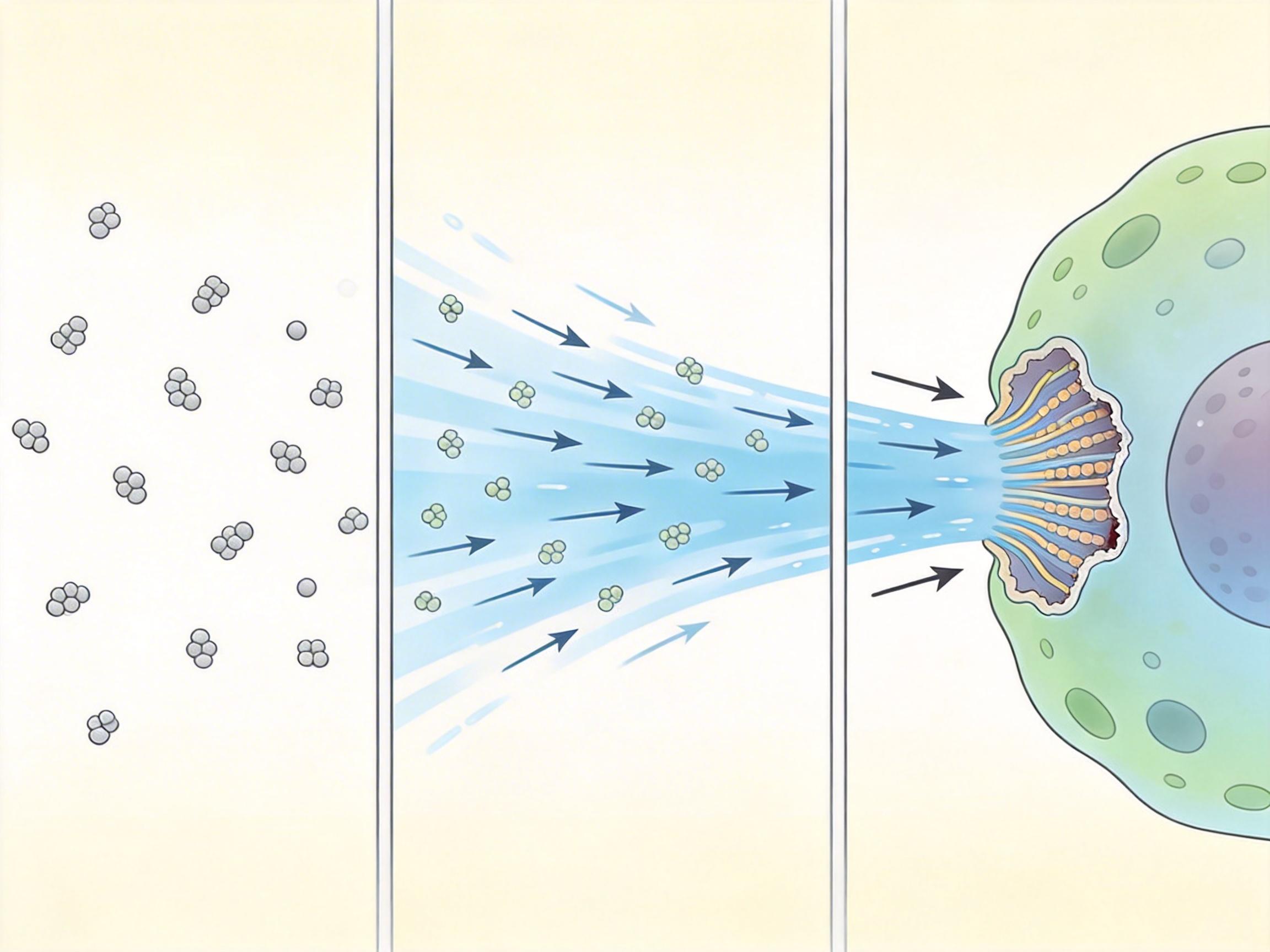
这解释了很多过去说不通的现象:为什么伤口能快速愈合?因为免疫细胞和修复细胞能通过“细胞风”快速调配材料,在伤口处搭建修复结构;为什么有些癌细胞侵袭性极强?因为它们把这套“风系统”开到了最大功率——和正常细胞相比,它们的肌球蛋白收缩更强劲,屏障结构更“听话”,能以远超正常细胞的速度,把迁移所需的蛋白质、信号分子送到细胞前缘,支撑它们快速突破组织屏障,在体内四处扩散。
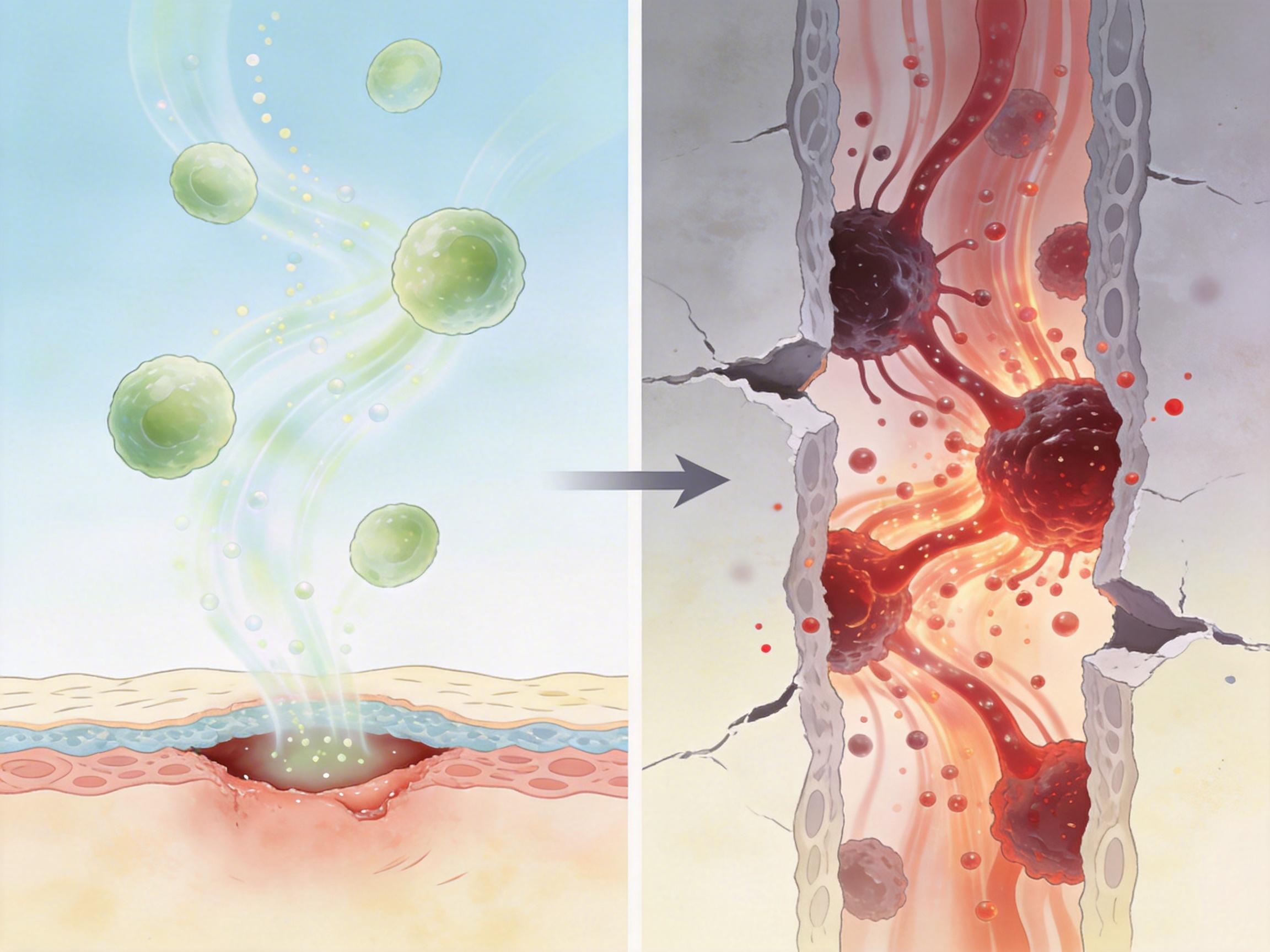
更值得关注的是,这套系统的运作不依赖任何膜结构,是一种“伪细胞器”——它靠蛋白质凝聚物形成的物理边界和流体压力维持功能,却没有传统细胞器的膜包裹。这意味着它的调控机制可能比我们想象的更灵活,也更脆弱——只要破坏肌球蛋白的收缩,或者打乱屏障的结构,就能让这股“风”停下来。
当然,这个发现还只是开始。目前的研究还只揭示了“细胞风”的基本框架,还有很多问题等待解答:不同细胞的“风系统”调控机制有什么差异?除了肌动蛋白,还有哪些分子会被这股风运输?“细胞风”和传统的分子马达运输之间,是如何协同工作的?
在临床应用上,最直接的潜力是抗癌转移。既然侵袭性癌细胞依赖“细胞风”快速迁移,那如果能找到只针对癌细胞“风系统”的抑制剂,就能在不影响正常细胞的前提下,阻断癌细胞的扩散。但这里也有挑战:正常细胞的“风系统”也参与伤口愈合、免疫反应等重要生理过程,如何精准区分癌细胞和正常细胞的调控差异,是未来研究的关键。
从技术层面看,“细胞风”的发现也依赖于成像技术的突破。如果没有iPALM这种纳米级分辨率的显微镜,我们根本看不到那道无形的屏障,更无法量化流体的速度和方向。未来更高时空分辨率的成像技术,或许能让我们实时观察“细胞风”在活细胞里的动态变化,甚至看清单个蛋白质在流场里的运动轨迹。
当我们以为已经摸清了细胞的运作规律时,它总会用新的发现提醒我们:生命的复杂度远超我们的想象。从随机扩散到定向“风系统”,这个发现不仅改写了教科书,更让我们对细胞的“智能”有了新的认知——细胞不是一堆分子的简单集合,而是一个能主动调控物理环境、优化资源分配的动态系统。
“生命的本质,是有序对无序的对抗。” 这股小小的“细胞风”,正是这种对抗的缩影:它用定向的流动,对抗分子随机扩散的无序,为细胞的运动、修复和生存提供了高效的支撑。而对我们来说,理解这股风的运作,不仅是破解癌症转移的关键,更是在靠近生命运作的核心逻辑——毕竟,每一个生命的运动,从细胞的迁移到我们的行走,本质上都是有序力量的胜利。
点击催更,成为大圆镜下一个视频选题!