对抗知识焦虑,从看懂这条开始
App 下载
被误认的脑内配角,竟是自闭症关键推手
小鼠行为实验|威尔康奈尔医学院|自闭症患者干细胞|星形胶质细胞|神经生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
小鼠行为实验|威尔康奈尔医学院|自闭症患者干细胞|星形胶质细胞|神经生物学|生命科学
2022年,纽约威尔康奈尔医学院的实验室里发生了一件颠覆常识的事:研究者把自闭症患者干细胞分化出的星形胶质细胞——一种曾被当成「脑内清洁工+后勤」的非神经元细胞——移植到健康新生小鼠脑中。原本活泼的小鼠渐渐变得刻板,反复做着埋弹珠的动作,甚至连熟悉的恐惧场景都记不清了。没人料到,这群一直被神经元光芒掩盖的「配角细胞」,居然能直接诱发自闭症核心症状。这背后,藏着半个世纪以来神经科学最被低估的认知盲区。
过去100年里,神经科学的聚光灯全打在神经元身上——毕竟是它们用电信号传递信息,构成了我们的思想和行为。星形胶质细胞(astrocytes)因为占脑内细胞总量的40%,却只会默默清理神经递质、维持离子平衡,被理所当然归为「支持细胞」,连研究经费都很难分到一杯羹。
直到20世纪80年代末,科学家才发现这群「星形小不点」能通过钙信号在细胞间传递信息,形成独立于神经元的庞大网络。更惊人的是,它们不是被动响应,而是主动调控:每一个星形胶质细胞的「触手」能包裹数十万甚至上百万个突触,像导演一样调节神经元的兴奋与抑制平衡,甚至直接释放胶质递质影响突触可塑性。
你可以把神经元想象成舞台上的演员,而星形胶质细胞是躲在侧幕的导演——它们不直接上台,但演员的节奏、灯光的明暗、甚至整个剧的走向,都在它们的掌控之中。但真实的机制比这更精确:星形胶质细胞通过IP3受体调控内质网钙释放,形成的钙波能在细胞间快速扩散,进而调节谷氨酸、ATP等信号分子的释放,最终影响神经元的放电频率和网络同步性。
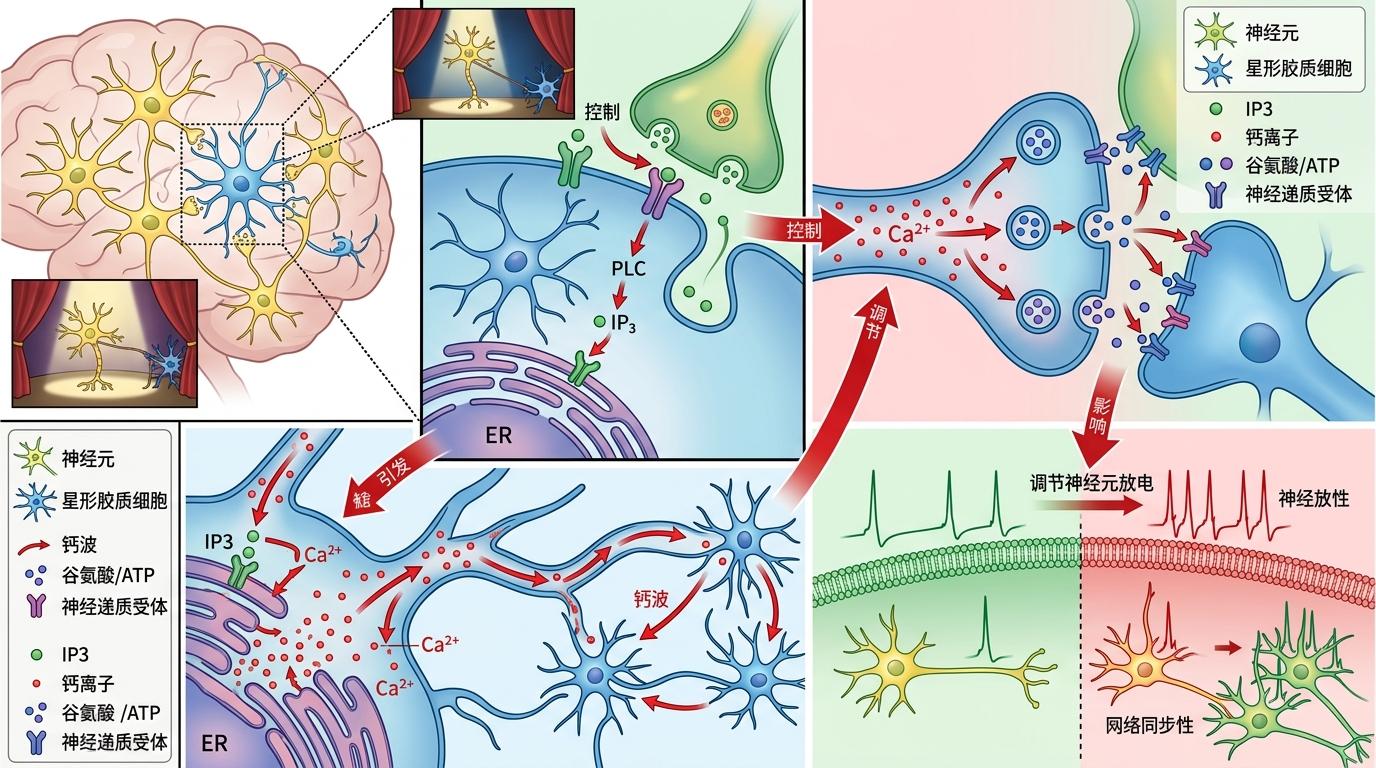
威尔康奈尔的移植实验,第一次把星形胶质细胞和自闭症的因果关系拍在了明处。他们发现,自闭症患者的星形胶质细胞存在一个核心缺陷:IP3受体介导的钙释放功能显著减弱,导致胞内钙信号波动异常——要么反应过度,要么时空协调性完全紊乱。
这种紊乱直接破坏了神经元的生存环境:异常的星形胶质细胞会过度分泌促炎因子IL-6,抑制神经元树突棘的生长;同时,它们清除谷氨酸的能力下降,导致脑内兴奋性神经递质堆积,打破兴奋-抑制平衡。当这些细胞进入健康小鼠脑内,就像把混乱的导演塞进了有序的剧组,原本正常的神经回路彻底失序——小鼠开始出现重复行为、记忆障碍,连海马区的长时程增强(LTP)都显著受损,而这正是学习记忆的核心神经机制。
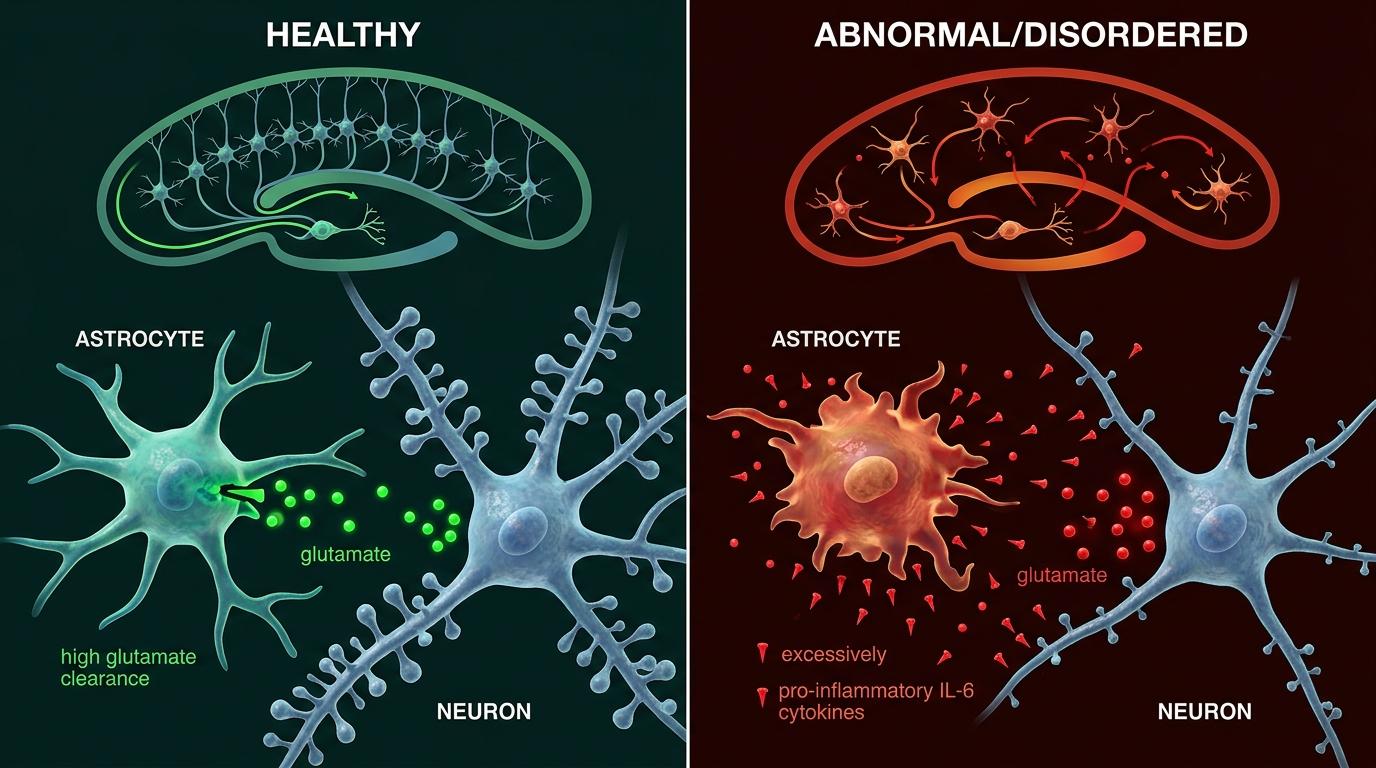
更关键的是,当研究者用基因技术下调星形胶质细胞的IP3受体,降低异常钙波动后,小鼠的重复行为居然得到了部分缓解。这意味着,星形胶质细胞的钙信号通路,可能是自闭症治疗的全新靶点——相比直接调控复杂的神经元网络,从「导演」入手调整整个剧组的秩序,或许是更高效的思路。
不过目前的研究仍有局限:移植实验只诱发了自闭症的部分核心症状,社交障碍并未出现。这说明星形胶质细胞可能只是自闭症病理拼图中的一块,而非全部。
星形胶质细胞的崛起,正在重构神经疾病的治疗框架。除了自闭症,阿尔茨海默病、抑郁症、癫痫等疾病中,都发现了星形胶质细胞的功能异常——比如抑郁症患者脑内的星形胶质细胞数量减少,谷氨酸转运功能下降;癫痫患者的星形胶质细胞钾离子调控功能紊乱,导致神经元过度兴奋。
针对星形胶质细胞的药物研发已经起步:抗炎药物如塞来昔布能抑制其过度分泌的IL-6,部分改善自闭症患者的行为;靶向IP3受体的调节剂也在动物实验中展现出潜力。但要走进临床,还有几道坎要跨:
首先是细胞异质性。不同脑区的星形胶质细胞分子标记和功能差异巨大,比如海马区的星形胶质细胞参与记忆调控,杏仁核的则负责情绪编码,一种药物很难覆盖所有亚型。其次是血脑屏障的限制,大部分药物无法有效到达脑内的星形胶质细胞。更重要的是,我们对星形胶质细胞与神经元、免疫细胞的交互机制还知之甚少——它们之间的信号通路像一张密密麻麻的网,牵一发而动全身,稍有不慎就可能引发新的神经紊乱。
当我们把视线从神经元移开,才发现脑内的「配角」们,正主导着一场认知革命。星形胶质细胞的故事,本质上是人类对自身认知的一次修正——我们曾以为生命的核心是那些最显眼的部分,却忽略了默默支撑、悄悄调控的「隐形力量」。
「脑的智慧,从来不是单一细胞的独奏。」这句话或许能概括这场革命的核心:无论是思考、记忆还是情绪,都是神经元、星形胶质细胞、小胶质细胞等所有细胞协同演奏的交响乐。而自闭症这类复杂疾病的答案,或许就藏在这些细胞的交互之中。未来的神经科学,终将从「神经元中心论」走向「脑网络整体论」,而那些曾被低估的「配角」,会在这场变革中,重新定义我们对脑的理解。