
3 个月前

3 个月前
抗生素,这个20世纪最伟大的医学发现之一,曾将人类的平均寿命延长了超过20年。然而,在这场人类与细菌的百年战争中,我们正节节败退。每年,全球有数百万人死于耐药菌感染,我们正滑向一个普通感染都可能致命的“后抗生素时代”。更棘手的是,一些细菌甚至无需进化出耐药性,就能在抗生素的轮番轰炸下存活。它们会进入一种**“休眠”或“假死”**状态,暂停生长,静待疗程结束,然后卷土重来,导致感染反复发作。我们如何判断抗生素是真的杀死了敌人,还是仅仅让它们暂时“装死”?这个问题,长期以来困扰着临床医生和科学家。
就在昨天(2026年1月12日),瑞士巴塞尔大学的研究团队在《自然微生物学》上投下了一枚重磅炸弹。由卢卡斯·博克(Lucas Boeck)博士领导的团队,开发出一种名为**“抗微生物单细胞测试”(antimicrobial single-cell testing)的革命性方法。这项技术宛如一部超高精度的摄像机,能够实时追踪数百万个独立细菌的命运。博克博士解释道:“我们用它来连续几天拍摄每一个细菌,观察药物是否以及多快能真正杀死它。” 这意味着,科学家们第一次能够直观地区分哪些药物是高效的“杀手”,哪些只是暂时的“麻醉剂”。当研究团队将该方法应用于结核病(由结核分枝杆菌引起)和另一种由其近亲脓肿分枝杆菌引起的严重肺部感染时,结果令人震惊:不同的药物组合,以及来自不同患者的菌株,其“耐受性”**——即在治疗中存活下来的能力——存在巨大差异。这一发现,为我们揭开了细菌“假死”骗局的一角。
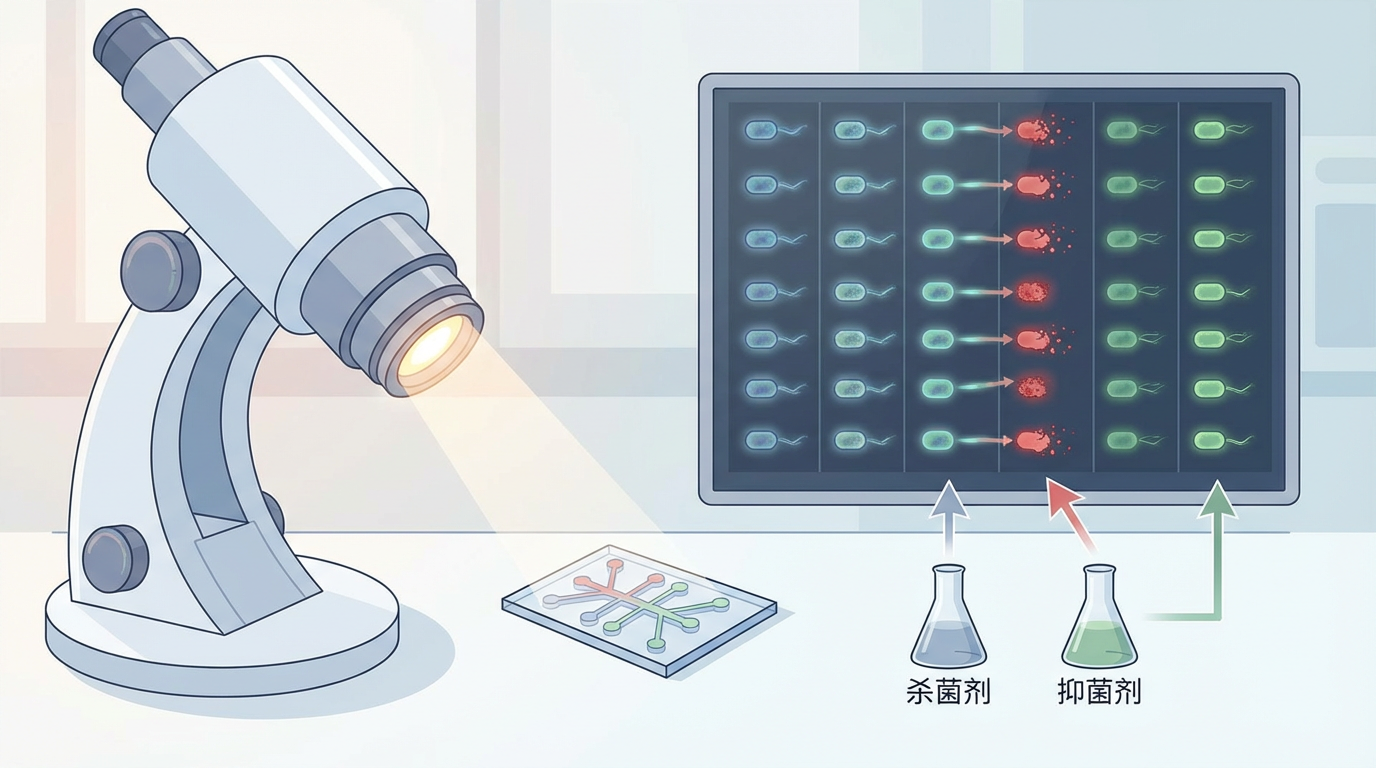
长期以来,评判抗生素疗效的金标准是**“最低抑菌浓度”(MIC),即在实验室中能抑制细菌生长的最低药物浓度。然而,这个标准存在一个根本性的盲点:抑制生长不等于彻底杀死。 许多被MIC标准判定为“有效”的药物,其实只是抑菌剂**(bacteriostatic),它们让细菌无法繁殖,最终依赖人体免疫系统完成“最后一击”。而杀菌剂(bactericidal)则能直接摧毁细菌,导致其死亡。在免疫系统功能不全的患者或面对结核病这类需要长期治疗的顽固感染时,这种区别至关重要。博克团队的新方法,正是从“抑制”的模糊地带,迈向了“杀灭”的精确领域。通过直接观察细菌的生死,该测试能精准量化一种疗法对整个细菌种群的杀灭效率。研究人员发现,细菌的特定基因特征会影响其耐受治疗的能力。“细菌对抗生素的耐受性越好,患者治疗成功的几率就越低。”博克博士说。更重要的是,这项新测试的结果与临床研究和动物模型的治疗效果高度吻合,证明了其强大的预测能力。
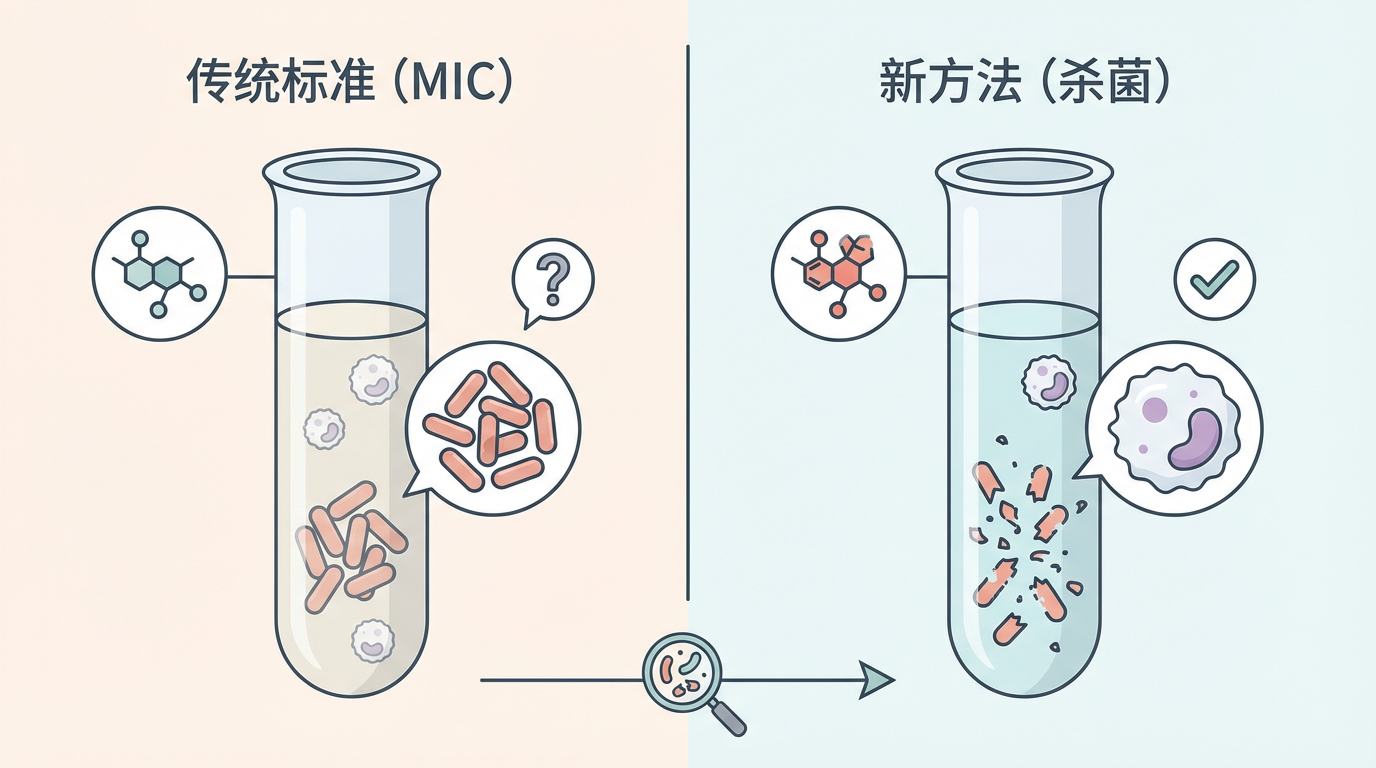
这场关于“杀灭”与“抑制”的精细化战争,源于近一个世纪的拉锯战。1928年,亚历山大·弗莱明在培养皿中偶然发现了青霉素,开启了抗生素的黄金时代。从链霉素攻克结核病,到各种“霉素”、“西林”层出不穷,人类一度以为已经驯服了这些微小的敌人。然而,细菌的进化速度远超我们的想象。抗生素的每一次广泛使用,都像一场自然选择的大筛选,催生出更强大的耐药菌株。抗生素滥用,无论是在医疗还是农业领域,都极大地加速了这一进程。如今,世界卫生组织(WHO)的重点病原体清单上,碳青霉烯类耐药的鲍曼不动杆菌(CRAB)、**肺炎克雷伯菌(CRKP)**等“超级细菌”被列为“关键优先级”,它们对多种甚至所有已知抗生素都刀枪不入,让医生束手无策。我们迫切需要新的武器,更需要新的作战策略。
巴塞尔大学的这项突破,正是新策略的曙光。它预示着感染治疗将从“地毯式轰炸”的经验用药时代,迈向“精确制导”的个体化治疗新时代。
尽管前景光明,但“抗微生物单细胞测试”要从前沿研究走向常规临床应用,仍有几座大山需要翻越。
博克团队的单细胞追踪技术,并非孤立的突破。它与近年来飞速发展的单细胞RNA测序(如BacDrop技术)、微流控技术、人工智能辅助药物发现以及噬菌体疗法等前沿探索一道,共同构成了对抗细菌耐药的立体战线。这些技术的核心思想是一致的:深入到单个细胞的微观层面,理解细菌的异质性、生存策略和脆弱之处。人类与细菌的战争永无终点,但巴塞尔的这项新发现,让我们得以告别过去那种“凭经验猜谜”式的治疗方式。通过为每一个微小敌人建立档案,实时监控它们的生死存亡,我们正在将抗生素的使用从一门艺术,转变为一门精确的科学。这不仅是对现有武器库的一次重大升级,更是作战理念的根本性变革,为我们在后抗生素时代的生存之战中,赢得了宝贵的主动权。
点击充电,成为大圆镜下一个视频选题!