20 天前

20 天前
想象一下:一位肺癌患者躺在PET扫描仪上,半小时后,屏幕上没有模糊的阴影,只有一块边界清晰、亮度精准的光斑——那是他体内的肿瘤,正清晰地“报出”自己的分子身份:EphA2蛋白高表达。医生立刻知道,针对这个靶点的靶向药会是他的最优解,不用再经历试错般的治疗。这不是科幻,是密苏里大学Barry Edwards团队刚拿出的新工具:用带放射性标记的迷你抗体当“分子手电筒”,让藏在体内的肿瘤在PET扫描里现形。但问题是,这个“手电筒”是怎么精准找到肿瘤的?它又能给抗癌带来什么本质改变?
你可以把这个过程看成一场定制化的狩猎——先给猎人配好专属追踪器,再用卫星定位锁定目标。 这里的“猎人”是迷你抗体(Minibody),一种被人工缩小的抗体片段,只有完整抗体的三分之一大。它的任务是找到癌细胞表面的专属标记:EphA2蛋白。这种蛋白像肿瘤的“身份证”,在肺癌、乳腺癌、胰腺癌等十多种癌症里大量存在,却几乎不在正常细胞上出现。Edwards团队给这个迷你抗体做了两个关键改造:一是让它对EphA2的亲和力达到了0.63纳摩尔级——相当于在一个足球场里,能精准找到唯一的那只足球;二是给它挂上了一个^64Cu放射性标记,这个标记会在PET扫描时发出信号,像给肿瘤装了个GPS。
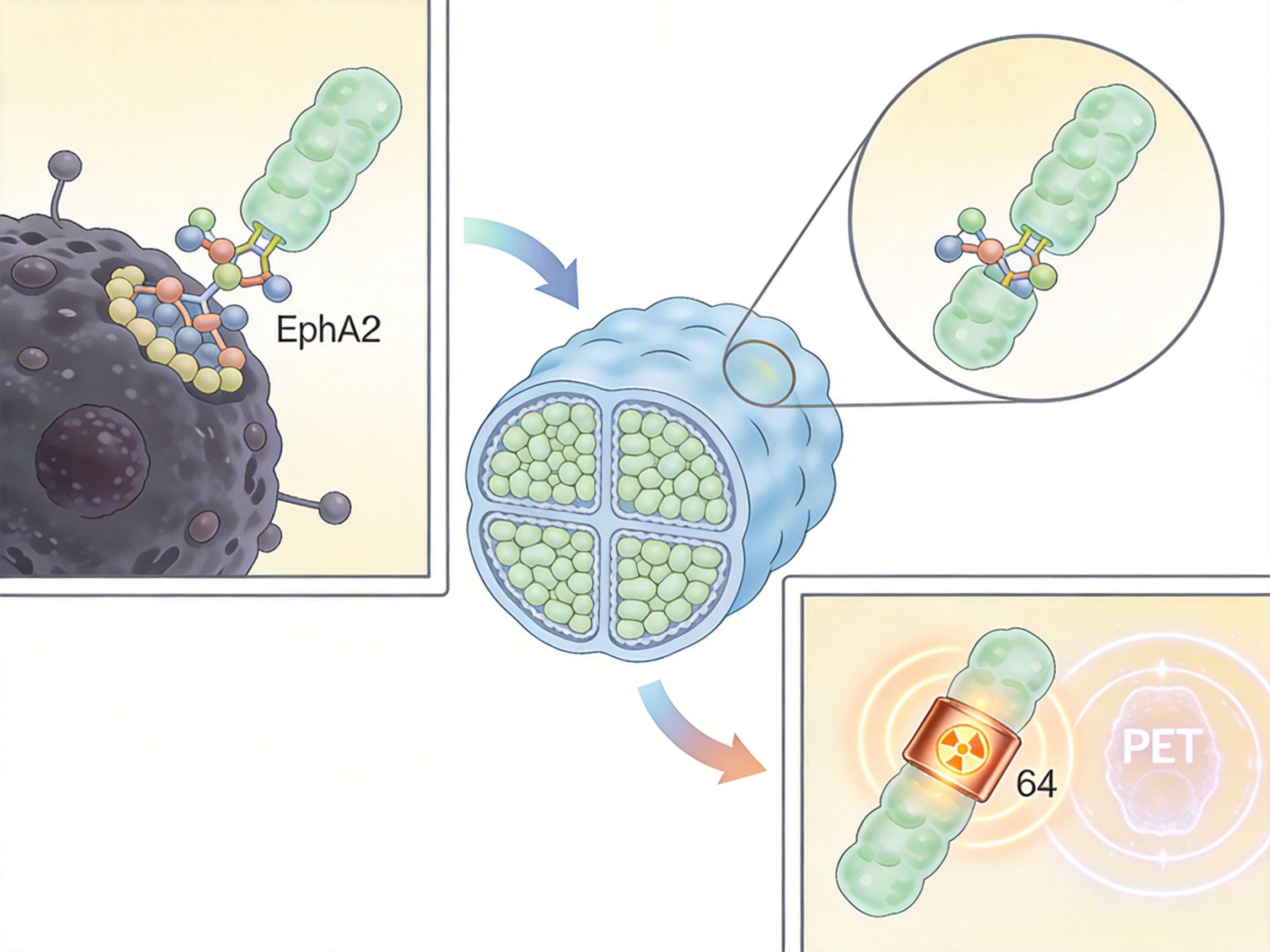
当这个“带追踪器的猎人”注入体内后,迷你抗体的小体积优势立刻显现:它能快速穿透肿瘤组织,同时在血液里快速清除,不会在正常器官里逗留太久。在小鼠实验里,注射4小时后,肿瘤部位的抗体摄取量就达到了25.53%ID/g——意味着每克肿瘤组织里,有超过四分之一的注射剂量精准聚集,而正常组织的信号几乎可以忽略。
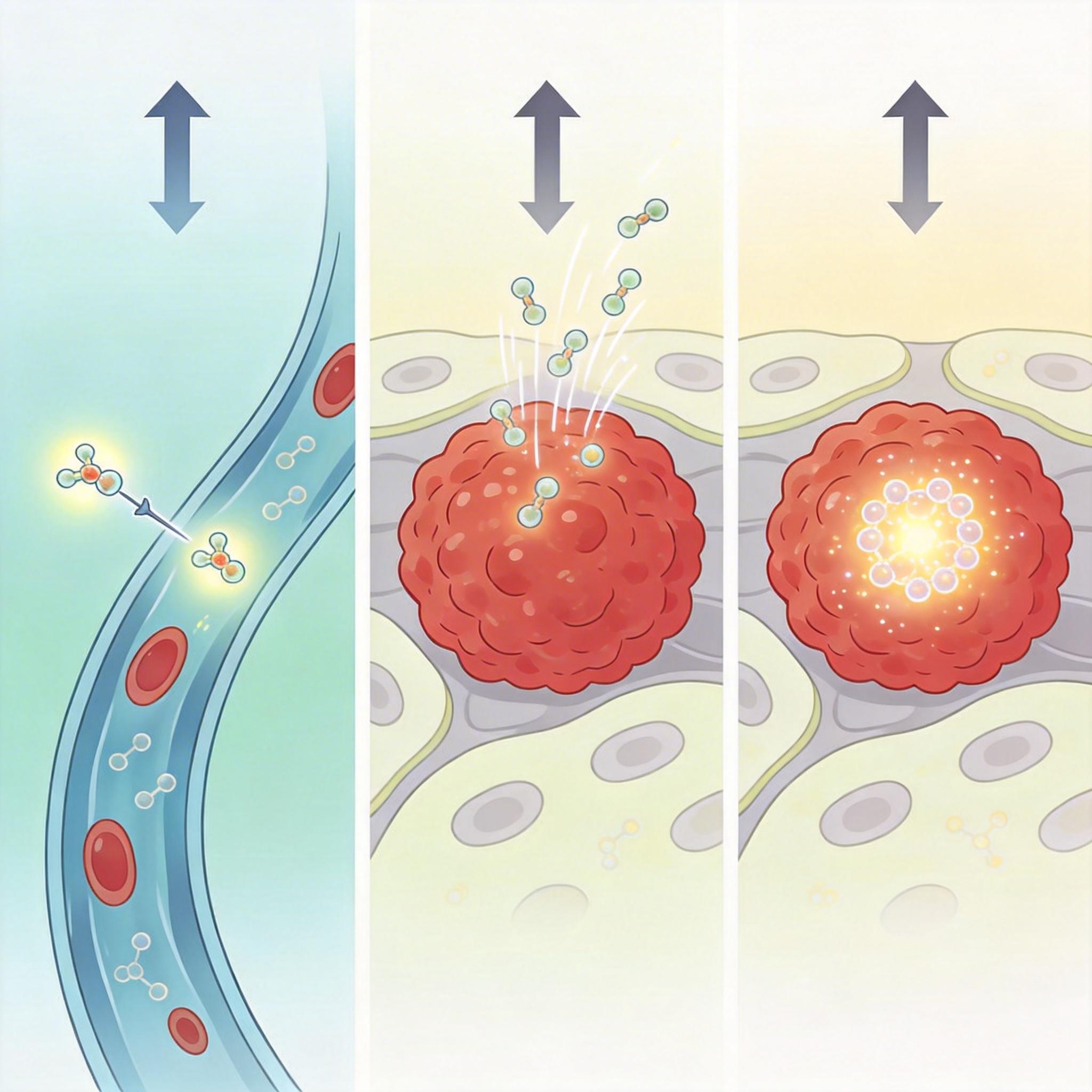
这个数据不是凭空来的。团队做了对照实验:同时注射无标记的迷你抗体竞争结合位点,肿瘤的信号立刻下降了一半,证明它的结合完全是特异性的,不会“认错人”。
过去,医生给患者用靶向药,有点像“开盲盒”。 比如针对EphA2的靶向药,明明只对高表达EphA2的患者有效,但传统的活检只能取肿瘤的一小部分组织,万一取的刚好是EphA2低表达的区域,就会导致“假阴性”——明明患者适合治疗,却被排除在外;反之,也可能给不适合的患者用药,白花钱还遭罪。而这个免疫PET技术,相当于给医生开了个“上帝视角”:它能一次性扫描全身所有肿瘤病灶,不管是原发灶还是转移灶,都能精准量化EphA2的表达量,甚至能区分同一个肿瘤里不同区域的表达差异。 我认为,这才是这项技术最被低估的价值:它不是简单的“看清楚肿瘤”,而是把抗癌从“试错模式”切换到了“精准匹配模式”。Edwards团队算过一笔账:如果能提前筛选出适合靶向治疗的患者,每一位患者能节省至少3个月的无效治疗时间,以及数万元的治疗费用。更重要的是,它能避免患者在无效治疗中承受的副作用——那些靶向药不会伤害正常细胞,但如果用在不适合的患者身上,每一次给药都是对身体的无意义消耗。 在HER2阳性乳腺癌的治疗里,类似的逻辑已经被验证:用^89Zr标记的曲妥珠单抗做PET成像,能比传统活检更准确地识别HER2阳性病灶,预测靶向药的疗效,准确率能达到100%。现在,这个逻辑被复制到了EphA2靶点上,未来还能扩展到EGFR、PD-L1等更多肿瘤标记物。
当然,这个“分子手电筒”也不是万能的。 它目前还面临几个关键挑战:首先是放射性标记的稳定性,^64Cu虽然半衰期适中,但如果标记工艺不够精准,可能会在体内脱落,导致正常组织的背景信号升高;其次是迷你抗体的肾脏摄取问题,因为小分子量的蛋白会通过肾脏代谢,可能会给肾脏带来一定的辐射负担;最后是成本,目前这种定制化的迷你抗体和放射性标记,成本还比较高,大规模临床应用需要进一步优化生产工艺。 但这些挑战都在被逐步解决。比如团队已经在尝试用更稳定的螯合剂固定^64Cu,减少标记脱落;也在通过基因工程改造迷你抗体的结构,降低肾脏的非特异性摄取。更值得期待的是“诊疗一体化”的方向:未来可以用同一个迷你抗体,既标记^64Cu做成像,又标记治疗性放射性核素(如^67Cu)做治疗——先给患者做PET成像,确认肿瘤的位置和靶点表达,立刻就能用同一个抗体进行精准放疗,真正实现“诊断即治疗”。 目前,这项技术已经在小鼠实验里验证了安全性和有效性,Edwards团队计划在未来7年内推进到人体临床试验。如果一切顺利,它会成为精准抗癌的又一个核心工具。
当我们谈论抗癌的进步时,往往会聚焦于新药的研发、治疗方案的创新,但很多时候,“看清楚”的意义并不亚于“治疗”本身。 这个能让肿瘤“发光”的迷你抗体,本质上是给医生和患者提供了一个“决策工具”——它把模糊的“可能有效”变成了精准的“确定有效”,把被动的“试错治疗”变成了主动的“精准匹配”。 看见,才是精准治疗的第一步。 未来的抗癌战场,不会是医生拿着各种药物挨个尝试,而是先给肿瘤做一次“分子CT”,精准定位它的弱点,再用最适合的武器一击即中。这束从分子世界发出的光,正在照亮抗癌的新路径。
点击催更,成为大圆镜下一个视频选题!