对抗知识焦虑,从看懂这条开始
App 下载
缺了一种蛋白,肺癌就学会了卷土重来
细胞凋亡|化疗耐药|caspase-8蛋白|小细胞肺癌|肿瘤学|医学健康
五年生存率仅5%,初期对化疗响应率超60%,却几乎注定在半年内复发——这就是小细胞肺癌(SCLC),肺癌里最凶险的“隐形杀手”。患者熬过了第一轮化疗的副作用,却往往躲不过肿瘤卷土重来后的极速恶化。
科隆大学的科学家最近在《自然·通讯》上揭开了这个致命循环的关键:小细胞肺癌细胞普遍缺失一种叫caspase-8的蛋白,正是它的缺席,触发了一连串让肿瘤越变越强的连锁反应。为什么一种蛋白的缺失会让癌症变得如此难缠?这要从细胞死亡的“生死开关”说起。
生死开关失灵:从“温和清理”到“炎症风暴”
你可以把caspase-8蛋白想象成细胞里的“温和清道夫”——它负责启动“程序性细胞死亡(凋亡)”:当细胞受损或癌变时,它会引导细胞安静地自我溶解,全程不会引发炎症,就像用碎纸机悄悄处理掉废纸。
但真实的机制比这更精确:caspase-8是外源性凋亡通路的核心启动因子,它通过与死亡受体结合,激活下游酶类,让异常细胞“体面退场”,同时避免释放细胞内容物引发免疫紊乱。
当小细胞肺癌细胞缺失caspase-8时,这个温和的清理程序就失灵了。细胞死亡的控制权被转交给另一条通路:坏死性凋亡(necroptosis)。这是一种“暴力死亡”——细胞膜破裂,细胞内的损伤相关分子模式(DAMPs)被大量释放,就像在组织里引爆了一颗炎症炸弹。
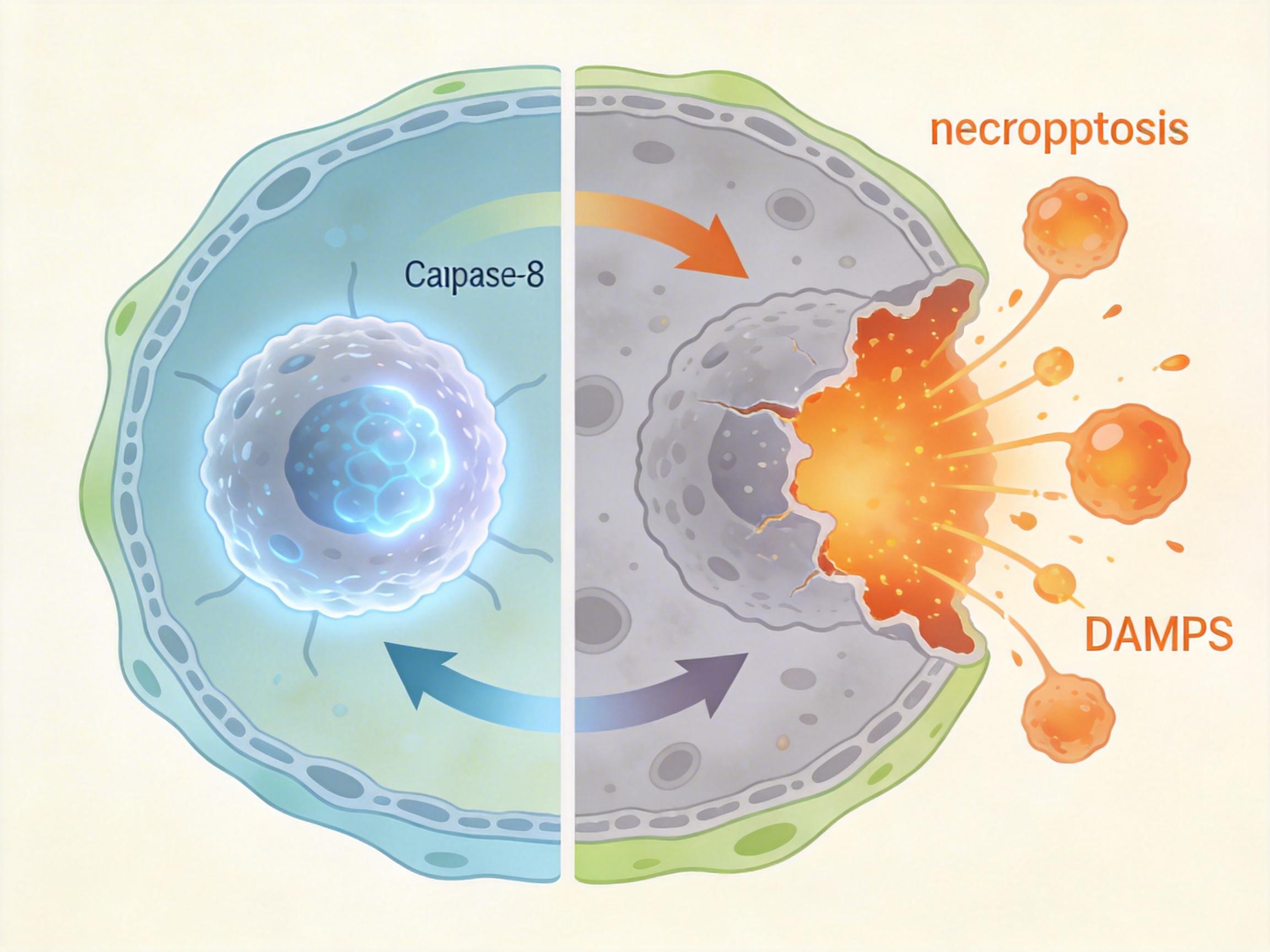
研究团队用敲除caspase-8的基因工程小鼠做实验,发现肿瘤还没完全形成,肺部就已经出现了明显的炎症浸润:中性粒细胞、巨噬细胞大量聚集,促炎因子IL-6、TNF-α的水平飙升。
炎症温床:癌细胞的“变身”与免疫逃逸
这场由caspase-8缺失引发的炎症风暴,成了肿瘤生长的“温床”。
首先,炎症环境会招募大量调节性T细胞(Tregs)和M2型巨噬细胞——前者分泌免疫抑制因子,压制效应T细胞的抗肿瘤活性;后者则像“帮凶”一样,分泌血管生成因子,给肿瘤输送营养。小鼠模型显示,缺失caspase-8的肺部组织中,Tregs的比例比正常组织高出3倍,免疫系统彻底沦为了肿瘤的“保护伞”。
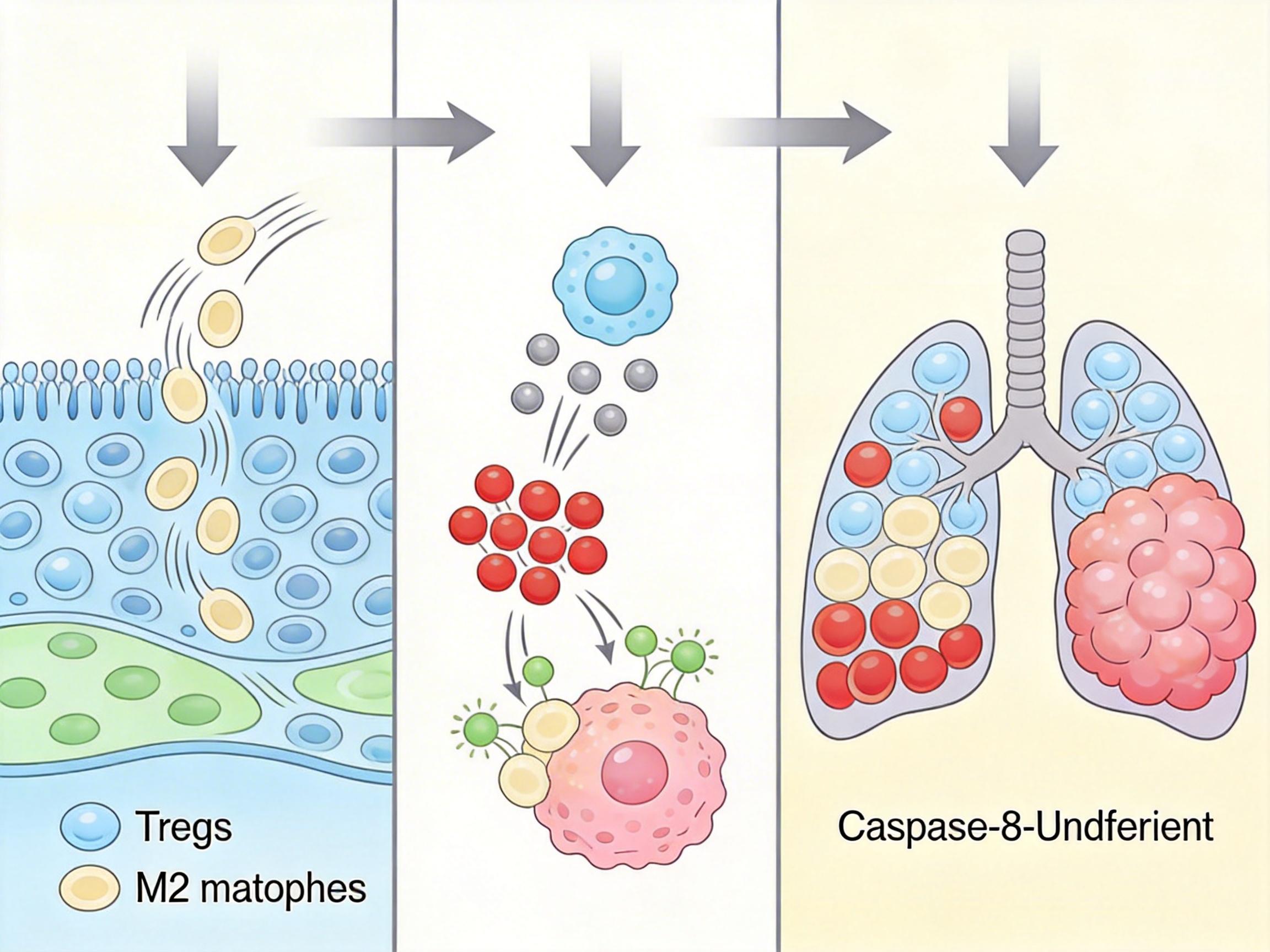
更可怕的是,炎症信号还会诱导癌细胞“变身”:小细胞肺癌原本就带有神经细胞的特征,而炎症会进一步推动癌细胞向“神经祖细胞样”状态重编程——这种未成熟的细胞拥有更强的增殖、迁移能力,就像回到了“干细胞阶段”,能轻易躲过化疗药物的攻击,还能在体内到处转移。
单细胞RNA测序证实,这种神经祖细胞样的基因特征,在复发的人类小细胞肺癌样本中显著富集。也就是说,caspase-8缺失不仅让癌细胞逃避免疫监视,还让它们进化出了“耐药体质”。
研究团队还发现了关键的执行分子MLKL:它是坏死性凋亡通路的“最终执行者”,敲除MLKL后,小鼠的炎症反应显著减轻,肿瘤转移率下降40%以上,神经祖细胞样的重编程也被逆转。
亚型差异:同一种蛋白的“双面人生”
有意思的是,caspase-8在不同肺癌亚型里扮演着完全不同的角色。
在非小细胞肺癌(NSCLC)中,caspase-8通常高表达,但它的促凋亡功能会被另一种蛋白c-FLIP抑制。这时的caspase-8反而会通过激活NF-κB通路,促进炎症因子的产生,推动肿瘤生长。研究显示,用抑制剂阻断caspase-8后,非小细胞肺癌的肿瘤负荷能减少一半以上。
而在小细胞肺癌中,caspase-8的缺失是“标志性事件”——约79%的小细胞肺癌细胞系都检测不到它的表达,这主要是因为基因启动子区域被甲基化沉默了。
这种差异意味着,针对caspase-8的治疗策略必须“分型而治”:对非小细胞肺癌,要抑制caspase-8的促炎功能;对小细胞肺癌,或许可以通过去甲基化药物恢复caspase-8的表达,或者直接靶向MLKL阻断炎症通路。
更值得关注的是,目前这一机制还只在小鼠模型中得到了完全验证,人类患者体内是否存在同样的“炎症-重编程”轴,还需要更多临床样本的验证。
当我们把癌症当成“敌人”时,总想着用药物彻底消灭它,却常常忽略了肿瘤微环境里的“暗流涌动”。caspase-8的缺失不是一个孤立的事件,它像多米诺骨牌的第一张,推倒了细胞死亡的平衡,引发了炎症、免疫抑制、细胞重编程的连锁反应,最终让肿瘤变得无孔不入。
蛋白缺一点,肿瘤恶十分。 这个发现让我们意识到,癌症的凶险不仅在于癌细胞本身,更在于它能利用人体的生理机制“反客为主”。未来的治疗或许不只是瞄准癌细胞,还要修复那些被打破的平衡——比如重启caspase-8的“温和清理”程序,或者阻断MLKL的“炎症开关”。
毕竟,对付狡猾的敌人,我们需要的不只是武器,还有读懂它战术的能力。