对抗知识焦虑,从看懂这条开始
App 下载
清走脑内斑块却没用,阿尔茨海默病药踩了坑
Cochrane研究|斑块清除疗法|淀粉样蛋白斑块|阿尔茨海默病|神经退行性疾病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
Cochrane研究|斑块清除疗法|淀粉样蛋白斑块|阿尔茨海默病|神经退行性疾病|医学健康
20342名早期阿尔茨海默病患者、17项临床试验、7款热门药物——当这些数字被Cochrane的研究者汇总到一起时,结果给了整个领域一记闷棍:那些花了几十亿美元研发、旨在清除脑内淀粉样蛋白斑块的药物,几乎没给患者带来任何能感知到的好处。更糟的是,每10个用药患者里,就有1到3人会出现脑肿胀或微出血,有些甚至没有明显症状。为什么被寄予厚望的「斑块清除疗法」会走到这一步?我们得从那个统治了学界30年的假说说起。
你可以把阿尔茨海默病的大脑想象成一个被垃圾堆满的图书馆——淀粉样蛋白β就是那些堆在书架前的废纸团,科学家们坚信,只要把这些废纸清走,读者(神经元)就能重新顺畅地取书(传递信号)。这个「淀粉样蛋白假说」从1992年提出以来,一直是药物研发的绝对核心:早发性患者的基因突变会导致更多「废纸」产生,无症状老人的脑内也能提前发现「废纸堆」,甚至有基因变异能减少「废纸」,降低患病风险。
但真实的大脑比图书馆复杂得多。
直给段落:
当药企们顺着「清废纸」的思路砸钱,造出了能精准绑定斑块、调动免疫细胞吞噬的单抗药物时,临床数据却泼了冷水:这些药物确实能把脑内斑块扫干净,但患者的记忆力、日常生活能力,甚至痴呆的严重程度,几乎没有变化。用研究者的话说,「改善幅度远低于患者能感知到的临床阈值」。
比无效更让人不安的是那些看不见的副作用。
抗淀粉样蛋白药物最常见的不良反应是「淀粉样相关影像异常」(ARIA),分为两种:一种是脑内出现水肿,像海绵一样吸饱了水;另一种是微出血,就像大脑里出现了无数针尖大的血点。这些异常大多只能通过MRI扫描发现,患者可能只是有点头痛、头晕,甚至完全没感觉——但谁也不知道,这些看不见的损伤会不会在未来引发更严重的问题。
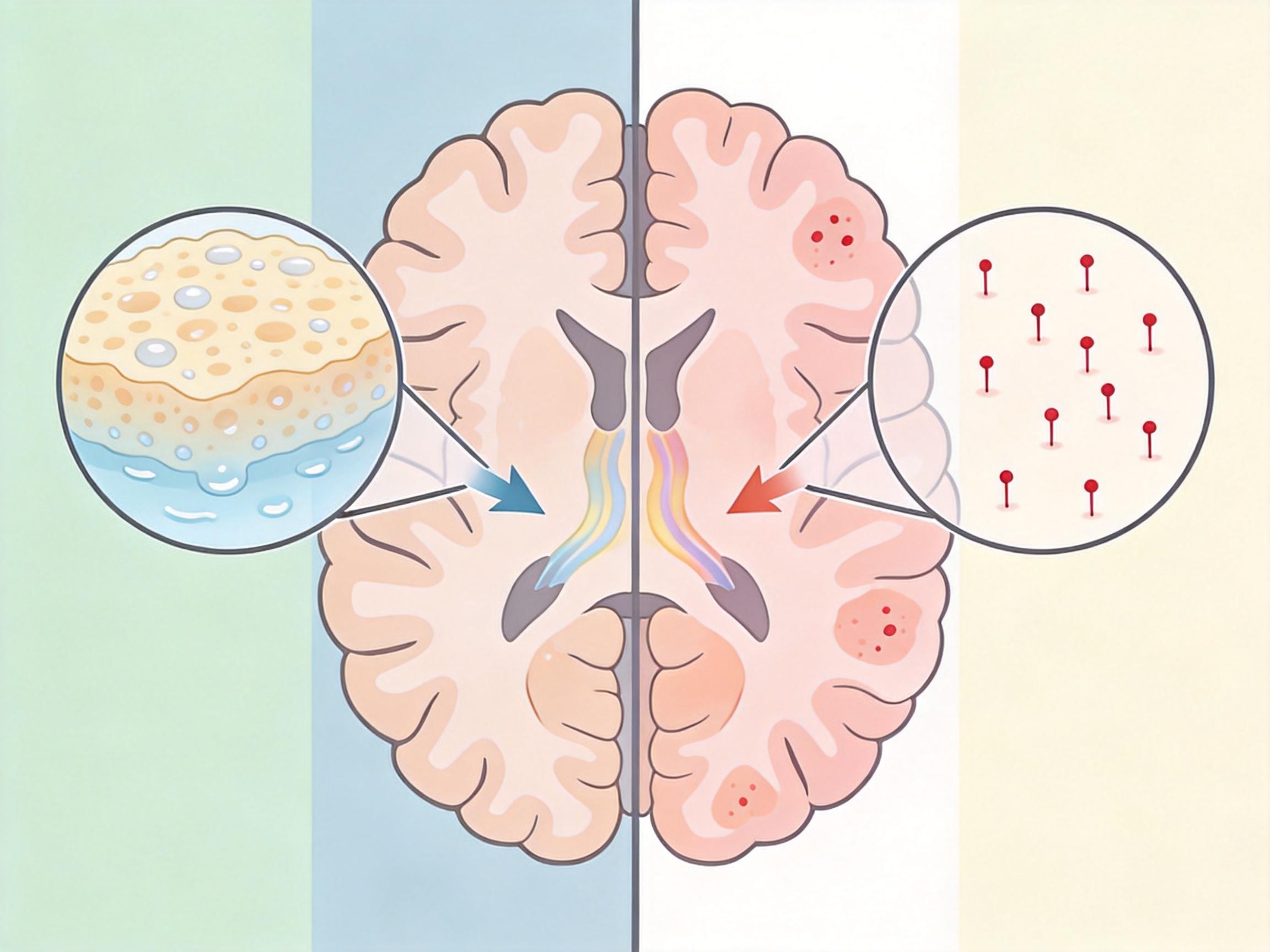
风险还和基因挂钩:携带APOE ε4等位基因的患者,脑内血管本来就更脆弱,用药后出现水肿的风险是普通人的3到11倍。在多纳单抗的临床试验里,24%的患者出现了脑水肿,6.1%的人因此出现了明显症状,甚至有极少数病例导致了死亡。
更现实的问题是成本:这些药物需要静脉注射,每月花费动辄上万美元,还得定期做MRI监测副作用。对医疗系统来说,这是一笔沉重的负担;对患者来说,花了钱、遭了罪,却换不来切实的改善——这种落差,比副作用更让人绝望。
现在,越来越多的研究者开始把目光从「清斑块」转向「灭火灾」。
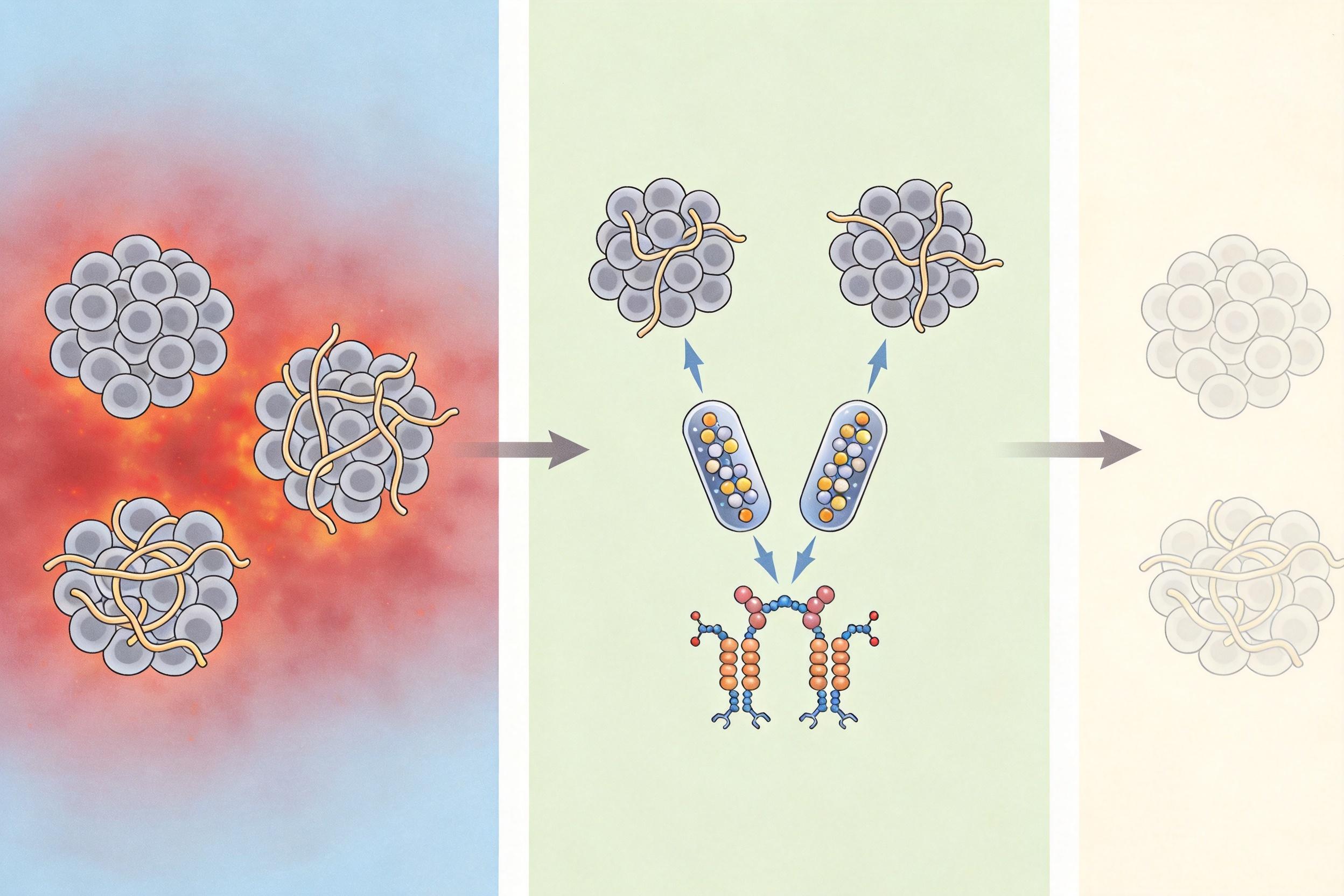
有人瞄准了tau蛋白——这种会在神经元内缠成结的蛋白质,才是和认知衰退直接相关的「纵火犯」。目前已有多款靶向tau的药物进入临床试验,有的试图阻止tau蛋白聚集,有的想切断它在脑内扩散的路径。还有人盯上了神经炎症:激活的小胶质细胞本来是大脑的「消防员」,但在阿尔茨海默病患者脑内,它们会失控攻击正常神经元,JAK抑制剂、TNFα抑制剂等抗炎药物正在测试能否平息这场混乱。
更有前景的是多靶点组合疗法——就像同时用灭火器、洒水车和防火材料一样,同时针对淀粉样蛋白、tau蛋白和炎症。比如把抗Aβ单抗和抗tau药物联用,或者用一款药物同时抑制β分泌酶(产生Aβ的酶)和GSK-3β(促进tau缠结的酶)。
AI也正在改变游戏规则:通过分析多模态数据(临床症状、影像、生物标志物),它能精准识别阿尔茨海默病的不同亚型,把对药物敏感的患者筛选出来,避免无效治疗。甚至能预测患者的病情进展速度,帮医生制定个性化的干预方案。
当我们回望这30年的研发历程,会发现「淀粉样蛋白假说」的最大价值,或许不是造出了多少药物,而是让我们看清了阿尔茨海默病的复杂性——它不是单一蛋白堆积的疾病,而是一场涉及整个大脑生态系统的崩塌。
「清除斑块不是答案,解决问题才是。」这句话正在成为领域内的共识。对那些在诊室里盼着有效治疗的患者来说,这或许是个迟到的结论,但至少,我们终于从死胡同里转了出来,朝着真正的答案又近了一步。