对抗知识焦虑,从看懂这条开始
App 下载
癌症基因灾变元凶锁定:N4BP2酶如何引爆染色体?
基因组不稳定性|加州大学圣地亚哥分校|染色体灾变|N4BP2酶|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
基因组不稳定性|加州大学圣地亚哥分校|染色体灾变|N4BP2酶|肿瘤学|医学健康
在癌症的微观战场中,癌细胞的基因组并非一本稳定传承的生命法典,而更像是一部被疯狂篡改、撕毁和重写的混乱手稿。正是这种持续的混乱,赋予了癌症狡猾的进化能力,使其能够逃避治疗、疯狂增殖。然而,在这场混乱中,最极端、最富戏剧性的事件——染色体灾变(Chromothripsis),其“点火器”究竟是什么,十多年来一直困扰着科学家。如今,这个谜题的答案终于浮出水面。
加州大学圣地亚哥分校(UC San Diego)的科学家们发布了一项里程碑式的研究,精准锁定了引爆这场基因组灾难的幕后黑手。这项发表于顶尖期刊《科学》(Science)的报告指出,一种名为**N4BP2**的酶,是导致染色体灾变的直接元凶。
研究团队由细胞与分子医学教授唐·克利夫兰(Don Cleveland)博士领导,他们发现,在约四分之一的癌症(尤其在骨肉瘤和脑癌等恶性肿瘤中比例更高)中观察到的染色体灾变现象——即单条染色体在一次灾难性事件中被粉碎成数十甚至数百个片段,然后被错误地重新拼接——其始作俑者正是N4BP2。
克利夫兰博士指出:“这一发现最终揭示了点燃癌症中最具侵袭性基因组重排的‘分子火花’。通过找到最初是什么打破了染色体,我们现在有了一个全新的、可操作的干预点来减缓癌症的进化。”
染色体灾变的故事,始于一个名为**“微核”(Micronucleus)**的结构。在细胞分裂的混乱中,某些染色体可能会“掉队”,被包裹在一个脆弱、临时的核膜中,形成一个与主细胞核隔离的“微型监狱”。
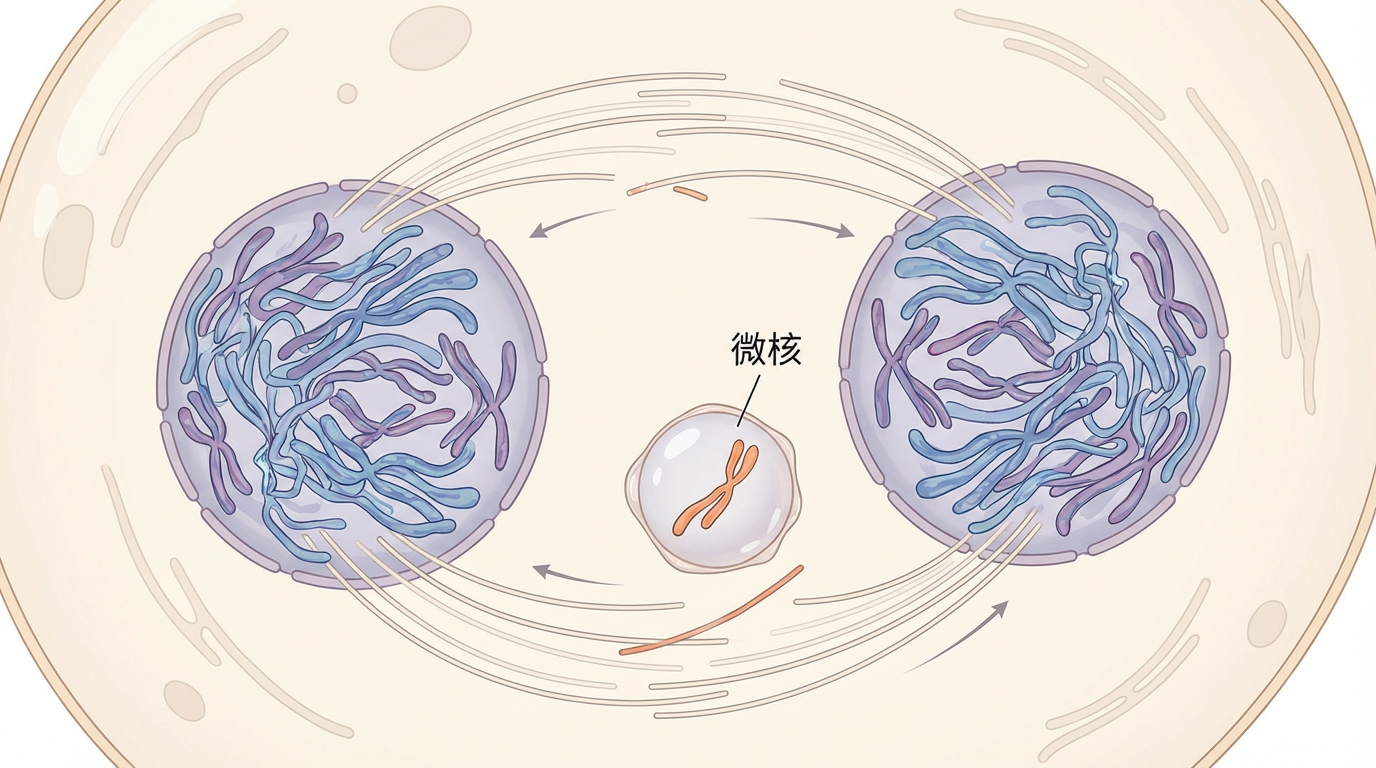
然而,这个监狱的围墙并不坚固。微核的核膜一旦破裂,被囚禁的染色体就瞬间暴露在充满各种酶的细胞质中,一场“屠杀”随即上演。加州大学圣地亚哥分校的团队通过精密的成像筛选技术,在204种已知和推定的人类核酸酶中进行排查,最终发现,N4BP2就是那个手持利刃的“刺客”。
这种通常存在于细胞质中的酶,拥有进入破裂微核并切割DNA的独特能力。实验证据极具说服力:
这证实了N4BP2不仅仅是相关者,而是足以引发染色体灾变的充分条件。它将一条完整的染色体瞬间肢解,而细胞的修复系统在慌乱中只能将这些碎片胡乱拼接,最终制造出一个充满错误连接、基因缺失和异常扩增的“弗兰肯斯坦”式染色体,为癌细胞的恶性进化提供了海量的“原材料”。
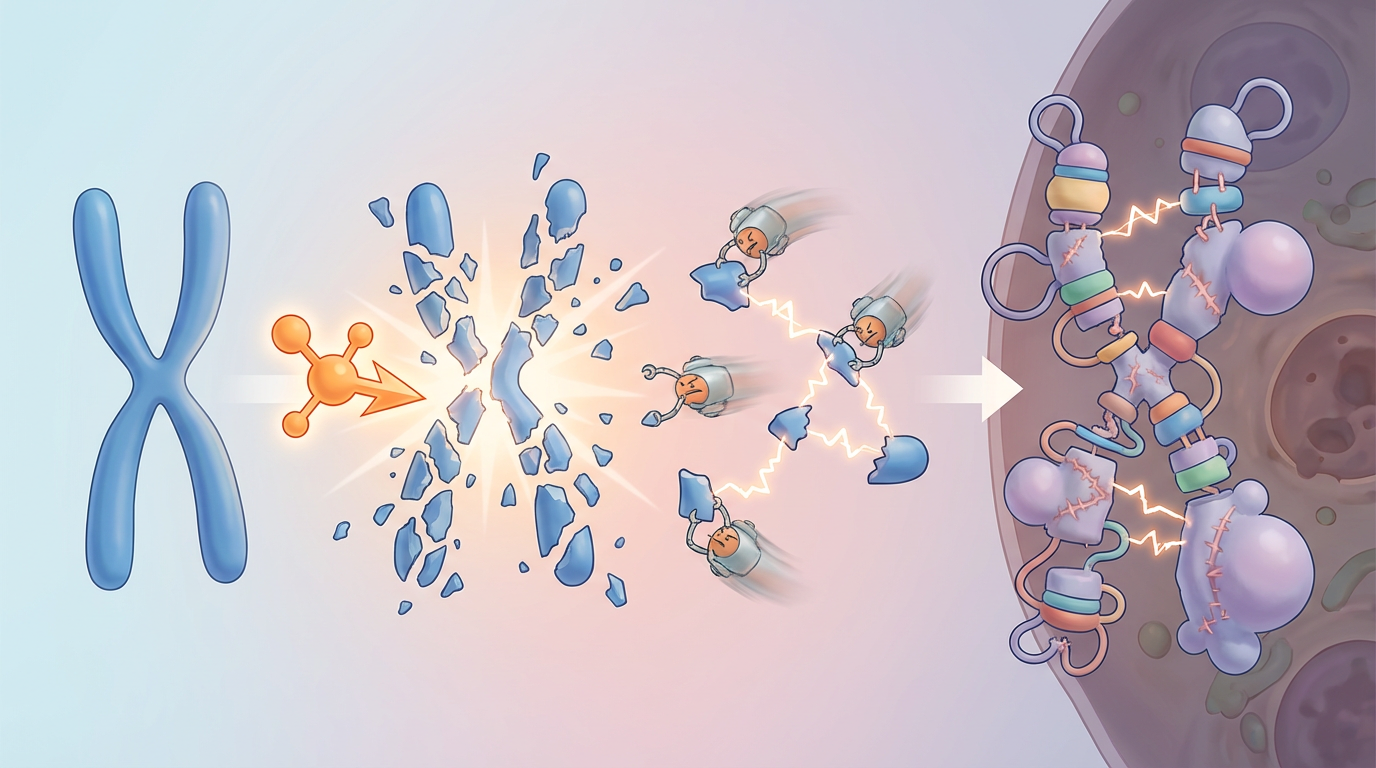
N4BP2的破坏力远不止于制造混乱的染色体。这场灾变的直接产物中,还诞生了癌症中最危险的“超级武器”之一——染色体外DNA(ecDNA)。
这些ecDNA是携带强力促癌基因(如MYC、EGFR)的环状DNA片段,它们像幽灵一样游离于染色体之外。它们之所以极其危险,原因有三:
这项新研究最关键的洞见在于,它明确指出,ecDNA并非一个孤立的现象,而是N4BP2所驱动的染色体灾变的直接下游产物。N4BP2正是这条通往癌症快速进化、耐药和复发的“毁灭之路”的起点。
锁定N4BP2,意味着科学家们终于找到了一个可以从源头阻止基因组混乱的潜在靶点。这一发现为未来的癌症治疗开辟了激动人心的新方向。
全新的治疗靶点:针对N4BP2开发特异性抑制剂,有望在癌细胞试图通过染色体灾变进行“基因重组”之前就将其扼杀在摇篮里。数据显示,N4BP2拷贝数高的肿瘤,发生染色体碎裂的风险增加了3.7倍,其预测能力甚至强于著名的抑癌基因TP53突变,凸显了其作为靶点的重要性。
与免疫疗法的协同潜力:N4BP2在细胞质中切割DNA产生的碎片,可能会激活细胞内的天然免疫信号通路(如cGAS-STING)。这条通路是人体的“火灾警报系统”,能够召唤免疫细胞前来攻击。因此,靶向N4BP2的药物,或许能通过增加细胞质中的DNA碎片,将免疫系统不识别的“冷肿瘤”转化为易于攻击的“热肿瘤”,从而增强免疫检查点抑制剂等疗法的效果。
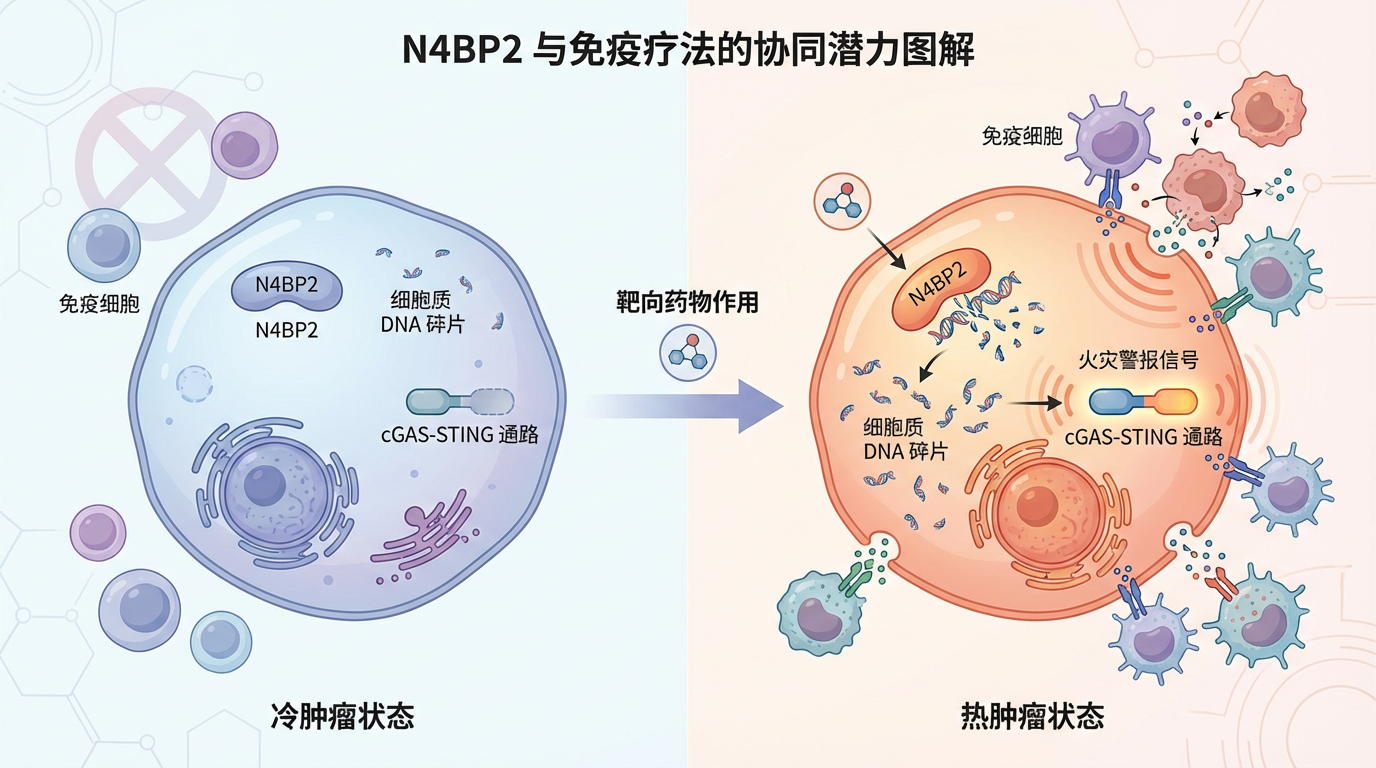
从观察到癌症基因组的极端混乱,到最终锁定其背后的分子“点火器”N4BP2,人类在对抗癌症的征途上又迈出了坚实的一步。这一发现不仅深刻揭示了癌细胞最核心的生存与进化策略,更重要的是,它将我们的目光从应对下游的“混乱后果”转向了干预上游的“混乱之源”。
理解敌人最狡猾的战术,是赢得战争的第一步。通过靶向N4BP2,我们或许将有机会为这场混乱的基因战争,重新引入秩序的曙光。