内容由AI生成,思考得你完成
App 下载
内容由AI生成,思考得你完成
App 下载
一管血,预见未来二十年的记忆风暴。这曾是阿尔茨海默病(AD)血液检测技术带给世界的承诺。这项革命性技术,通过捕捉血液中微量的β-淀粉样蛋白(Aβ)、tau蛋白等“大脑代谢废物”,有望将AD的诊断窗口提前15至20年,为早期干预赢得宝贵时间。当全球的目光都聚焦于这一巨大突破时,一则来自瑞典卡罗林斯卡医学院的最新研究,却像投入平静湖面的一颗石子,激起了层层涟漪。它揭示了一个被忽视的“盲点”:我们身体的“沉默过滤器”——肾脏,可能正在严重干扰我们对大脑发出的信号的解读。
2025年12月3日,顶级医学期刊《神经病学》(Neurology)发表了一项大规模研究,为这场诊断热潮敲响了警钟。由弗朗西斯卡·加斯帕里尼(Francesca Gasparini)博士领导的团队,对2279名平均年龄72岁的成年人进行了长达八年的追踪。研究结果出人意料:
这项研究清晰地指出,AD血液检测并非简单的“是”或“否”测试。医生在解读报告时,必须将大脑和肾脏这两个看似遥远的器官联系起来,否则,诊断可能失之毫厘,谬以千里。
要理解肾脏为何能“欺骗”AD检测,我们需要回归到最基本的生理学原理。AD的核心病理,是Aβ和tau蛋白在大脑中异常聚集,形成斑块和神经纤维缠结,毒害神经元。这些病理过程的“副产品”会少量泄漏到血液中,成为我们检测的生物标志物。
而肾脏,正是人体的终极净化系统。它的核心功能之一就是过滤血液,清除包括蛋白质代谢产物在内的各种废物。可以把它想象成一个精密的滤网。
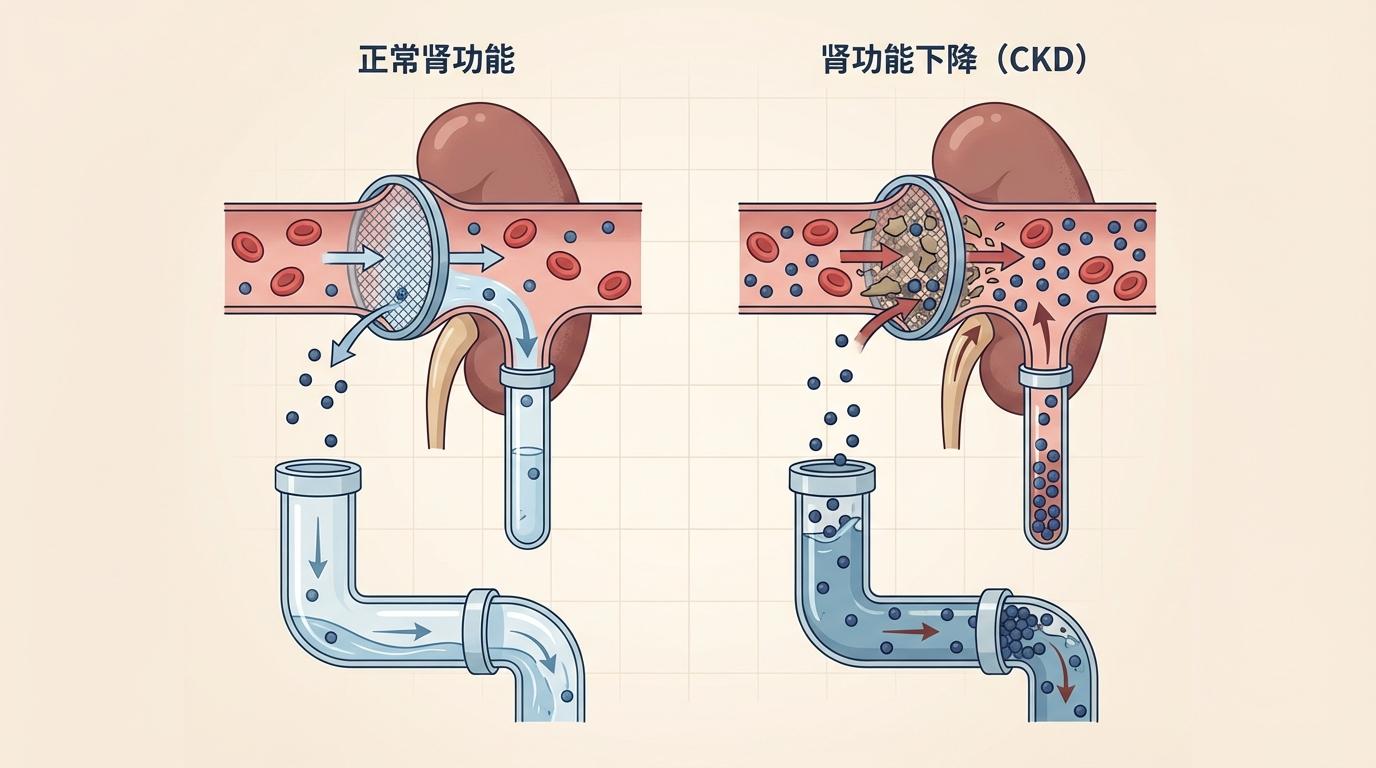
当肾功能正常时,这个“滤网”高效工作,及时清除血液中的AD标志物蛋白,使其维持在较低水平。而当肾功能下降(例如,在慢性肾病CKD患者中),“滤网”的孔隙被堵塞或效率降低,这些本该被排出的蛋白质便开始在血液中积聚。这就导致了血液检测到的浓度“虚高”,它反映的可能更多是肾脏的“失职”,而非大脑病变的真实程度。这个过程,就像一个堵塞的排水管导致水位异常上涨,但水源本身并未增加。
这一发现将AD的早期诊断推入了一场更复杂的“攻防战”,要求我们从多个维度重新审视这项技术。
科学角度:从“单一指标”到“综合评估”
肾脏的影响解释了研究中的核心悖论:为何指标高而总体风险不增加?因为指标的来源被混淆了。这提示我们,血液标志物的存在与它的病理意义之间,隔着一个“器官功能”的变量。尤其是NfL和GFAP这类反映神经损伤和炎症的标志物,它们并非AD所特有,在肾功能不全时,其清除率下降尤为明显。而肾脏问题本身也可能通过血管损伤、毒素累积等方式加重神经炎症,形成恶性循环。这种“双重打击”或许正是肾脏加速高风险人群发病的深层机制。
临床角度:误诊风险与新诊断流程的呼唤
这一发现对临床实践的冲击是巨大的。老年人是AD的高发群体,同时也是肾功能自然衰退或患有慢性肾病的高发群体。一个70多岁、患有中度肾功能不全的老人,很可能因为血液标志物“假性升高”而被错误地贴上“AD高风险”的标签。这不仅会带来巨大的心理负担,还可能导致一系列不必要的、昂贵的检查(如PET-CT扫描),甚至在未来被纳入不必要的药物治疗,造成资源浪费和潜在的副作用。
因此,未来的AD诊断流程必须升级。正如《2025年版慢性肾脏病与认知障碍专家共识》所强调的,在进行AD血液检测的同时,评估肾功能(如检测估算肾小球滤过率eGFR)应成为标准化操作。只有这样,医生才能剥离肾脏的“干扰”,看到大脑更真实的状况。
当然,加斯帕里尼博士的研究也存在局限性,例如生物标志物仅在研究开始时测量了一次,无法追踪其动态变化。此外,研究对象多为瑞典高教育水平人群,结论是否适用于其他族裔和地区仍需验证。
更重要的是,它留下了一系列亟待解答的关键问题:
挑战的出现,也催生了解决方案的探索。科学界已经开始行动,试图在复杂的生理噪音中,寻找到来自大脑的、更纯净的信号。
最终,这项关于肾脏的研究并非为了否定AD血液检测的价值,而是为其大规模临床应用扫清了障碍。它提醒我们,人体是一个精妙而复杂的整体,任何一个器官的失衡都可能引发连锁反应。在迈向精准医疗的道路上,真正的智慧不在于找到一个完美的工具,而在于深刻理解这个工具的适用边界,并以一种更全面、更人性化的视角,去解读生命发出的每一个复杂信号。