对抗知识焦虑,从看懂这条开始
App 下载
不用冷链的DNA折纸疫苗,要接棒mRNA了
纳米级精准设计|常温储存|哈佛团队|DNA折纸疫苗|DoriVac|新药研发|医学健康
2020年12月8日,第一支mRNA新冠疫苗注入人体,一年里它挡住了1440万条生命的逝去——这曾是人类对抗传染病的高光时刻。但高光背后的阴影从未消失:疫苗效力在半年后开始衰减,新变异毒株总能钻空子;超低温冷链像一道无形的墙,把非洲等地区的96%疫苗困在失效边缘。
现在,哈佛团队拿出了破局的答案:一种叫DoriVac的DNA折纸疫苗。它在小鼠和人体模拟实验里,激发出了和mRNA疫苗相当的抗体与T细胞反应,却能常温储存、制造更简单。更关键的是,它靠纳米级的精准设计,把免疫系统的激活效率拉到了新高度。
这不是小修小补的改良。这是疫苗设计逻辑的一次重构——为什么它能做到这些?
一张DNA折出来的疫苗“智能卡片”
你可以把DoriVac想象成一张30纳米见方的DNA小卡片——大概是头发丝直径的三千分之一。它的两面分工明确:一面用3.5纳米的精准间距,整齐排列着18个CpG佐剂分子;另一面则牢牢固定着病毒或肿瘤的抗原肽段。
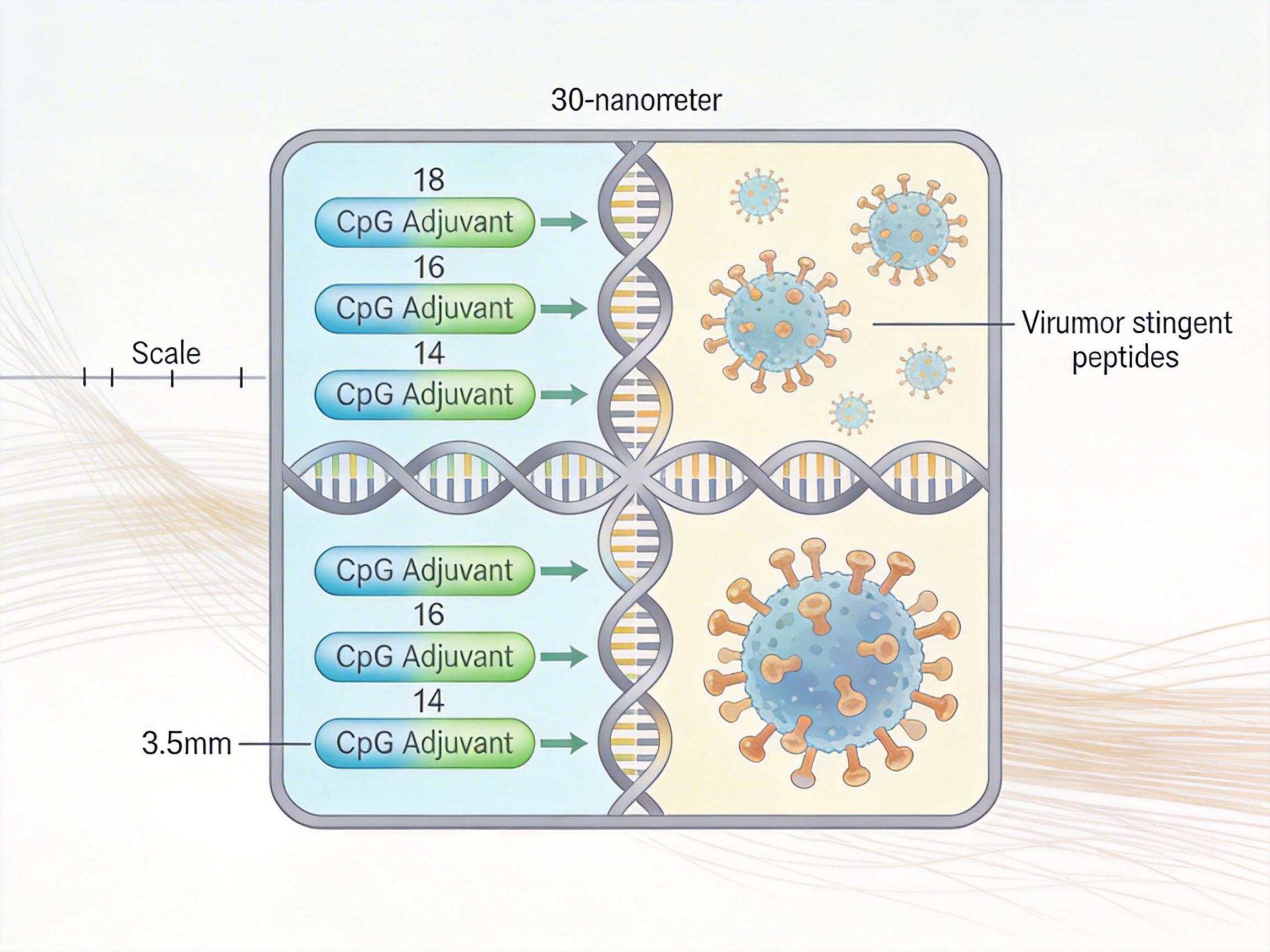
这个3.5纳米的间距是关键。免疫细胞里的TLR9受体,本来就需要凑成“小团体”才能高效激活,而天然病原体的CpG序列间距刚好是3.5纳米。DoriVac直接模拟了这个天然结构,让TLR9受体像被精准咬合的齿轮一样启动,把树突状细胞的激活效率提升了数倍。
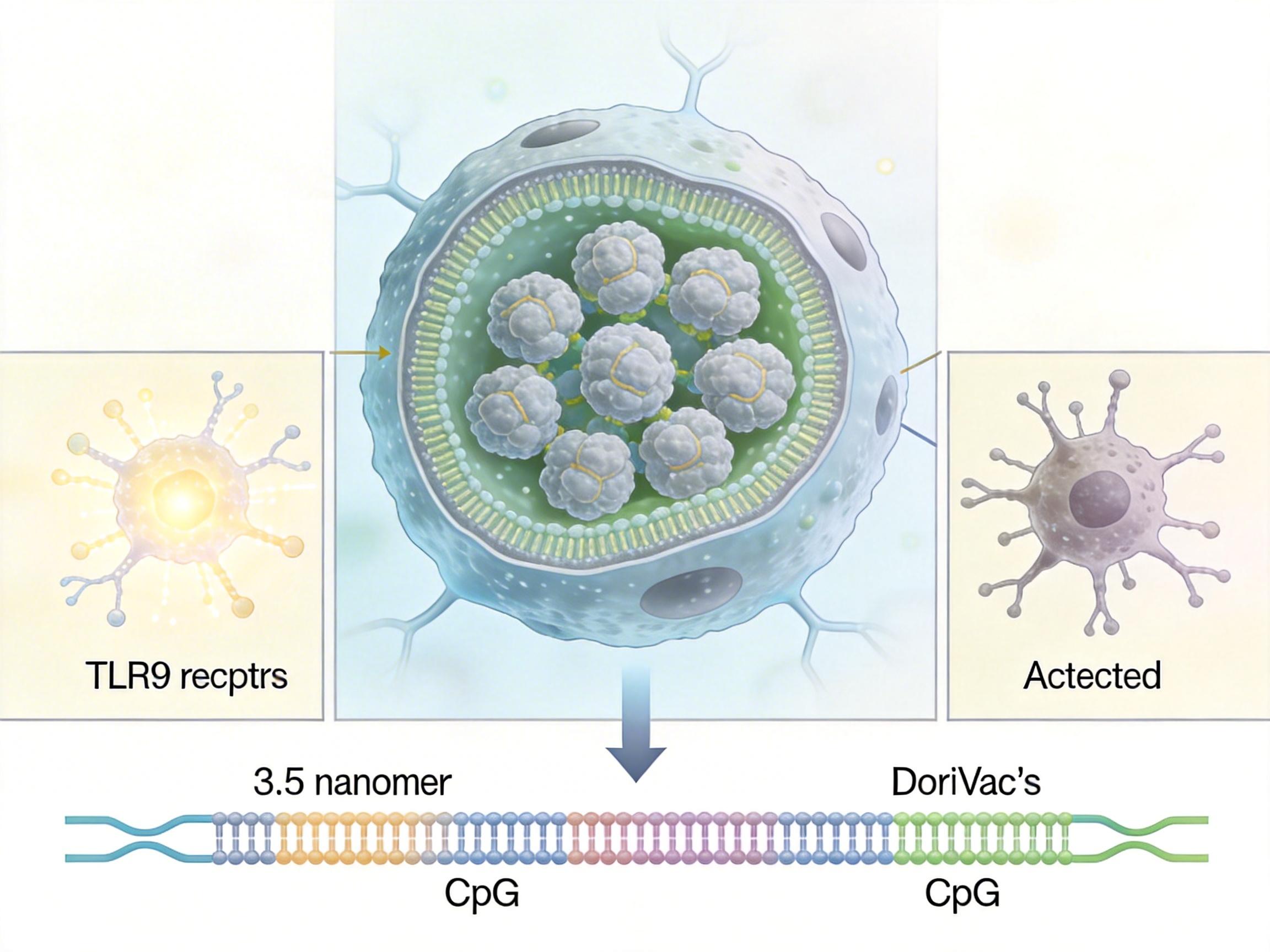
但真实的机制比这个类比更精确:
- DNA小卡片靠碱基互补配对自动折叠组装,不需要复杂的化学合成;
- 抗原肽通过无铜点击化学固定在卡片上,稳定且不会破坏活性;
- 整个结构在生理环境里能抵抗核酸酶降解,半衰期是游离CpG的10倍以上。
领导这项研究的曾杨(Claire Zeng)博士最初是为癌症免疫治疗开发这个平台,新冠疫情让她意识到,这套精准调控的逻辑,同样能解决传染病疫苗的痛点——尤其是那些靠变异躲避免疫的病毒。
从老鼠到“芯片人”的跨越
疫苗研发里最让人头疼的,就是老鼠身上的成功到了人身上可能全失效。哈佛团队这次跳过了传统的“动物实验→人体试验”的漫长试错,直接用上了Wyss研究所的人类淋巴结芯片——一个在微流控芯片上模拟出来的迷你人体免疫系统。
他们把DoriVac滴在芯片上,结果和小鼠实验里的反应高度吻合:人类树突状细胞表面的激活标记物CD86、MHC-II浓度翻了三倍,CD4+和CD8+ T细胞开始大量分泌干扰素-γ,甚至能产生针对新冠不同变异株的广谱抗体。
更直接的对比来自和mRNA疫苗的正面PK:在小鼠模型里,装载了完整新冠刺突蛋白的DoriVac,诱导出的中和抗体浓度、CD8+ T细胞数量,和辉瑞、莫德纳的mRNA疫苗不相上下。但DoriVac不需要-70℃的超低温冰箱,在25℃的室温下能稳定存放至少3个月,制造时也不用复杂的脂质纳米颗粒包裹——只要把DNA链放进缓冲液里加热冷却,它自己就会折成想要的形状。
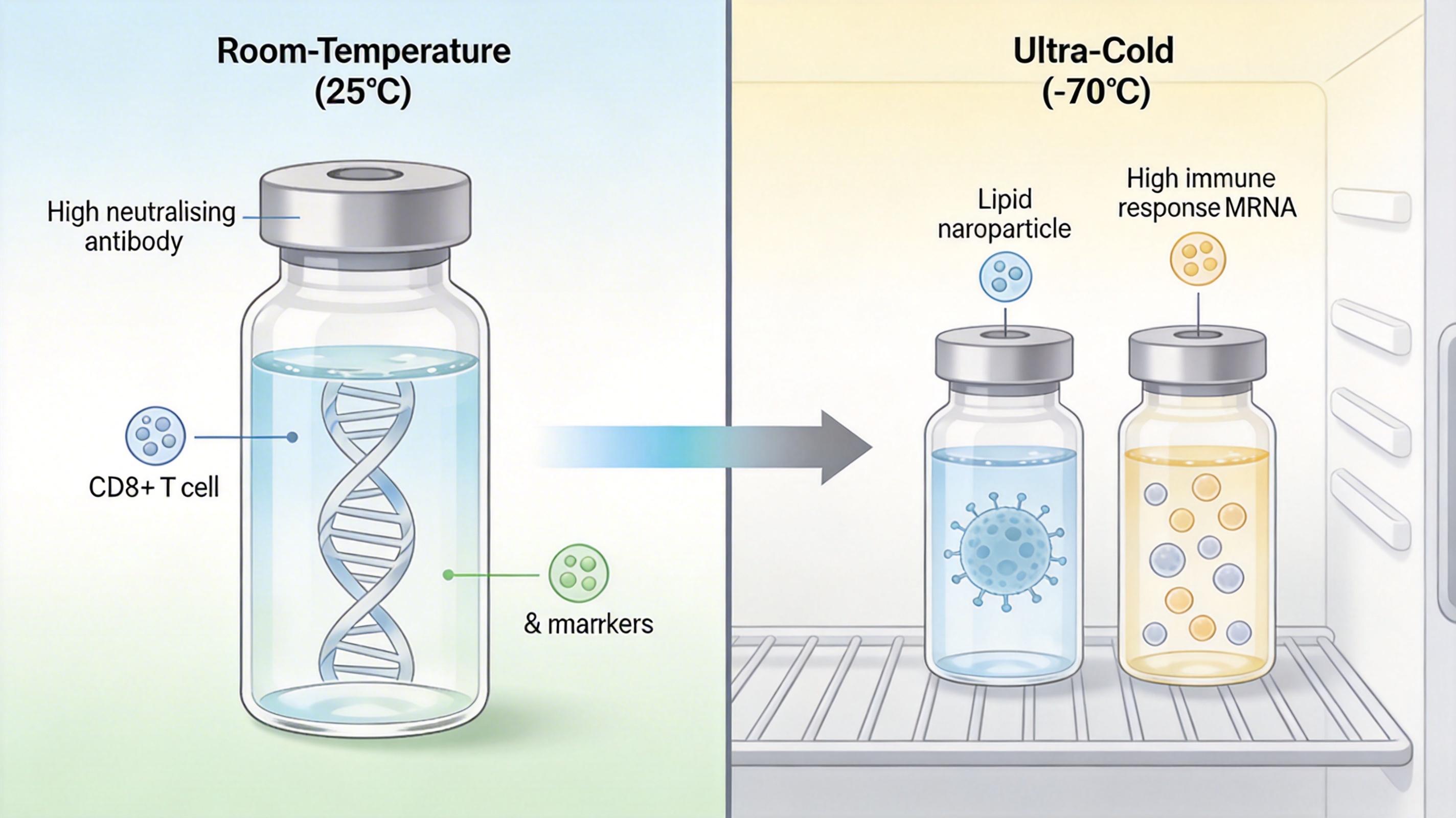
我认为,这才是DoriVac真正的革命性意义:它第一次把疫苗从“靠运气激活免疫”,变成了“按设计精准触发免疫”。以前我们是把抗原和佐剂混在一起“泼”给免疫系统,现在是拿着精准的分子钥匙,去开免疫细胞的特定门锁。
不止是新冠:从癌症到HIV的广谱潜力
DoriVac的野心远不止新冠。团队已经用它开发了针对HIV、埃博拉的疫苗,核心思路都是瞄准病毒里最保守的HR2肽段——这个区域是病毒膜融合的关键,几乎不会变异。
在HIV模型里,DoriVac诱导出的特异性T细胞数量,是传统疫苗的4倍以上;在埃博拉模型里,它能让小鼠的存活率从0提升到60%。更让人期待的是它在癌症治疗里的表现:把患者肿瘤的特异性新抗原装到DoriVac上,再和PD-1抑制剂联合使用,能让小鼠的黑色素瘤完全消退,并且形成长期免疫记忆——就算再注射肿瘤细胞,小鼠也能轻松清除。
当然,它也不是完美的。目前的大规模生产还面临成本问题:虽然DNA合成的价格每年都在降,但要做到和传统疫苗一样便宜,还需要更高效的合成技术。另外,长期的人体安全性数据还在积累,毕竟这是第一个进入临床前阶段的DNA折纸疫苗平台。
但这些都是技术迭代能解决的问题,而它带来的可能性是前所未有的:未来我们可能只需要一个DoriVac平台,就能快速定制出针对任何新病毒、任何肿瘤的疫苗,而且不需要冷链,能送到世界上任何一个角落。
当我们还在为mRNA疫苗的冷链问题头疼时,科学家已经在分子层面重新定义了疫苗的形态。DoriVac的出现,让我们看到了精准医学的另一种可能:不是用更复杂的技术去解决复杂的问题,而是用更精准的设计,把复杂的问题变得简单。
“免疫激活的本质,是分子空间的精准对话。”这句话或许能概括这项技术的核心。未来的疫苗,可能不再是一支支需要小心翼翼保存的液体,而是一张张能常温运输、按需定制的DNA卡片——它们带着人类对分子世界的理解,悄悄打开免疫系统的大门,在看不见的微观世界里,为我们筑起一道更坚固的防线。
而这,只是纳米技术和免疫学对话的开始。