
1 个月前

1 个月前
当一位被抑郁症纠缠十年、试过五种主流抗抑郁药都无效的患者,在静脉注射一剂氯胺酮后几小时内,突然说“我好像能看见窗外的花了”,医学家们既兴奋又困惑——这种原本用于麻醉的药物,为何能跳过传统抗抑郁药数周的起效期,直接“重启”情绪?这个问题悬了20年,直到2026年3月,日本横滨市立大学的团队用一项脑成像技术,第一次在活人的大脑里“看见”了答案:氯胺酮的秘密,藏在一种叫AMPAR的蛋白质的动态变化里。
要理解这个答案,得先搞懂AMPAR——这是大脑里负责神经细胞“传信”的关键蛋白质,就像神经元之间的“信号接收器”,谷氨酸这种神经递质一“敲门”,它就打开通道,让神经信号顺利传递,而突触可塑性(也就是大脑的“学习和适应能力”)全靠它调节。过去科学家只能在动物实验或死脑组织里研究它,活人脑中的AMPAR是怎么工作的,完全是个黑箱。
横滨团队解决这个难题的工具,是他们自己研发的PET示踪剂[¹¹C]K-2。你可以把它想象成一群带着“荧光标记”的微型探测器,注射进人体后,会精准绑定在神经细胞表面的AMPAR上,再通过PET扫描仪,就能给这些受体拍一张全脑的“3D密度图”。更厉害的是,他们还能在治疗前后各拍一次,直接对比AMPAR的变化——这是人类第一次在活体中动态追踪这种关键受体的活动。
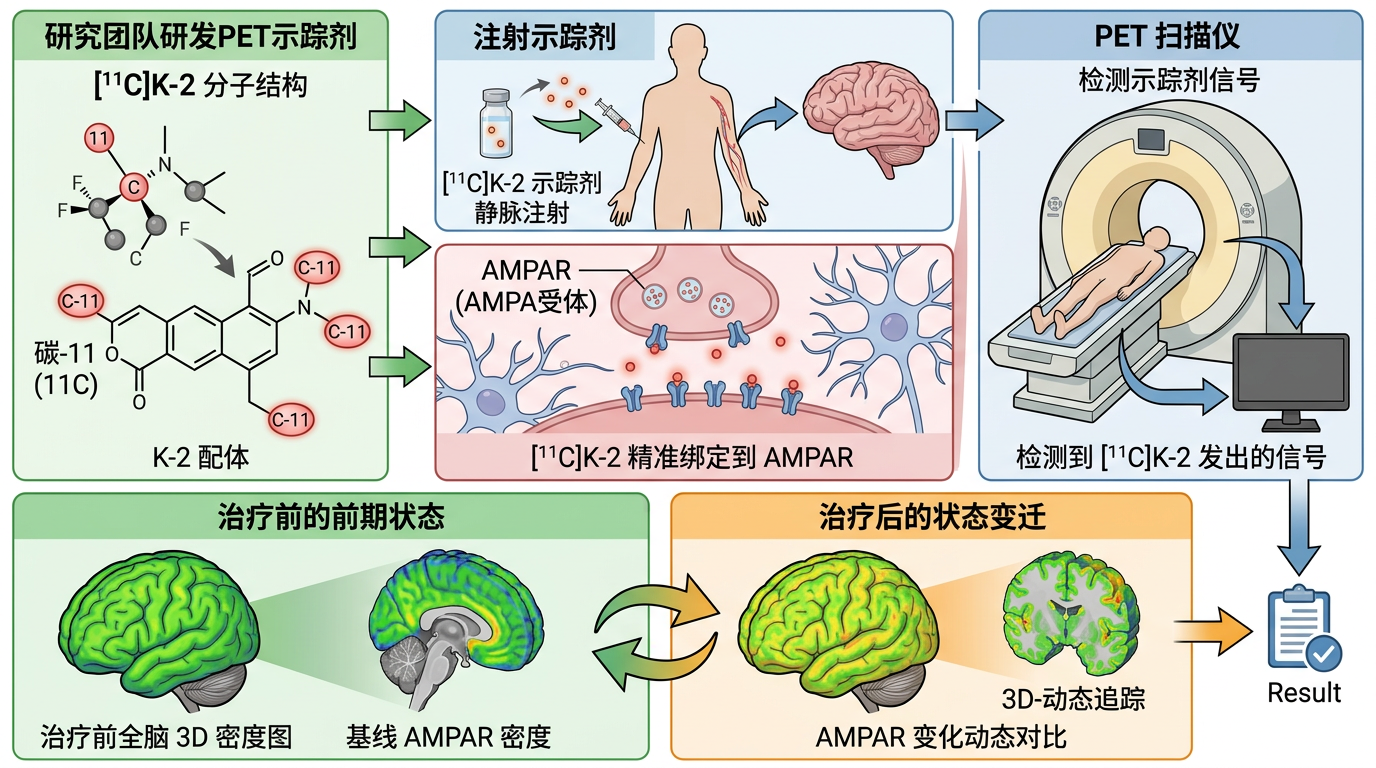
研究招募了34名难治性抑郁症患者和49名健康人,患者接受两周的氯胺酮静脉注射治疗。扫描结果的反差一目了然:治疗前,患者大脑的AMPAR分布就像一张被打乱的拼图——前额叶、顶叶这些管情绪和认知的区域,受体密度比健康人低一大截;而缰核这个“负面情绪放大器”区域,受体密度却异常偏高。
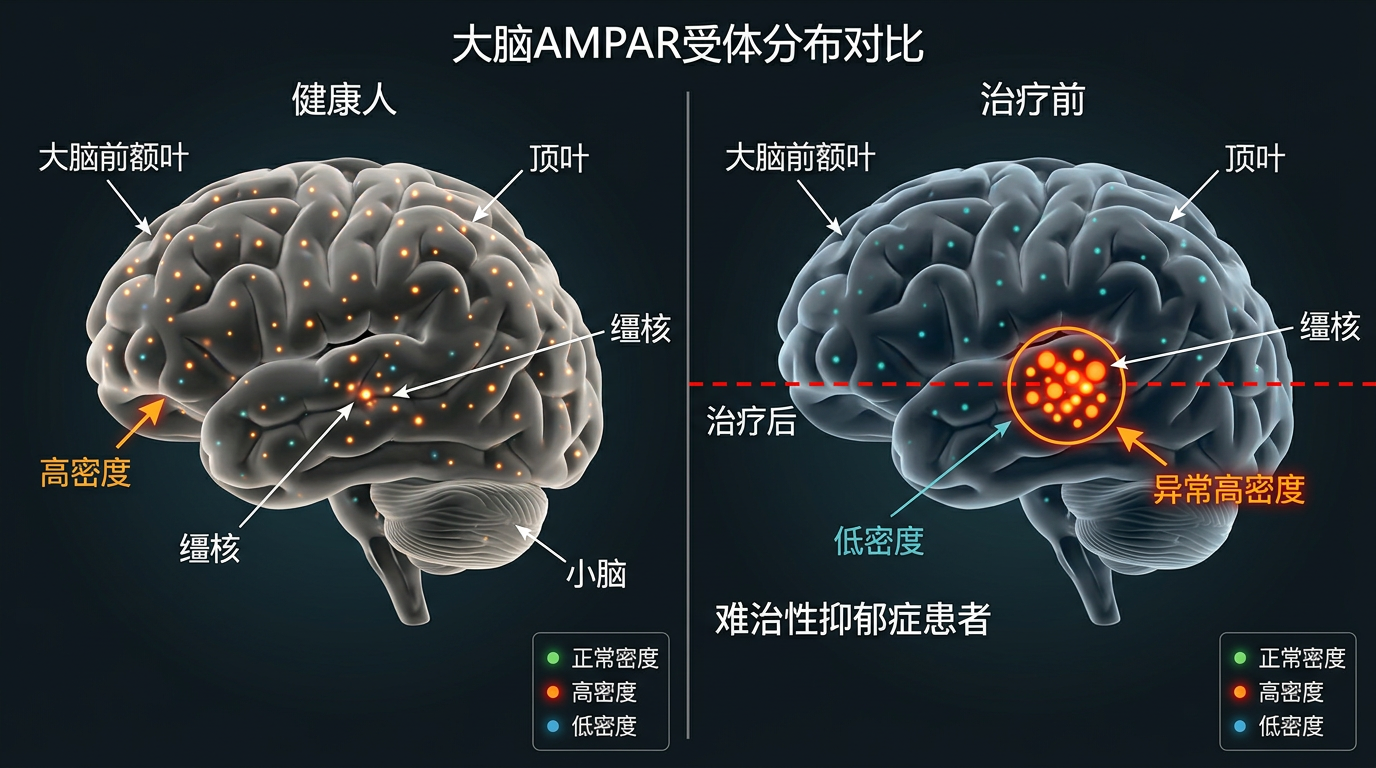
最关键的发现藏在治疗后的对比图里:氯胺酮没有像洒水一样给全脑“补”AMPAR,而是精准地做了“加减法”——
那些原本AMPAR不足的皮层区域,比如顶叶、枕叶和前额叶,受体密度显著上升,就像给信号接收器加了天线,神经细胞之间的信息传递重新变得顺畅。而缰核区域的AMPAR密度明显下降,相当于给过度活跃的“负面情绪放大器”调低了音量。
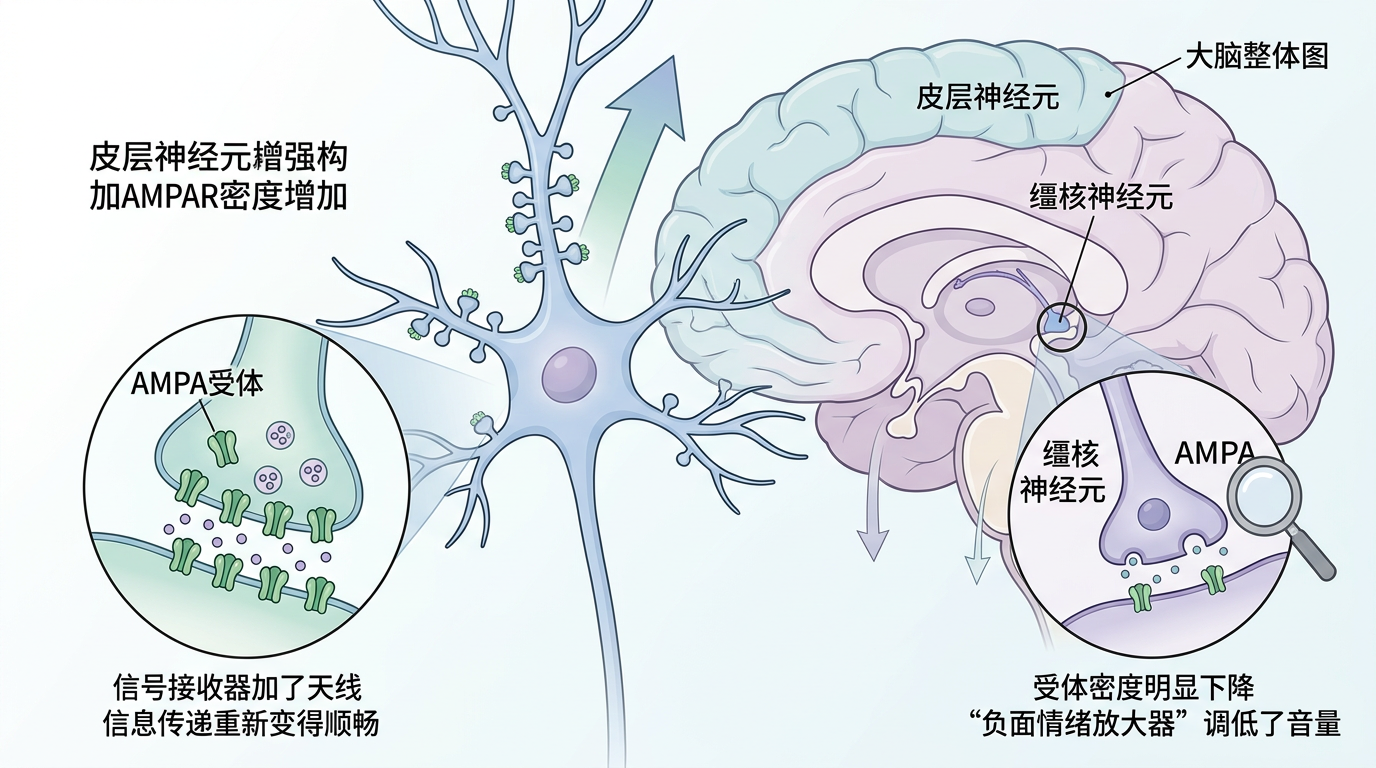
更重要的是,这些变化和患者的症状改善完全同步:皮层AMPAR密度越高,抑郁量表的评分降得越多;缰核的AMPAR降得越明显,患者的快感缺失、绝望感缓解得越彻底。安慰剂组的患者则没有出现这种针对性的变化,彻底排除了心理暗示的可能。
我认为,这是这项研究最被低估的价值:它打破了“氯胺酮只是简单兴奋大脑”的误解,证明它是在精准修复抑郁症患者失衡的神经回路——就像给一台某个零件过载、某个零件缺油的机器,做了一次定向的调试,而不是粗暴地按下重启键。
这项发现的意义,远不止于搞懂氯胺酮的原理。
首先,它给难治性抑郁症的治疗带来了“精准预测”的可能。未来医生可以在治疗前给患者做一次AMPAR PET扫描,如果发现患者皮层AMPAR不足、缰核AMPAR过度活跃,那么氯胺酮治疗的有效率会大大提高;反之,可能就需要换其他疗法。这能帮患者避开无效治疗的痛苦,也能节省医疗资源。
其次,它给新型抗抑郁药的研发指明了方向。既然AMPAR的动态调节是关键,科学家就可以开发专门针对AMPAR的药物——比如只在皮层区域增强AMPAR活性,同时抑制缰核的AMPAR,这样既能达到氯胺酮的快速抗抑郁效果,又能避免氯胺酮可能带来的解离、成瘾等副作用。目前已经有类似的AMPAR正向调节剂进入临床试验,比如TAK-653,初步显示出不错的安全性和抗抑郁效果。
当然,挑战依然存在:[¹¹C]K-2的半衰期只有20分钟,必须在有回旋加速器的机构才能使用,很难普及到普通医院。不过团队已经开发出半衰期更长的[¹⁸F]K-40示踪剂,未来有望让更多患者受益。
抑郁症曾被看作“心灵的感冒”,但现在我们知道,它更是大脑神经回路的“故障”——不是简单的“想不开”,而是神经细胞的信号传递出了实实在在的问题。
氯胺酮的故事,是一个从“意外发现”到“精准破解”的科学旅程。它让我们第一次在活人的大脑里,看见抑郁症的“病根”,也看见治疗如何精准地修复这些病根。情绪的开关,原来藏在蛋白质的动态变化里。
未来的精神医学,或许不再是“试错式”的开药,而是像修机器一样,先给大脑做一次“精准体检”,再针对性地调试每一个出问题的零件。而这一切的起点,正是我们终于“看见”了那些藏在大脑深处的、决定着我们喜怒哀乐的微小蛋白质。
点击充电,成为大圆镜下一个视频选题!