对抗知识焦虑,从看懂这条开始
App 下载
失明25年靠一针复明,基因疗法做到了
FDA批准疗法|简·贝内特|遗传性失明|基因增强疗法|RPE65基因突变|眼科学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
FDA批准疗法|简·贝内特|遗传性失明|基因增强疗法|RPE65基因突变|眼科学|医学健康
当12岁的科里第一次在深夜认出路边的路牌时,没人会想到,这束迟到的光,来自25年前一堂解剖课上的偶然。宾夕法尼亚大学的简·贝内特教授在那次解剖中注意到眼科遗传病的隐秘逻辑,从此踏上了一条从实验室到临床的漫长旅程——直到她和团队研发的基因增强疗法拿下“科学界奥斯卡”,成为首个获FDA批准的遗传性失明治疗方案,让上千名像科里一样的患者重新看见世界。这不是科幻电影的桥段,而是发生在当下的医学奇迹,可它究竟是如何在黑暗里“种”出光的?
要理解这项疗法,得先搞懂遗传性失明的根源:像RPE65这样的基因突变,会让视网膜里的“视觉加工厂”停工——负责把光信号转化为神经信号的蛋白彻底失效,眼睛就成了没装芯片的摄像头。贝内特团队的解法,是用一种经过改造的腺相关病毒当“快递员”,把正常的RPE65基因打包,通过视网膜下腔注射送进患者眼里。这个病毒就像一把精准的钥匙,只会打开视网膜色素上皮细胞的门,不会打扰其他组织,更不会引发剧烈免疫反应。
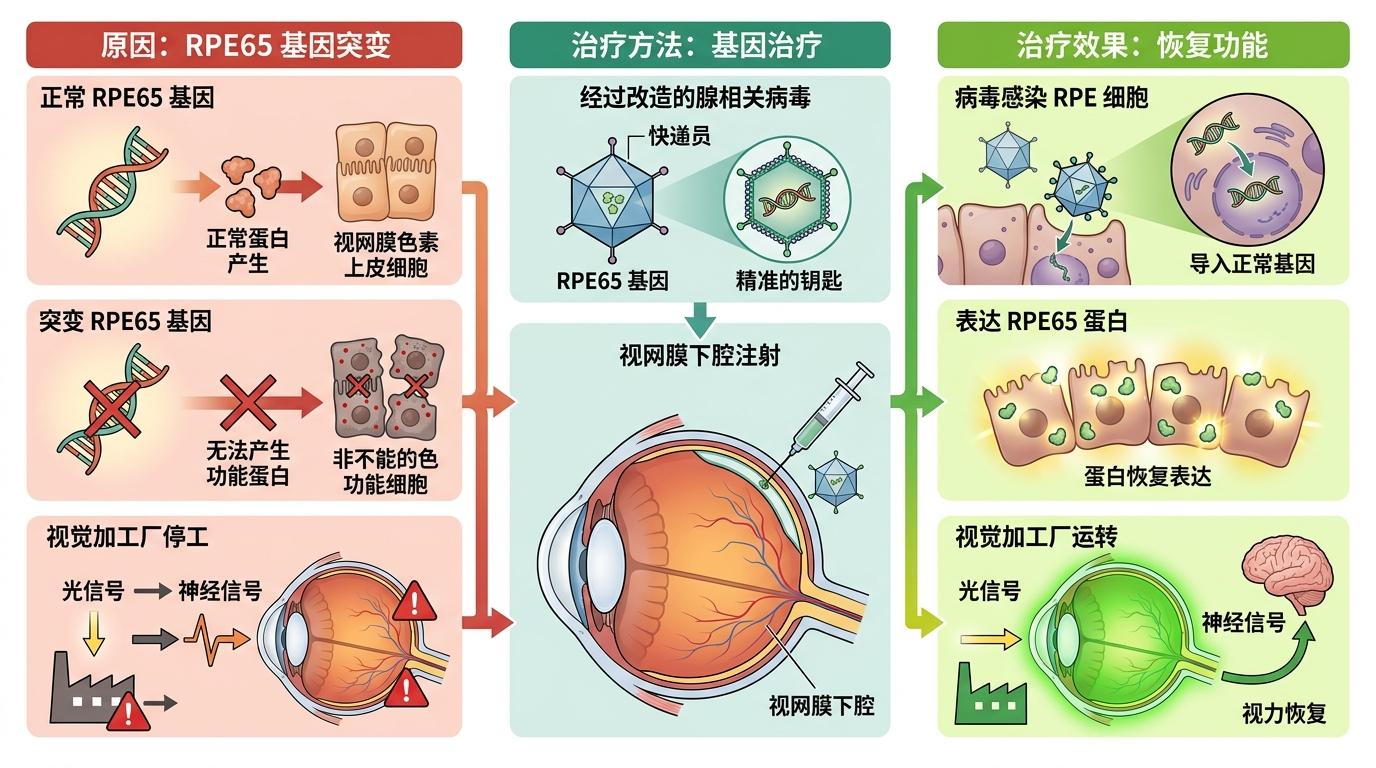
你可以把整个过程想象成给故障的灯泡换灯丝:不用换掉整个灯座,只要把好的灯丝送进去,就能重新点亮。更准确地说,正常基因进入细胞后,会指导合成能工作的视觉蛋白,修复被打断的光信号通路,让原本“罢工”的视网膜重新开始处理光信息。临床试验里,72%的患者在低光环境下的导航能力显著提升,有人甚至能第一次看清家人的脸——这种改变不是暂时的,随访四年后,疗效依然稳定。
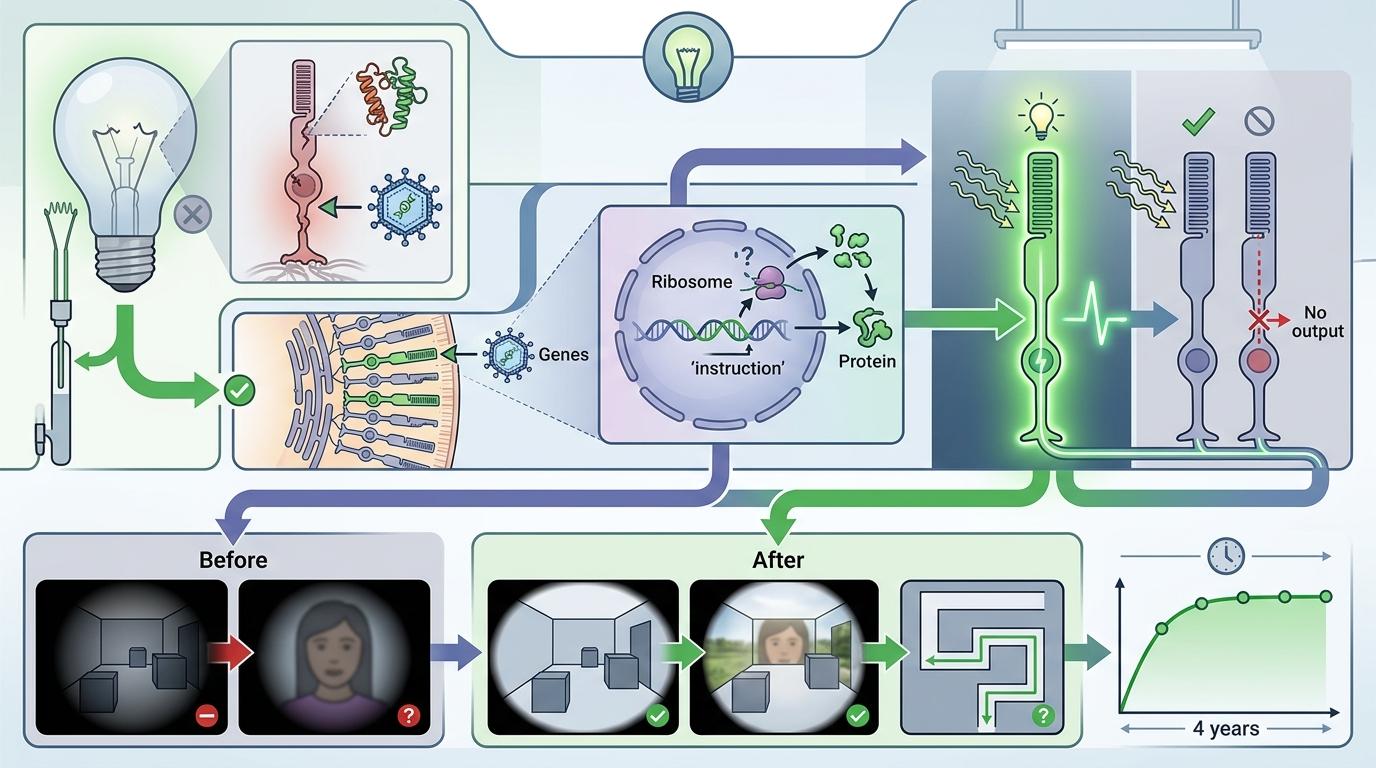
但我们必须清醒地看到,这项突破并非完美的“万能钥匙”。它只适用于还有存活光感受器细胞的患者,那些视网膜已经完全退化的晚期患者,暂时还无法从中获益。更现实的是,单眼治疗几十万到上百万美元的费用,让它像一件昂贵的奢侈品,绝大多数患者还难以触及。贝内特团队主动放弃经济利益的选择固然令人敬佩,但如何让这样的疗法从“少数人的希望”变成“多数人的福利”,才是更值得关注的命题。
从实验室里的小鼠模型,到犬类试验的成功,再到人类患者的复明,这25年的研究不仅点亮了黑暗中的眼睛,更照亮了基因疗法的未来。它让我们意识到,曾经被视为“绝症”的遗传病,或许只是等待被精准修复的“程序bug”。而真正的光明,从来不是某一项技术的突破,而是让每一个渴望看见的人,都能平等地握住那束光。
科技的终极意义,从来不是突破极限,而是让每个生命都能被温柔照亮。