对抗知识焦虑,从看懂这条开始
App 下载
困死癌王的新钥匙:锁定活跃态RAS突变
生存期延长|蛋白结构|口服药|RAS突变|胰腺癌|肿瘤学|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
生存期延长|蛋白结构|口服药|RAS突变|胰腺癌|肿瘤学|医学健康
当医生告诉你“胰腺癌晚期”,过去意味着平均只剩6.7个月的生存期——这是一种把五年生存率压到13%的“癌王”,90%的患者体内都带着驱动肿瘤疯长的RAS突变,却被医学界卡了几十年:因为这个突变的蛋白结构光滑得像颗台球,找不到下嘴的“药物口袋”。直到2026年4月,一组数据砸开了僵局:一款口服药把晚期患者的中位生存期拉到了13.2个月,死亡风险直接砍半。更关键的是,它瞄准的正是那个曾被判定“不可药物化”的RAS突变,而且是盯着它最嚣张的活跃状态下死手。这到底是怎么做到的?
你可以把正常的RAS蛋白想象成家里的电灯开关:结合GDP时是“关”,细胞安分生长;结合GTP时是“开”,细胞开始分裂。但胰腺癌患者体内的RAS突变,会把这个开关焊死在“开”的位置——它失去了水解GTP的能力,永远处于活跃的GTP结合态,不断给细胞发“疯长”的指令。
过去的药物都在盯着“关”态的RAS下手,就像试图把已经关上的灯再按一遍,对焊死在“开”态的突变蛋白毫无办法。而这款口服药的思路完全相反:它直接扑向处于“开”态的RAS蛋白,还拉来一个叫环孢素A的“帮手”,三者形成一个稳定的三元复合物——相当于在已经打开的开关上,额外加了一把锁,彻底卡死它和下游效应蛋白的结合路径。
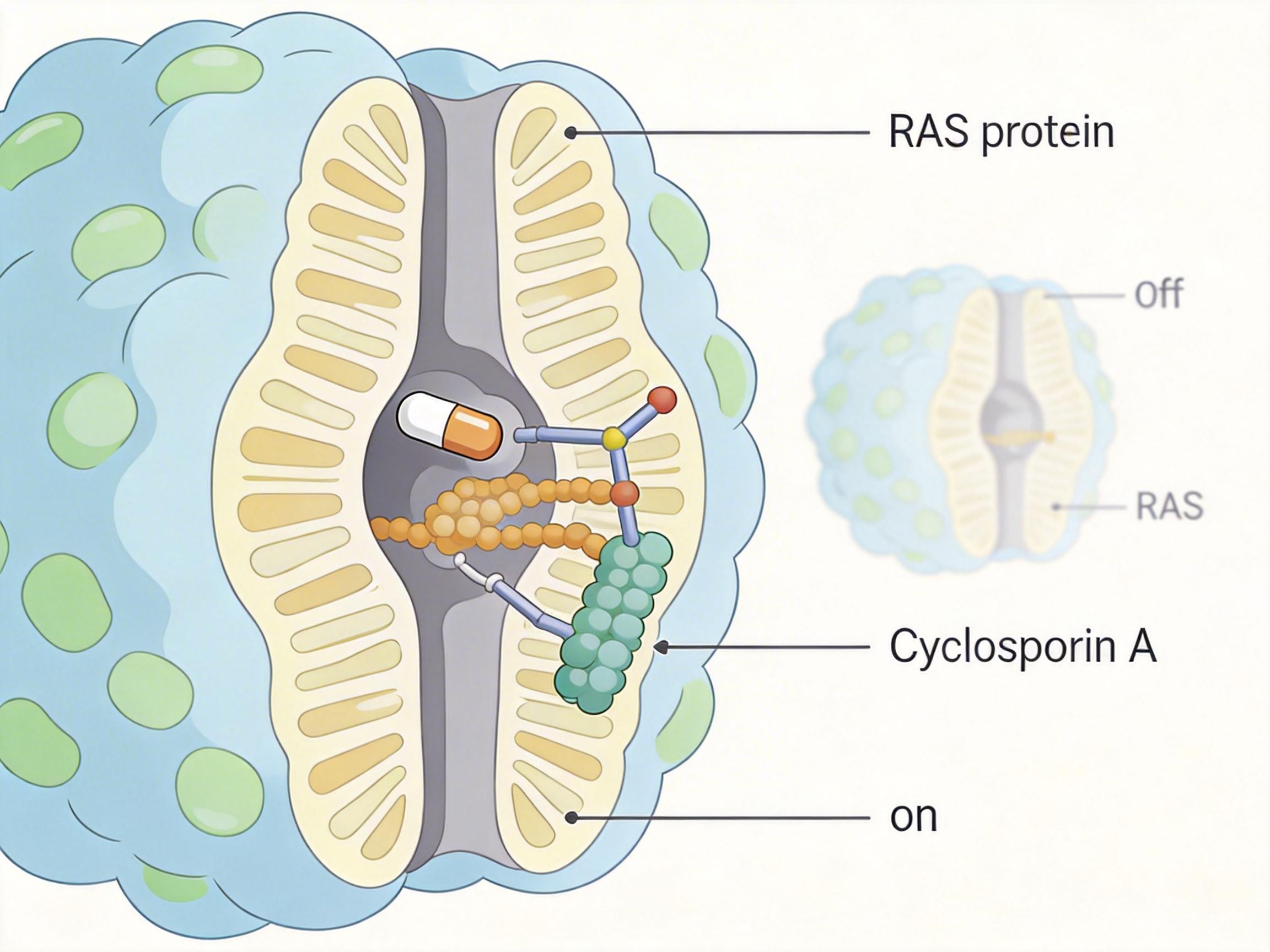
直给补刀:它能覆盖KRAS G12D、G12V、Q61X等多种胰腺癌高发的突变亚型,而不是只针对占比1%-2%的G12C突变。临床数据显示,300mg每日剂量下,RAS突变胰腺癌患者的中位无进展生存期达到8.5个月,疾病控制率超过90%——这是过去化疗连想都不敢想的数字。
胰腺癌的恶,不止在于RAS突变驱动的疯长,更在于它给自己搭了一层密不透风的“免疫防火墙”:肿瘤周围堆满了纤维化基质和免疫抑制细胞,免疫细胞根本冲不进去。但这款药的作用不止于直接锁死RAS信号。
临床前研究显示,它能显著降低肿瘤微环境里的免疫抑制细胞比例,同时提高趋化因子的水平——相当于在防火墙里炸开了几个缺口,把外周的CD8+T细胞招进肿瘤内部。更有意思的是,它还能让肿瘤细胞表面的抗原呈递分子表达量上升,相当于逼着癌细胞把自己的“通缉令”举得更高,方便免疫细胞识别追杀。
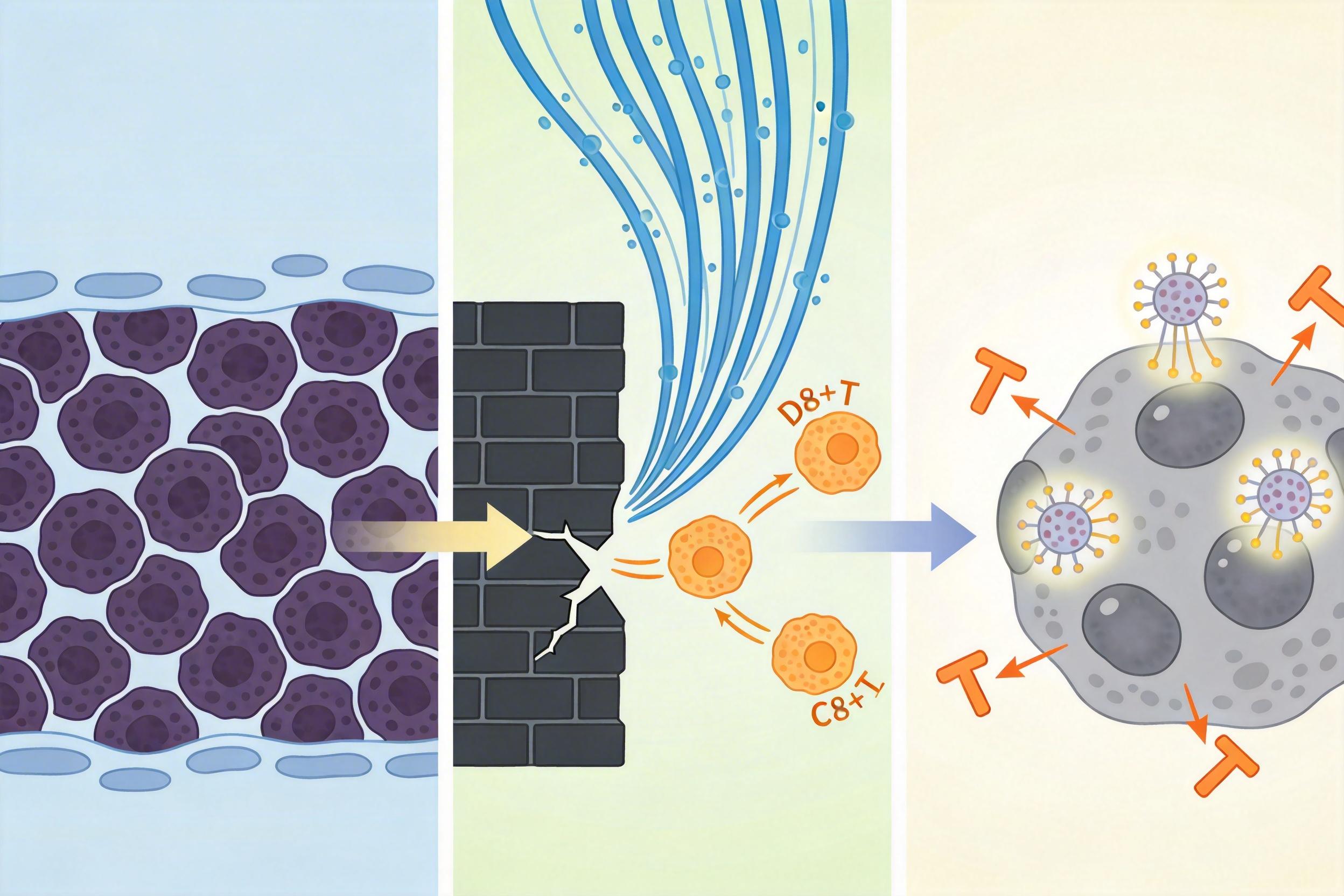
但它也不是无懈可击。目前的III期数据只覆盖了二线治疗,也就是已经经历过其他治疗失败的患者;而且耐药问题依然存在:部分患者会出现KRAS二次突变,或者激活其他旁路信号通路绕开抑制。更值得关注的是,它的皮疹副作用虽然可控,但在部分患者身上可能影响生活质量——这也是所有靶向RAS药物的共性问题。
单一靶向药的天花板显而易见,研究者们已经在推进联合治疗的试验:比如和化疗药物吉西他滨联合,或者和免疫检查点抑制剂搭档。在胰腺癌小鼠模型里,这款RAS抑制剂联合PD-1抗体的方案,让肿瘤完全消退的比例大幅提升,而且疗效维持时间更长。
还有一个方向是针对耐药机制的“精准补漏”:比如针对KRAS二次突变的Y64位点,开发新一代的抑制剂;或者联合抑制RAF二聚化的药物,堵死下游信号的逃逸路径。目前,针对一线治疗的III期试验已经启动,如果数据达标,它将能更早地介入胰腺癌治疗,给更多患者争取手术机会。
不过,距离真正改写胰腺癌的治疗格局还有一段路要走:它的价格可能会非常昂贵,而且需要伴随基因检测来筛选合适的患者——这在医疗资源不足的地区可能会成为普及的障碍。
从1982年发现RAS突变是胰腺癌的驱动因子,到终于找到能精准锁定活跃态RAS的药物,医学界花了整整44年。这不仅仅是一款新药的诞生,更像是给所有被“不可药物化”难题困住的研究者打了一针强心剂:再光滑的“台球”,只要盯着它最关键的动态,总能找到破绽。
“与其等开关关上,不如给开着的锁加栓。”这句话不仅是这款药的研发逻辑,更像是对所有医学难题的回应——有时候,困住我们的不是问题本身,而是我们默认的解题思路。未来的胰腺癌治疗,或许会在一个又一个这样的思路突破里,慢慢把“癌王”的标签撕下来。