
3 个月前

3 个月前
人体内的造血干细胞,如同一个永不停歇的生命工厂,日夜不息地生产着红细胞、白细胞和血小板,维持着生命的运转。然而,随着岁月流逝,这个精密工厂的生产线也不可避免地会出现一些微小的“差错”——基因突变。这些突变悄然累积,让一部分干细胞获得了微弱的生长优势,开始“违规”地加速分裂,形成一个个克隆军团。
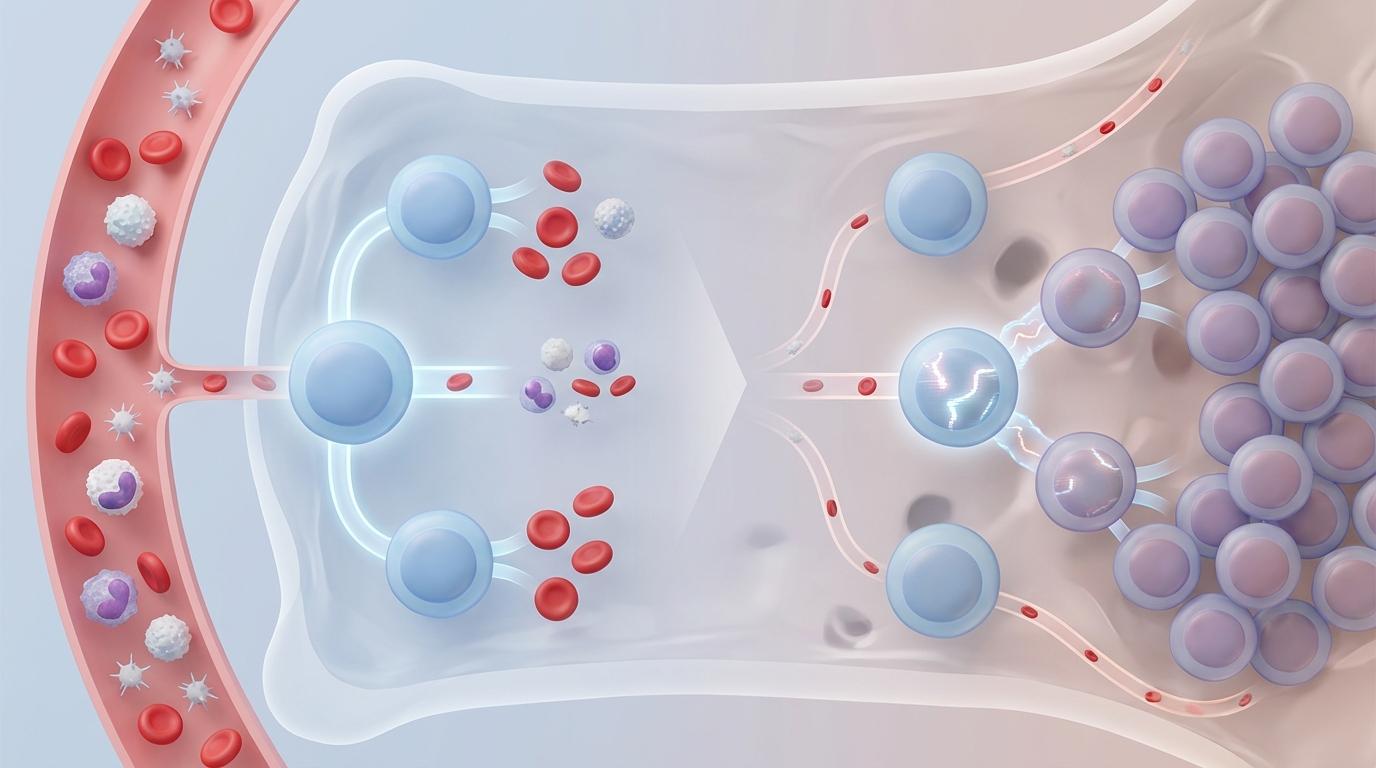
这种现象被称为“潜能未定的克隆性造血”,简称CHIP。它像一个深刻的“衰老印记”,潜伏在许多中老年人的血液中。数据显示,在70岁以上的人群中,高达10%至20%的人体内都存在着这样的克隆细胞。大多数时候,它们与我们相安无事。然而,在少数人身上,这些克隆细胞会进一步演变,最终引爆一颗致命的“定时炸弹”——白血病等血液癌症。CHIP携带者患上血癌的风险比普通人高出3到5倍。
一个长期困扰科学界的谜题是:为何同样携带CHIP,有些人的命运走向了癌症,而另一些人却能安然无恙?这背后,究竟是纯粹的运气,还是隐藏着更深层的生物学密码?
最近,一项发表在顶级期刊《科学》上的研究,为解开这个谜题带来了一线曙光。由波士顿儿童医院和博德研究所的科学家维杰·尚卡兰(Vijay Sankaran)领导的团队,通过分析英国生物银行(UK Biobank)等大型数据库的基因组数据,发现了一个惊人的秘密:一种特定的遗传变异,如同一个天生的“护身符”,能够显著降低CHIP进展为血癌的风险。
这项研究的核心发现直指一个名为**Musashi2(MSI2)**的蛋白质。研究人员发现,那些天生携带一种能降低体内MSI2蛋白水平的遗传变异的人,似乎对血癌有着更强的抵抗力。
这一发现之所以意义重大,是因为它不仅揭示了CHIP演化过程中的一个关键角色,更重要的是,它指明了一条全新的、可被干预的路径,为开发预防血癌的药物打开了一扇前所未有的大门。
MSI2蛋白究竟扮演着什么角色?在正常的造血干细胞内,MSI2像一个细胞生长的“油门”或“放大器”。它的主要工作是与细胞内编码生长相关蛋白的信使RNA(mRNA)结合,稳定这些mRNA,从而让细胞能够制造出更多的生长蛋白,驱动细胞增殖和自我更新。
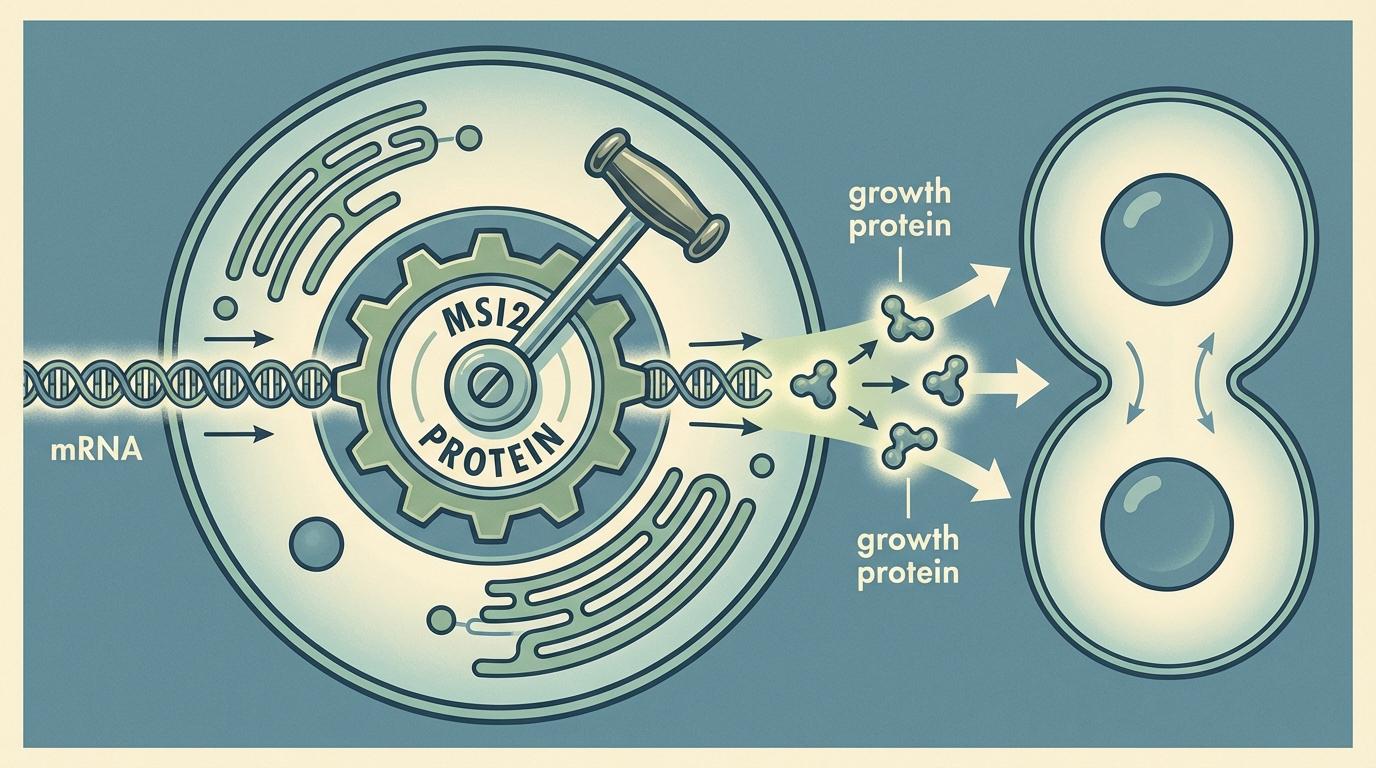
而癌细胞的疯狂增殖,正是利用并放大了这种自我更新机制。当CHIP克隆中的细胞获得突变后,它们本就有了更强的生长倾向。如果此时MSI2这个“油门”还被踩得很深,无疑会助长它们的扩张。
而这项研究中发现的保护性遗传变异,其作用恰恰是降低了MSI2的水平。尚卡兰将其比作“给细胞的自我更新踩下了刹车”。当“油门”松开,“刹车”介入,即使某些细胞获得了驱动突变,它们想要肆意扩张的势头也会被有效遏制。这就像一辆有故障但刹车灵敏的汽车,即便引擎偶尔失控,也不容易酿成大祸。
长期以来,临床上发现CHIP后,能做的非常有限,大多是定期监测,眼睁睁看着风险数字的变化,却无力干预。CHIP不仅与血癌相关,它还是心血管疾病、慢性肾病等多种老年疾病的独立风险因素,是一个系统性的健康警报。
MSI2的发现,标志着我们对CHIP的认知进入了一个新时代。德克萨斯大学MD安德森癌症中心的肿瘤学家高桥浩一(Koichi Takahashi)博士评价称,这项发现是“开创性的”,它让“精准肿瘤学”的概念从治疗延伸到了预防。
这意味着,未来我们或许不再只是被动地观察CHIP的发展。科学家们可以着手研发能够模拟这种保护性变异效果的药物——MSI2抑制剂。通过药物手段主动“踩刹车”,就有可能阻止甚至逆转高危CHIP克隆的癌变进程,将血癌扼杀在摇篮之中。
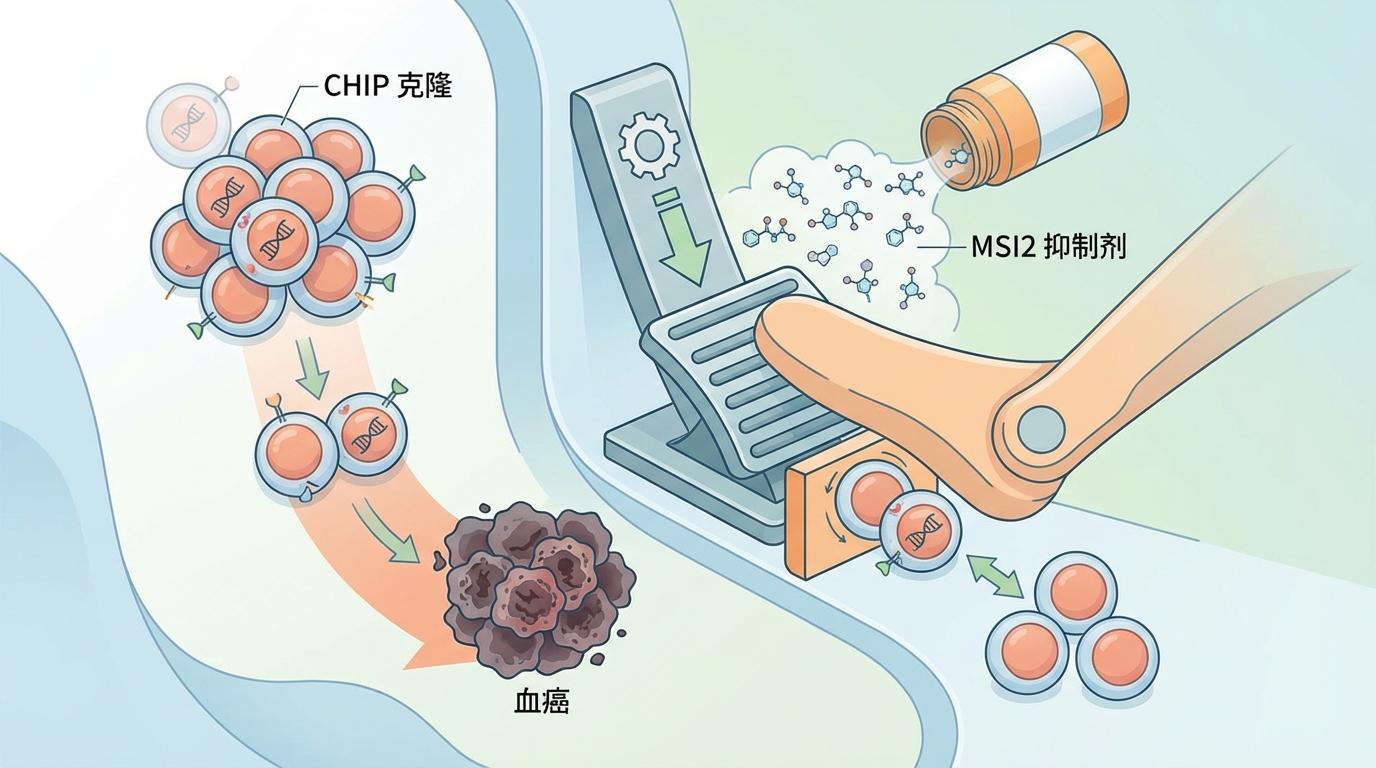
然而,通往新疗法的道路并非一帆风顺。这个“护身符”也并非完美无瑕。研究同时发现,携带这种保护性变异的人,其整体血细胞计数会略低于常人。这提示了一个潜在的风险:人为降低MSI2水平来预防癌症,可能会带来轻微的出血或感染风险增加。
这正是未来药物研发必须面对的核心挑战:如何精准地找到一个治疗窗口?既要能有效抑制癌前克隆的生长,又不能过度影响正常的造血功能。
对于不同风险的CHIP携带者,这种利弊权衡的考量也会不同。对于那些携带高危突变(如TP53突变),未来5到10年内患癌风险高达60%的个体而言,承受一定程度的治疗副作用,来换取“拆除”体内这颗“定时炸弹”的机会,或许是完全可以接受的选择。
尚卡兰团队的研究,为我们描绘了一个激动人心的未来。它将CHIP从一个与衰老相关的、似乎无法改变的风险状态,转变为一个具有明确分子靶点、有望被干预的临床前病变。
这不仅仅是一项关于血癌的研究,它更象征着现代医学在对抗癌症上的理念转变——从被动治疗,走向主动预防。通过深入解码生命的遗传密码,我们正一步步学会如何识别风险、预测未来,并最终在疾病萌芽之初就精准地介入。血液中的“衰老印记”或许无法抹去,但我们正获得前所未有的能力,去改写它最终的结局。
点击充电,成为大圆镜下一个视频选题!