
11 天前

11 天前
我坐在自家沙发上看着护士抽走两小管血,冰袋裹着的样本将被送去实验室——这管血要查50多种癌症。800多美元的花费,一周出结果,我明明没症状、没家族史,离推荐筛查年龄还早10年,胃里却翻起了浪。
这是当下火遍硅谷的多癌种早筛血液检测:从血液里抓肿瘤的蛛丝马迹,把癌症扼杀在萌芽里。可等待结果的那两周里,我才后知后觉:我们对癌症的恐惧,已经让愿意为“可能性”买单的人越来越多,但这管血里的真相,真的如想象中清晰吗?
你可以把血液早筛想象成在装满清水的泳池里找几根掉进去的头发——这根“头发”就是循环肿瘤DNA(ctDNA),是肿瘤细胞坏死或凋亡时,碎成片段飘进血液里的遗传物质。
但真实的机制比这更严苛:早期癌症患者的血液里,ctDNA的占比可能不到万分之一,比泳池里的头发还要稀疏。为了揪出它们,技术人员得先把血液里的所有DNA片段捞出来,用高通量测序把每一段都“读”一遍,再用AI算法在海量数据里找肿瘤特有的突变或甲基化标记——就像在一堆碎纸里拼出只有肿瘤才有的“密码”。
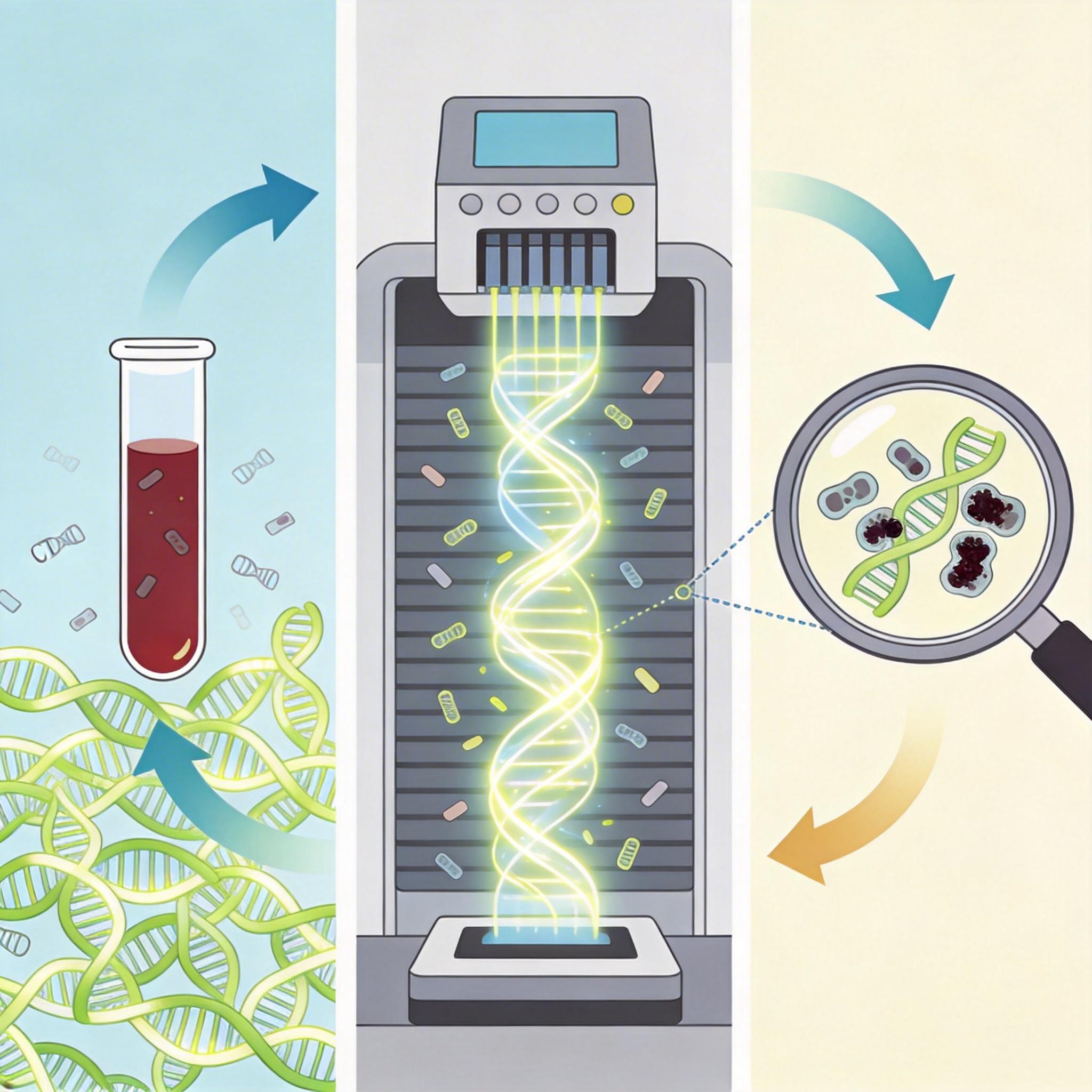
这类检测的核心逻辑,是肿瘤的甲基化模式:正常细胞的DNA甲基化像给基因“盖公章”,决定哪些基因该工作;而肿瘤细胞的“公章”会乱盖,形成独特的甲基化图谱。通过比对这种图谱,不仅能判断有没有癌,还能大致定位是哪个器官出了问题。
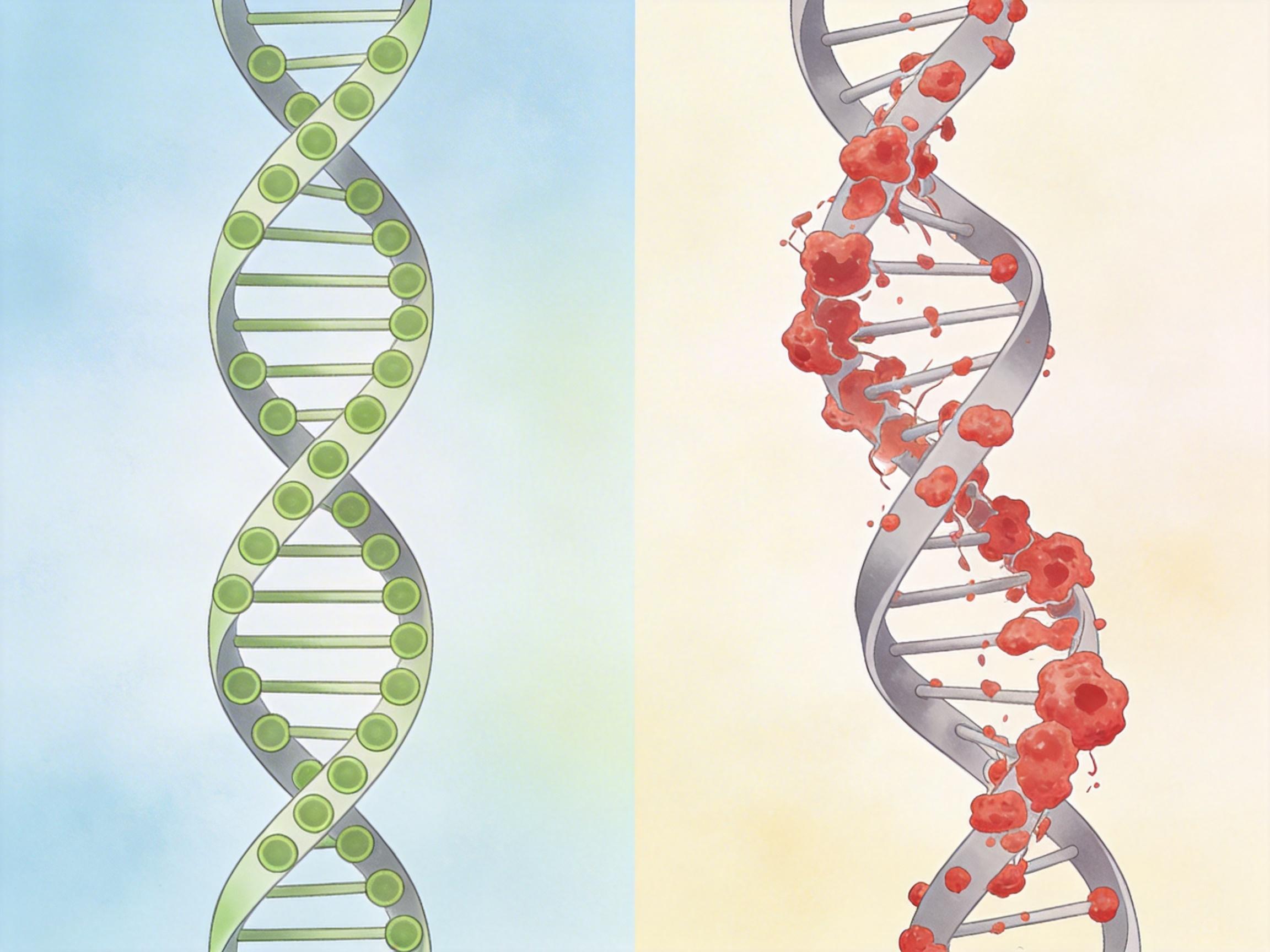
实验室数据看起来很美好:整体能检出约50%的癌症,晚期癌症的检出率甚至能到85%以上。可一旦走进现实,问题就暴露了。
旧金山消防员的试点项目里,1786名受试者中11人测出阳性,最终仅5人确诊癌症——且全都是晚期,剩下6人是假阳性;更扎心的是,有3名检测阴性的消防员,半年内确诊了黑色素瘤、前列腺癌和淋巴瘤。另一项覆盖23000人的试验显示,检测漏掉了196例后来确诊的癌症,还出了83个假阳性。
核心瓶颈就两个:早期信号太弱,以及肿瘤的异质性。早期肿瘤释放的ctDNA少得可怜,现有技术很难精准捕捉;而不同癌种、甚至同一癌种的不同患者,ctDNA的释放量都天差地别——胰腺癌这类“沉默杀手”,可能到晚期才会往血液里释放足够多的信号,而脑瘤受血脑屏障限制,信号根本飘不到血液里。
更麻烦的是“假阳性”:血液里的正常细胞也可能出现类似肿瘤的基因突变,比如老年人常见的“克隆性造血”,会被算法误判为癌症信号,让平白无故的人经历一轮焦虑甚至侵入性检查。
现在的多癌种早筛,更像一个“预警器”,而非“诊断书”。它最大的价值,是填补了传统筛查的空白——比如没有常规筛查手段的胰腺癌、肝癌,一旦出现症状往往已是晚期,血液检测至少能给一部分人争取到早期干预的机会。
但要真正实现“能救命”,还有几道坎要跨:首先是灵敏度,尤其是早期癌症的检出率,目前15%-20%的数值远不足以支撑大规模筛查;其次是标准化,不同实验室的检测流程、算法阈值不统一,结果可能大相径庭;最后是后续诊疗路径,阳性结果后该做哪些检查、如何避免过度诊疗,至今没有统一规范。
成本也是绕不开的坎。单次检测近千美元的价格,让它目前更像“高净值人群的健康选项”。要走进普通大众,不仅技术成本要降,还得等医保覆盖——而这需要更扎实的证据,证明它真的能降低癌症死亡率,而非只是增加发现率。
我最终等到了“未检测到癌症信号”的结果,却没有想象中轻松——我知道这张报告不代表“绝对健康”,只是“当前没抓到信号”。
多癌种早筛的出现,本质上是人类在对抗癌症时的一次“主动出击”:我们不再等症状出现,而是提前在血液里布下天罗地网。但医学的进步从来不是一蹴而就的,它是在无数数据、试错和妥协中慢慢往前挪的。
早筛的本质,是与概率和解。 我们要接受它的不完美,也要相信它的潜力——毕竟,在与癌症的赛跑里,能多提前一步,就多一分胜算。
点击充电,成为大圆镜下一个视频选题!