对抗知识焦虑,从看懂这条开始
App 下载
基因“变体”激增,解开脊椎动物演化之谜?
遗传变异|脊椎动物起源|寒武纪大爆发|全基因组复制|进化生物学|生命科学
对抗知识焦虑,从看懂这条开始
App 下载
遗传变异|脊椎动物起源|寒武纪大爆发|全基因组复制|进化生物学|生命科学
在五亿多年前的寒武纪海洋中,生命正上演着一场前所未有的盛大“派对”——“寒武纪大爆发”。在那个时代,大多数动物的身体构造相对简单,它们是蠕虫、是贝壳、是形态各异的无脊椎生物。然而,就在这片喧嚣的生命舞台上,一支全新的谱系正在悄然崛起。它们将拥有复杂的神经系统、精密的感官、坚固的内部骨骼,并最终演化出鱼类、两栖动物、爬行动物、鸟类和哺乳动物,包括我们人类。它们,就是脊椎动物。这一跃迁是如何发生的?从一个简单的、类似海鞘的生物,到拥有大脑、脊椎和复杂器官的生命形态,其背后的遗传密码究竟隐藏着怎样的秘密?长期以来,科学家们普遍认为全基因组复制事件(WGD)——即整个基因组被复制一或两次——是关键的驱动力,它为演化提供了丰富的“原材料”。但这就像是说,一个建筑师突然拥有了双倍的砖块,却无法完全解释他如何用这些砖块建造出一座宏伟教堂而非两座一模一样的小屋。最近,一项突破性的研究为我们揭示了故事中缺失的关键一环:演化的真正魔术,或许不在于基因数量的简单叠加,而在于如何创造性地“使用”它们。
2026年2月2日,发表在《BMC生物学》(BMC Biology)上的一项研究,为这个宏大的演化谜题提供了惊人的答案。由圣安德鲁斯大学的科学家领导的团队,通过一次巧妙的跨物种比较,捕捉到了生命演化史上的一个决定性瞬间。他们的研究对象堪称演化史上的“活化石”:
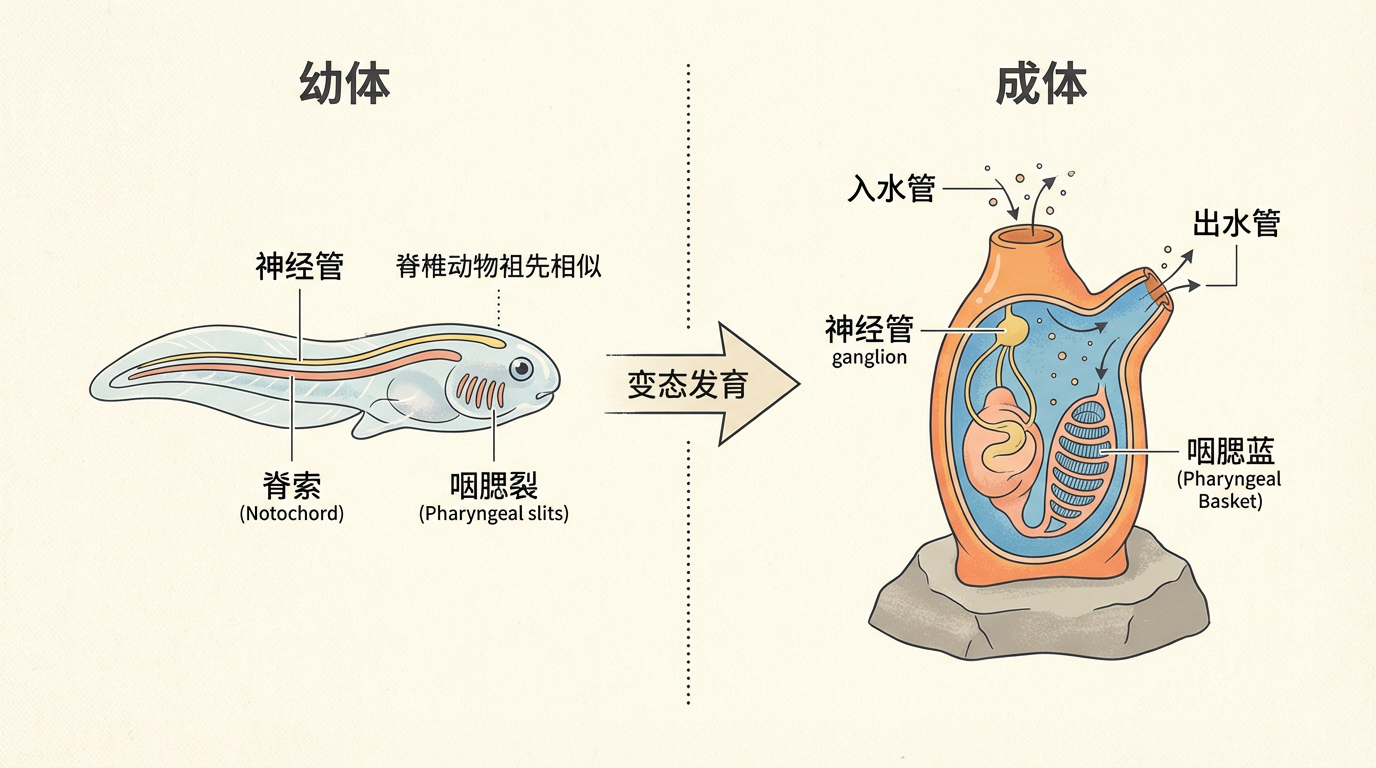
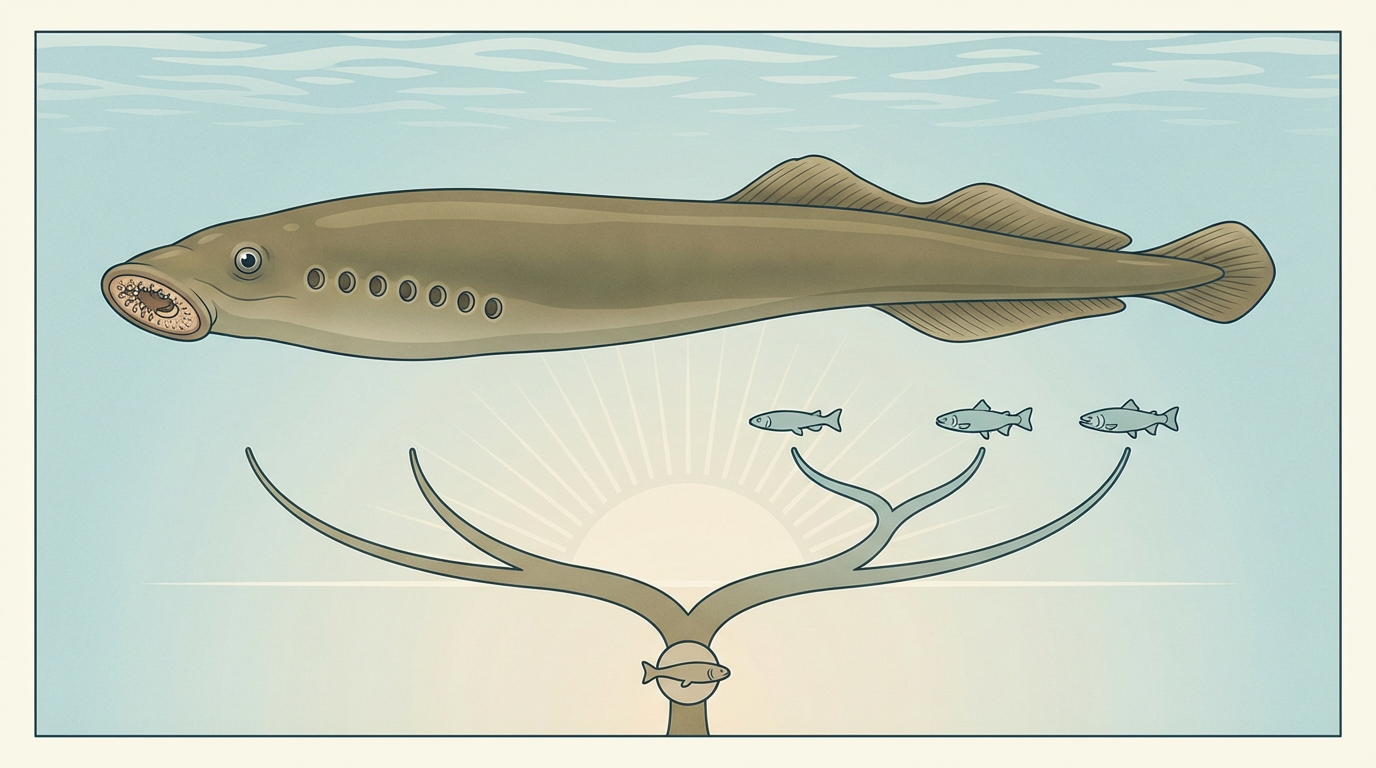
研究团队利用了前沿的长读长DNA测序技术。与传统的短读长测序像是在阅读一本被撕碎的书不同,长读长测序能够一次性读取更长的基因片段,从而以前所未有的清晰度,拼凑出基因表达的完整图景。首席研究员大卫·费里尔(David Ferrier)教授的团队发现,在从海鞘(无脊椎)到七鳃鳗和青蛙(脊椎)的演化节点上,一小部分特定的基因发生了戏剧性的变化。这些基因负责编码细胞间通讯网络中的关键信号输出蛋白——它们就像是细胞内部的“指令调度官”。与海鞘中每个基因主要产生一种蛋白质的模式不同,在七鳃鳗和青蛙体内,**同一个基因竟然能产生出数量庞大、种类繁多的蛋白质“变体”,即蛋白质异构体(isoform)。**这种蛋白质多样性的“爆发式”增长,远远超过了其他类型的基因。这表明,脊椎动物的祖先不仅获得了更多的基因,更重要的是,它们学会了一套“一基因多用”的高效策略。
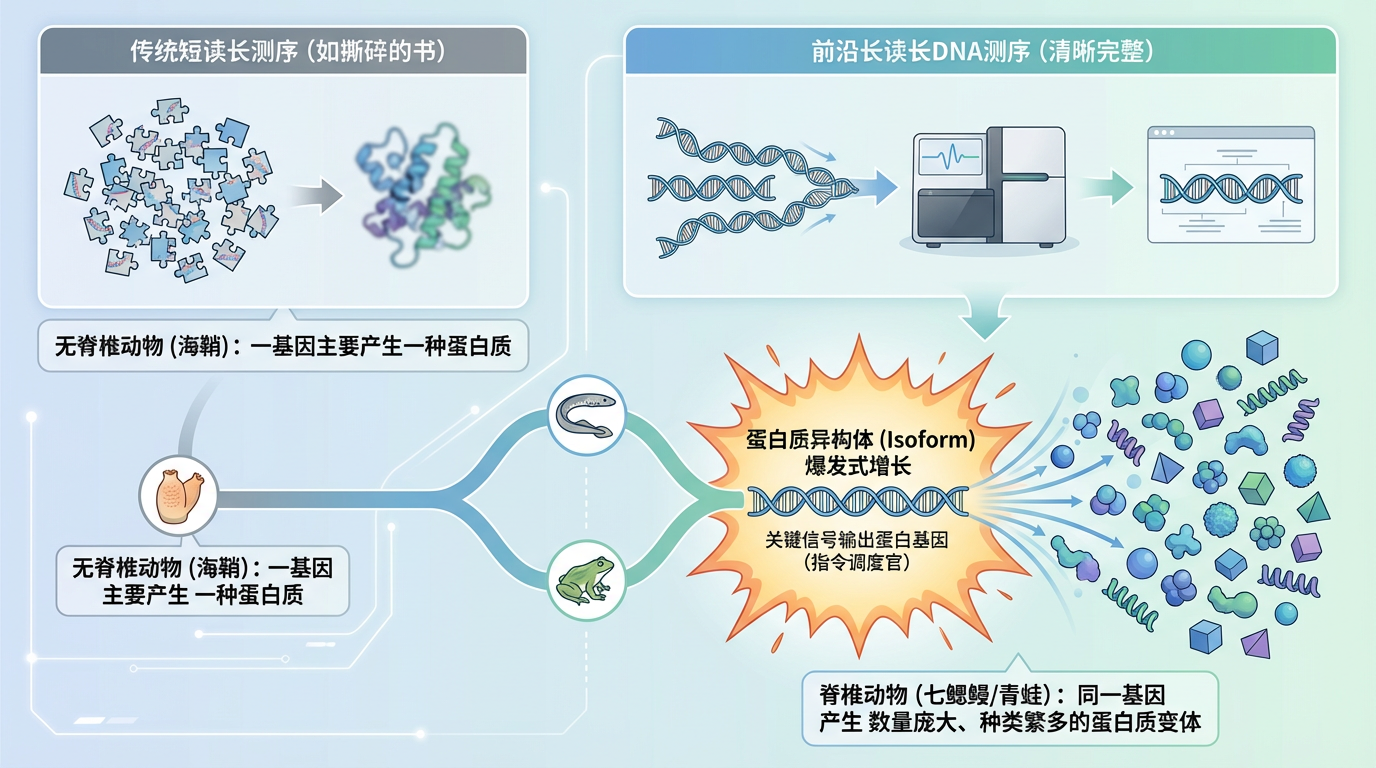
要理解这一发现的重要性,我们首先需要了解什么是蛋白质异构体。想象一个基因是一份核心食谱,通过一种名为“选择性剪接”的分子机制,细胞可以像一位创意厨师一样,对这份食谱进行微调——有时省略某个步骤,有时替换某种配料。这样一来,一份核心食谱就能烹饪出风味各异的多道菜肴。这些不同的“菜肴”,就是功能各异的蛋白质异构体。而细胞信号通路,则像是维持一座城市(生物体)正常运转的庞大通讯网络。从胚胎形成到器官发育,细胞之间无时无刻不在通过这个网络交换信息,决定自己的身份和行为。在这套网络中,费里尔团队发现的那些能产生大量异构体的基因,正扮演着通讯枢纽中“高级调度员”的角色。在简单的无脊椎动物中,一个指令可能只有一个执行方案。但在脊椎动物体内,由于这些“调度员”能产生多种蛋白质变体,一个来自外界的信号可以被解读和执行为多种不同的指令,从而引导细胞分化成神经、肌肉、骨骼等高度特化的类型。正是这种指数级增长的调控复杂性,为构建脊椎动物精密的身体蓝图——包括大脑、心脏和感觉器官——提供了可能。复杂性,源于多样性。
让我们将这一发现置于更宏大的演化时间轴中。大约在5.3亿年前,脊椎动物的祖先经历了至少两次全基因组复制事件。这为演化提供了丰富的基因“硬件”。然而,硬件的堆砌本身并不足以驱动复杂性的飞跃。圣安德鲁斯大学的研究恰恰揭示了与之相伴的“软件”升级。这次蛋白质异构体的激增,正是发生在基因组复制之后,它如同一套全新的操作系统,极大地释放了新增基因的潜力。这解释了为什么像文昌鱼这类拥有脊椎动物祖先基因组雏形的生物,虽然在基因数量上已初具规模,但在身体结构上仍相对简单。它们或许拥有了硬件,却还未完全掌握这套高效的“一谱多曲”的软件。这个“软件”的出现,标志着生命演化从量的积累转向了质的飞跃。它驱动了神经嵴细胞(一种脊椎动物特有的干细胞,能分化成头骨、神经等多种组织)的出现和分化,塑造了我们独特的头部和感官系统,并最终铺就了从海洋游鱼到陆地行者的漫漫长路。
这项研究的意义远不止于改写一本演化教科书。它为我们理解人类自身的健康与疾病,打开了一扇全新的窗户。那些在演化中扮演了关键角色的细胞信号通路,如今依然在我们体内精确地运作着。当这些通路中的基因发生突变,导致蛋白质异构体的产生出现异常时,就可能引发包括癌症、神经退行性疾病和先天性发育缺陷在内的多种疾病。例如,许多癌症的发生,正是因为细胞通讯失控,导致细胞无序增殖。理解这些蛋白质“变体”各自的功能,以及它们是如何协同工作的,将为开发更精准的靶向药物提供新的思路。我们可以不再仅仅针对某一个基因或蛋白质,而是针对性地调节特定异构体的功能,从而在不影响正常细胞功能的情况下,修正致病信号。这不仅是对生命过去的深刻洞察,更是对未来医学的有力启示。正如费里尔教授所言:“确定这些不同的蛋白质形式如何以独特的方式工作,以产生我们现在在脊椎动物中看到的细胞类型多样性,这将是令人兴奋的。”
尽管这一发现具有里程碑意义,但它也开启了更多待解的谜题。我们现在知道了存在一个庞大的蛋白质异构体库,但我们对其中绝大多数成员的具体功能仍然知之甚少。它们各自在胚胎发育的哪个阶段、哪个组织中发挥作用?它们之间是如何相互作用,共同编织出复杂的生命网络?解答这些问题,需要结合单细胞测序、蛋白质组学和功能基因组学等多重技术手段,进行更为深入的探索。这就像是发现了一座巨大的图书馆,我们刚刚完成了书籍的编目,而真正精彩的内容,还隐藏在每一本书的字里行间,等待我们去逐一阅读和理解。
从一颗漂浮在古海洋中的简单细胞,到能够思考宇宙的我们,生命的演化是一部关于复杂性不断涌现的史诗。圣安德鲁斯大学的这项研究,为这部史诗谱写了新的篇章。它告诉我们,生命演化的智慧,不仅在于创造新的基因,更在于以一种近乎艺术的方式,最大化地利用已有的遗传信息。那场发生在五亿年前的基因表达“大爆炸”,是决定我们之所以成为我们的关键一步。它是一曲由基因谱写的、关于多样性、复杂性与创新的颂歌,其悠远的回响,至今仍在我们每一个细胞中激荡。