对抗知识焦虑,从看懂这条开始
App 下载
细胞骨架的致命偏航:一个突变如何让大脑停止生长?
德国灵长类研究所|迷你大脑模型|大脑发育障碍|细胞骨架突变|罕见遗传病|医学健康
对抗知识焦虑,从看懂这条开始
App 下载
德国灵长类研究所|迷你大脑模型|大脑发育障碍|细胞骨架突变|罕见遗传病|医学健康
在构建一座宏伟建筑时,最关键的莫过于其内部钢筋骨架的精确对位。任何微小的偏离,都可能导致整个结构的崩塌。现在,让我们将视线从宏观世界转向生命的微观尺度。在人类大脑这座宇宙间最复杂的“建筑”的早期施工阶段,同样依赖于一个精密的内部支架——细胞骨架。如果这个支架在细胞分裂的瞬间发生一次极其微小的“偏航”,将会引发怎样的连锁反应?一个看似无关紧要的蛋白质突变,是否真的能决定一个大脑的尺寸,甚至一个生命的命运?
2025年12月17日,一则突破性的研究为这个深刻的问题提供了惊人的答案。由德国灵长类研究中心(DPZ)领导的国际科研团队,利用在实验室中培育的“迷你人脑”(脑类器官),成功揭示了一种罕见脑疾病——巴雷特-温特综合征(Baraitser-Winter syndrome)的发生机制。发表于《EMBO Reports》的研究明确指出,一个编码细胞骨架蛋白“肌动蛋白”(actin)的基因发生的单一突变,正是导致部分大脑过早停止生长的元凶。
这项研究的核心发现是:这个微小的突变,像一个错误的指令,扰乱了早期大脑神经祖细胞分裂时的方向。本应垂直分裂以“复制”更多干细胞的祖细胞,被迫转向水平或倾斜分裂,过早地分化成神经元。这个关键的“方向错误”导致了“建筑工人”(祖细胞)的过早枯竭,最终使得大脑这座宏伟建筑因“人手不足”而规模缩减,形成小头畸形(microcephaly)。
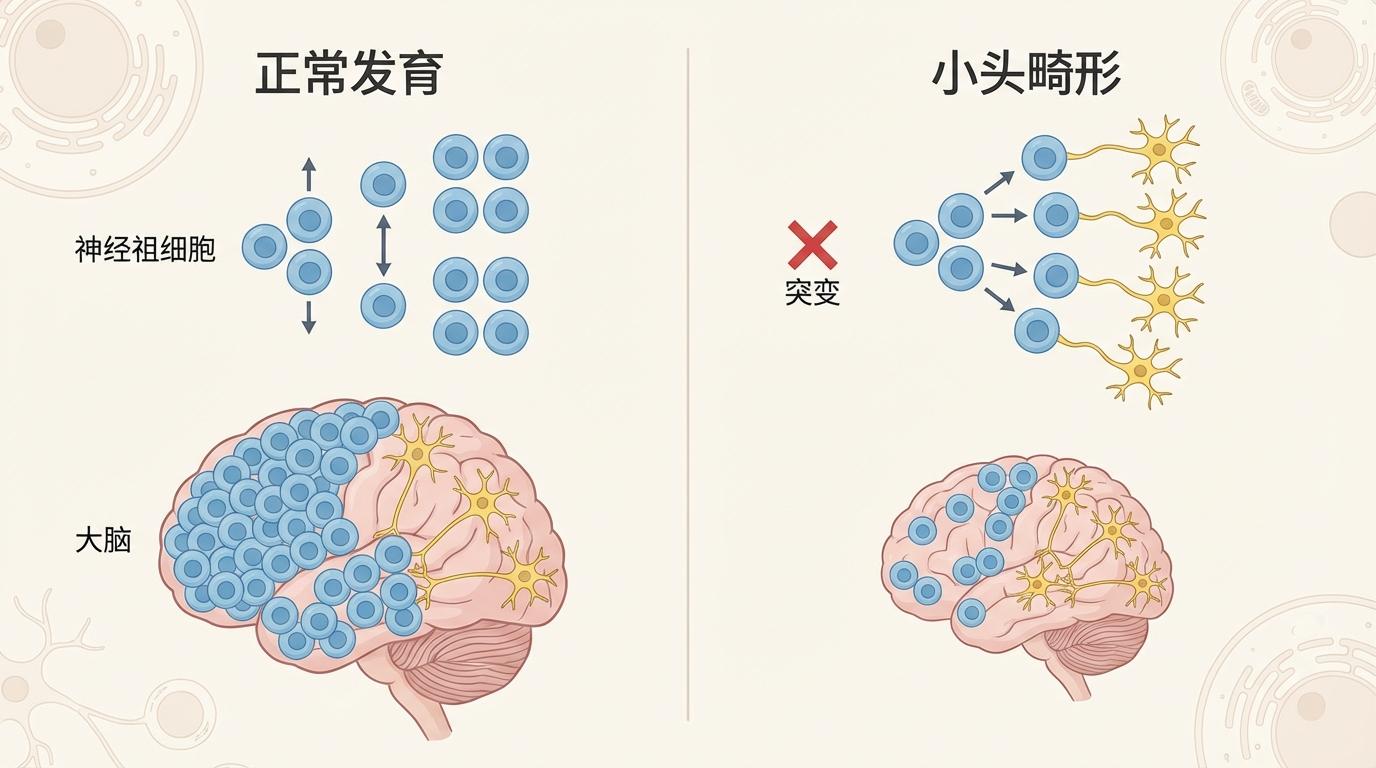
要理解这一发现的重要性,我们必须深入细胞内部,观摩一场名为“分裂”的精妙舞步。细胞骨架不仅是细胞的“钢筋”,更是细胞活动的“编舞指导”。在大脑发育的初期,神经祖细胞是构建大脑皮层的主力军。它们的增殖方式决定了大脑的最终规模。
垂直分裂(对称分裂):当细胞分裂的方向与脑室表面垂直时,就像一个细胞完美地复制了自己,产生两个一模一样的神经祖细胞。这是大脑在发育早期快速扩充“施工队”的关键步骤,确保有足够的细胞储备。
水平或倾斜分裂(不对称分裂):当分裂方向平行或倾斜于脑室表面时,一个祖细胞会分化成一个神经元和一个保留部分干性的基底祖细胞。这标志着大脑开始进入“精装修”阶段,即神经元的生成。
正常的脑发育,是这两种分裂方式在时间和空间上的完美平衡。而肌动蛋白作为细胞骨架的关键成员,正是确保分裂方向精准无误的“舞步节拍器”。
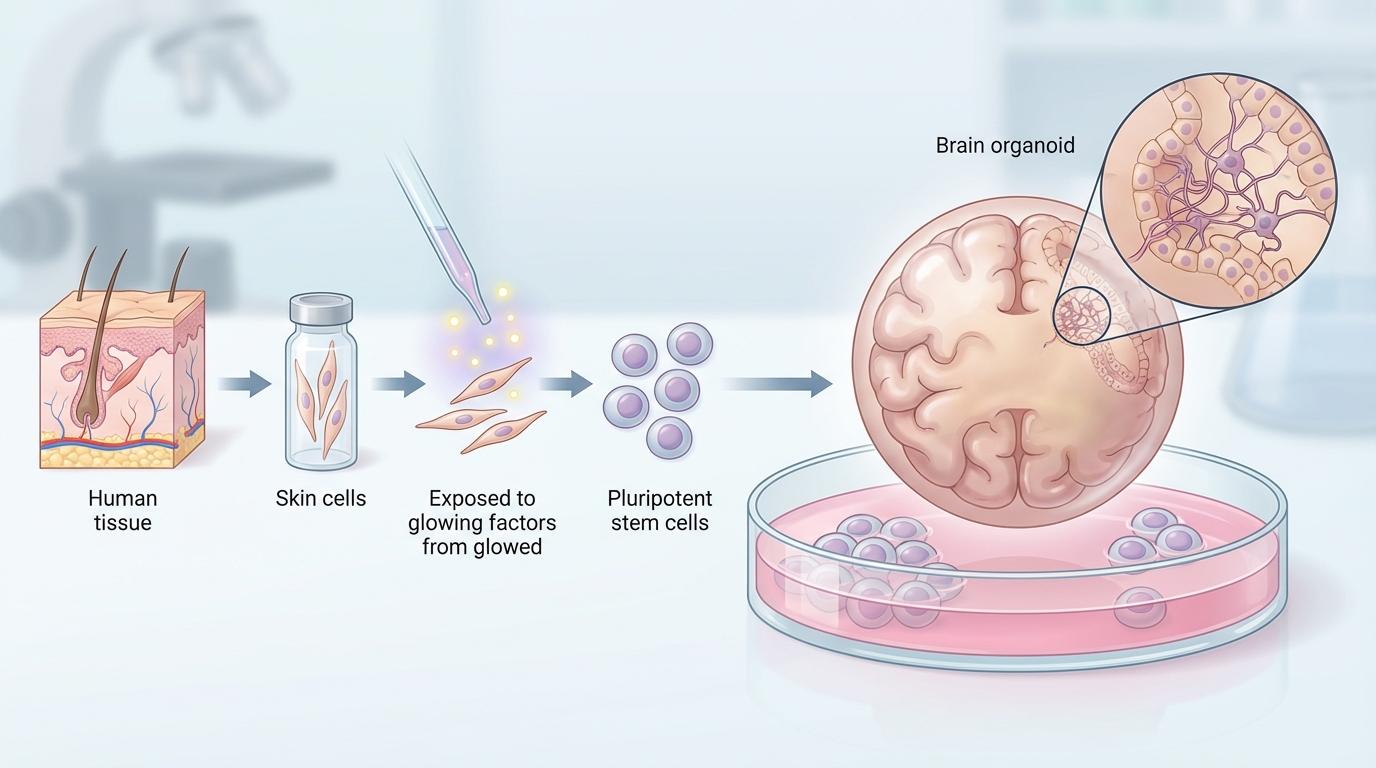
德国的科学家们通过一项巧妙的实验,将这一微观层面的“舞步失误”呈现在世人面前。他们提取了巴雷特-温特综合征患者的皮肤细胞,通过诱导多能干细胞(iPSC)技术,将其“返老还童”为干细胞,随后在培养皿中培育出三维的脑类器官——这些“迷你大脑”复刻了患者大脑的早期发育过程。
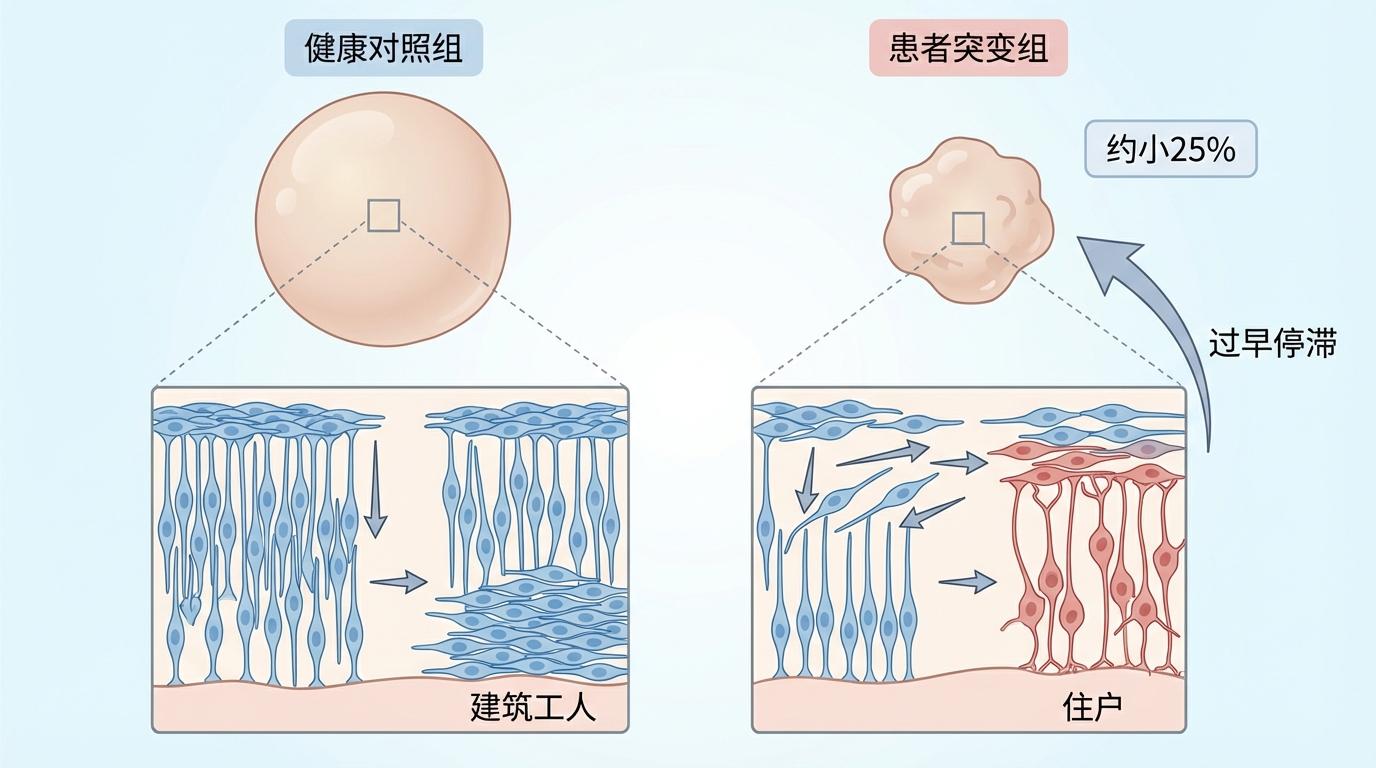
三十天后,结果令人震惊。源自患者细胞的脑类器官,比健康对照组的小了约25%。通过高分辨率显微镜,研究团队清晰地观察到,在携带肌动蛋白突变的类器官中,神经祖细胞的分裂方向发生了戏剧性的偏转。原本占主导地位的垂直分裂变得稀少,取而代之的是大量的水平和倾斜分裂。这意味着,大脑的“建筑工人”过早地被告知“转行”去当“住户”(神经元),导致整个“建筑工程”因劳动力短缺而提前停滞。
为了排除其他遗传因素的干扰,研究团队动用了强大的基因编辑工具CRISPR/Cas9,在健康的干细胞系中精确地引入了这一个突变。结果,这些经过编辑的细胞发育成的脑类器官,完美复现了患者来源类器官的所有缺陷。这无可辩驳地证明,正是肌动蛋白的这一个微小突变,“劫持”了细胞的命运,改写了大脑的发育蓝图。
这项研究的意义远不止于解释一种罕见病。它揭示了一个更为普适的生物学原理:细胞骨架的结构完整性对神经系统的正常发育和功能至关重要。这一发现,为我们理解其他神经发育障碍和脑疾病打开了新的窗口。
注意力缺陷多动障碍(ADHD):近年来的研究发现,一些与ADHD高风险相关的罕见基因突变(如MAP1A、ANK2),其编码的蛋白质同样与细胞骨架的组织和功能密切相关。这暗示着,注意力和冲动控制等高级认知功能,可能也根植于神经元发育过程中细胞骨架的稳定。
大脑衰老:更有研究指出,随着年龄增长,大脑神经元中丝状肌动蛋白(F-actin)的过度积累,会干扰细胞的“垃圾回收系统”(自噬过程),从而加速认知功能的下降。这表明,细胞骨架的动态平衡不仅关乎大脑的“建造”,也关乎其长期的“维护”。
从罕见的小头畸形,到常见的ADHD,再到每个人都将面对的衰老问题,细胞骨架这个微观结构,正以一种超乎想象的方式,深刻影响着我们的大脑健康。
这一里程碑式的发现,为我们带来了什么?
首先是诊断的飞跃。明确了致病基因和机制,使得对此类罕见病的基因诊断更加精准。结合人工智能大模型(如华大基因的GeneT、哈佛的popEVE),医生能够更快地从海量基因数据中锁定致病元凶,为受困家庭提供明确的答案和遗传咨询,结束漫长而痛苦的“诊断之旅”。
其次是治疗的曙光。尽管直接干预胎儿大脑发育在伦理和技术上面临巨大挑战,但这一机制的阐明为未来疗法指明了方向。例如,开发能够稳定细胞骨架、调节肌动蛋白动态平衡的小分子药物,或靶向相关信号通路(如mTOR通路)的药物,可能为部分神经发育障碍提供新的干预策略。
更令人期待的是基因编辑技术的远景。以CRISPR为代表的基因编辑疗法正在迅速发展。虽然直接应用于人脑的基因编辑(如辉大基因针对MECP2重复综合征的临床试验)仍处于早期探索阶段,且面临严格的伦理监管,但它无疑代表了从根本上修正生命“设计图纸”的终极可能。
从一个蛋白质的微小突变,到大脑发育的宏伟蓝图;从一个罕见病家庭的困境,到全人类对大脑奥秘的共同探索。这项研究如同一束光,照亮了生命中最精妙也最脆弱的一环。它告诉我们,大脑的构建是一场不允许失误的精密舞蹈,而科学的使命,正是在这纷繁的舞步中,找到那可能偏离的节拍,并努力为之谱写出重回正轨的希望乐章。